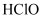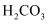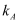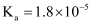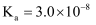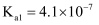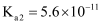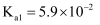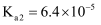第一节 弱电解质的电离 知识点题库
下列说法正确的是( )
A . 等质量的乙烯和丙烯中,所含碳原子数之比为2∶3
B . 等体积、等浓度的NH4Cl溶液和稀氨水中,所含NH4+的数目相等
C . 等物质的量的Cl2分别与足量的Fe和Cu反应,转移的电子数相等
D . 等物质的量的过氧化钡(BaO2)和Ba(OH)2固体中,阴阳离子个数比均为2∶1
下列物质中,属于弱电解质的是( )
A . 氯化氢
B . 氢氧化钠
C . 一水合氨
D . 酒精
欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO 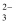 )、c(HCO
)、c(HCO  )都减少,其方法是( )
)都减少,其方法是( )
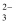 )、c(HCO
)、c(HCO  )都减少,其方法是( )
)都减少,其方法是( )
A . 通入二氧化碳气体
B . 加入氢氧化钠固体
C . 通入氯化氢气体
D . 加入饱和石灰水溶液
甲酸的下列性质中,可以证明它是弱电解质的是( )
A . 0.1mol/L甲酸溶液的c(H+)=10﹣3mol/L
B . 甲酸以任意比与水互溶
C . 10mL 1mol/L甲酸恰好与10mL 1mol/L NaOH溶液完全反应
D . 甲酸溶液的导电性比一元强酸溶液的弱
下列叙述正确的是( )
A . 95℃纯水的pH<7,说明加热可导致水呈酸性
B . 向水中加入少量稀硫酸,c(H+)增大,KW不变
C . 向水中加入氨水,水的电离平衡向正反应方向移动,c(OH﹣)增大
D . pH=3的醋酸溶液,稀释至10倍后pH=4
c(H+)相同的等体积的两份溶液A和B;A为盐酸,B为醋酸,分别和锌反应,若最后仅有一份溶液中存在锌,且放出的氢气的质量相等,则下列说法正确的是( )
①反应所需要的时间B>A
②开始反应时的速率A>B
③参加反应的锌的物质的量A=B
④反应过程的平均速率B>A
⑤盐酸里有锌剩余
⑥醋酸里有锌剩余.
A . ③④⑤
B . ③④⑥
C . ②③⑤
D . ②③⑤⑥
双氧水(H2O2)和水水都是极弱电解质,但H2O2比水更显酸性.
-
(1) 若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:
-
(2) 鉴于H2O2显弱酸性,它能同强碱作用形成正盐,在一定条件下也可以形成酸式盐.请写出H2O2与Ba(OH)2作用形成正盐的化学方程式:
-
(3) 水电离生成H3O+ 和OH﹣叫做水的自偶电离.同水一样,H2O2也有极微弱的自偶电离,其自偶电离方程式为:.
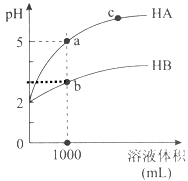
室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如下图所示:
-
(1) HB溶液体积稀释到1000毫升时,溶液中c(H+)=mol/L。
-
(2) 由图可判断:HA的酸性(填“>”或“<”)HB的酸性。
-
(3) pH均为2的一元酸HA和HB各1mL,分别加水稀释后pH不同的原因是什么?请进行完整说明。
有0.1 mol/L的盐酸(a)、硫酸溶液(b)、醋酸溶液(c)各50 mL,试比较:
-
(1) 三种酸的氢离子浓度由大到小的顺序是;三种酸的pH由大到小的顺序是(填字母代号,下同)。
-
(2) 三种酸跟足量的锌反应,开始时产生H2的速率由大到小的顺序是(不考虑Zn的纯度及表面积等问题)。
-
(3) 三种酸跟足量的锌反应产生H2的体积由大到小的顺序是。
-
(4) 三种酸分别跟0.1 mol/L的NaOH溶液中和,消耗NaOH溶液的体积由大到小的顺序是。
下列图示与对应的叙述相符的是()

A . 图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则等物质的量浓度的NaA和NaB混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
B . 图2中在b点对应温度下,将pH=2的H2SO4溶液与pH=12的NaOH溶液等体积混合后,溶液显中性
C . 用0.0100mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/LCl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl-
D . 图4表示在N2(g)+3H2(g)  2NH3(g)达到平衡后,减小NH3浓度时速率的变化
2NH3(g)达到平衡后,减小NH3浓度时速率的变化
 2NH3(g)达到平衡后,减小NH3浓度时速率的变化
2NH3(g)达到平衡后,减小NH3浓度时速率的变化
常温下,向10 mL0.1 mol/L的HR溶液中逐滴加入0.1 mol/L的氨水,所得溶液pH及导电能力变化如图。下列分析正确的是( )
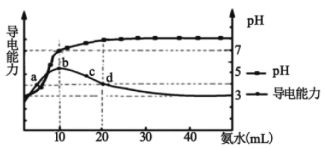
A . 各点溶液中的阳离子浓度总和大小关系:d>c>b>a
B . 常温下,R- 的水解平衡常数数量级为10 -9
C . a点和d点溶液中,水的电离程度相等
D . d点的溶液中,微粒浓度关系:c(R-)+2c(HR)=c(NH3∙H2O)
常温下pH=3的二元弱酸H2R溶液与a L pH=11的NaOH溶液混合后,混合液的pH刚好等于7(假设反应前后体积不变),则对反应后混合液的叙述正确的是( )
A . c(R2-)+ c(OH-)=c(Na+)+c(H+)
B . c(R2-)>c(Na+)>c(H+)=c(OH-)
C . 2c(R2-)+ c(HR-)=c(Na+)
D . 混合后溶液的体积为2a L
相同温度下,关于盐酸和醋酸溶液的说法正确的是( )
A . pH相等的两溶液:c(CH3COO-)=c(Cl-)
B . pH=3盐酸和醋酸溶液,等体积混合后溶液的pH>3
C . 浓度均为0.1mol·L−1盐酸和醋酸溶液,导电能力相同
D . 相同浓度的两溶液,分别与NaOH固体反应后呈中性的溶液中(忽略溶液体积变化)c(CH3COO-)=c(Cl-)
下列实验的操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | NaHCO3溶液与 NaAlO2溶液混合 | 生成白色沉淀 | 结合H+的能力:CO |
| B | 常温下,相同的铝片分别投入足量的稀、浓硫中 | 浓硫酸中铝片先溶解完 | 反应物浓度越大,反应速率越快 |
| C | 对装在针筒内的NO2气体推动活塞加压 | 气体颜色加深 | 平衡 |
| D | 2 mL 0.1 mol/L的NaOH溶液中滴加2滴0.1 mol/L的MgCl2溶液,再滴加2滴0.1 mol/L的FeCl3溶液 | 白色沉淀转化为红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
A . A
B . B
C . C
D . D
25℃时,用  溶液滴定某二元弱酸
溶液滴定某二元弱酸  ,
,  被滴定分数
被滴定分数  、pH及微粒分布分数
、pH及微粒分布分数 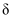 [
[ 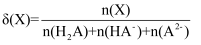 ,X表示
,X表示  、
、 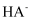 或
或 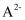 ]的关系如图所示:
]的关系如图所示:
 溶液滴定某二元弱酸
溶液滴定某二元弱酸  ,
,  被滴定分数
被滴定分数  、pH及微粒分布分数
、pH及微粒分布分数 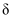 [
[ 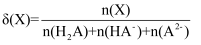 ,X表示
,X表示  、
、 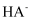 或
或 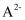 ]的关系如图所示:
]的关系如图所示:
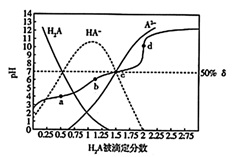
下列说法错误的是( )
A .  点溶液中溶质为
点溶液中溶质为 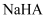 和
和  B .
B .  点溶液中:
点溶液中: 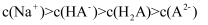 C .
C .  点溶液中:
点溶液中: 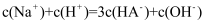 D . a、b、c、d四点溶液中水的电离程度:
D . a、b、c、d四点溶液中水的电离程度: 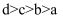
 点溶液中溶质为
点溶液中溶质为 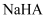 和
和  B .
B .  点溶液中:
点溶液中: 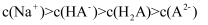 C .
C .  点溶液中:
点溶液中: 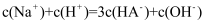 D . a、b、c、d四点溶液中水的电离程度:
D . a、b、c、d四点溶液中水的电离程度: 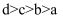
25℃,下列说法正确的是( )
A . 某溶液由水电离出 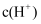 为
为  ,则该溶液可能是酸,也可能是盐
B . 将pH=3的
,则该溶液可能是酸,也可能是盐
B . 将pH=3的  加水稀释10倍,测得pH为4.则可证明
加水稀释10倍,测得pH为4.则可证明  为强酸
C . 测NaHA溶液的pH,若
为强酸
C . 测NaHA溶液的pH,若 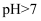 ,则
,则  是弱酸;若
是弱酸;若 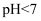 ,则
,则  是强酸
D . 同浓度、体积之比为1∶2的
是强酸
D . 同浓度、体积之比为1∶2的  溶液和NaOH溶液恰好完全反应,可证明
溶液和NaOH溶液恰好完全反应,可证明  是强酸
是强酸
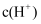 为
为  ,则该溶液可能是酸,也可能是盐
B . 将pH=3的
,则该溶液可能是酸,也可能是盐
B . 将pH=3的  加水稀释10倍,测得pH为4.则可证明
加水稀释10倍,测得pH为4.则可证明  为强酸
C . 测NaHA溶液的pH,若
为强酸
C . 测NaHA溶液的pH,若 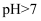 ,则
,则  是弱酸;若
是弱酸;若 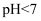 ,则
,则  是强酸
D . 同浓度、体积之比为1∶2的
是强酸
D . 同浓度、体积之比为1∶2的  溶液和NaOH溶液恰好完全反应,可证明
溶液和NaOH溶液恰好完全反应,可证明  是强酸
是强酸
下列说法正确的是( )
A . pH=1 的醋酸加水稀释到原体积的 1000 倍,稀释后 pH=4
B . 某温度下,某溶液中水电离出的 c(H+)=1×10-7 mol·L-1 , 则该温度下溶液呈中性
C . 室温下pH相同的NH4Cl溶液和CH3COOH溶液,由水电离产生的c(H+)相同
D . 其它条件相同时,同浓度同体积的CH3COOH 溶液和盐酸分别与镁反应,CH3COOH溶液反应放出气体的速率较慢
下表是25℃时某些弱酸的电离平衡常数
|
化学式 |
| | | |
| | | | | |
-
(1) 常温时,向冰醋酸加水稀释过程中溶液的导电能力Ⅰ随加入水的体积V变化的曲线如右图所示,则a、b、c三点处,溶液中pH值最小的点为,醋酸的电离程度最大的点为;
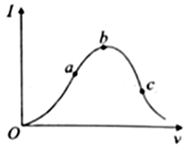
-
(2) 物质的量浓度均为
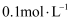 的四种溶液:
的四种溶液: ①
 ②
②  ③
③ 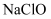 ④
④ 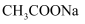
水的电离程度由小到大的顺序为;
-
(3) 向
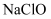 溶液中通入少量CO2的化学方程式为;
溶液中通入少量CO2的化学方程式为;
-
(4) 在25℃时向
 溶液中滴加
溶液中滴加 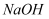 溶液至:
溶液至: 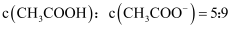 ,此时溶液的
,此时溶液的 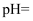 .
.
-
(5)
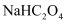 溶液呈(填“酸性”“中性”“碱性”),试简述其原因;
溶液呈(填“酸性”“中性”“碱性”),试简述其原因;
下列物质属于强电解质的是( )
A . CH3COOH
B . H2SO4溶液
C . Na2SO4固体
D . C2H5OH(乙醇)
大气中 含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(
含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(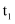 ,
,  )海水中
)海水中 浓度与模拟空气中
浓度与模拟空气中 浓度的关系曲线。下列说法错误的是( )
浓度的关系曲线。下列说法错误的是( )
 含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(
含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(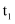 ,
,  )海水中
)海水中 浓度与模拟空气中
浓度与模拟空气中 浓度的关系曲线。下列说法错误的是( )
浓度的关系曲线。下列说法错误的是( )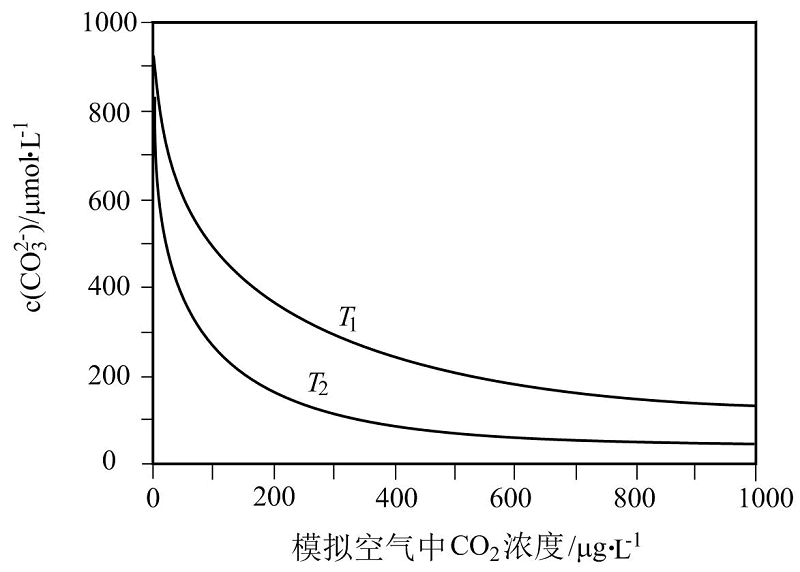
A . 海水温度一定时,大气中 浓度增加,海水中溶解的
浓度增加,海水中溶解的 随之增大,导致
随之增大,导致 浓度降低
B . 大气中
浓度降低
B . 大气中 含量增加时,海水中的珊瑚礁溶解的反应为:
含量增加时,海水中的珊瑚礁溶解的反应为: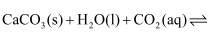
 C . 当大气中
C . 当大气中 浓度确定时,海水温度越高,则
浓度确定时,海水温度越高,则 浓度越低
D . 海水呈弱碱性,是铝、铁元素在海水中含量少,而在陆地含量高的原因
浓度越低
D . 海水呈弱碱性,是铝、铁元素在海水中含量少,而在陆地含量高的原因
 浓度增加,海水中溶解的
浓度增加,海水中溶解的 随之增大,导致
随之增大,导致 浓度降低
B . 大气中
浓度降低
B . 大气中 含量增加时,海水中的珊瑚礁溶解的反应为:
含量增加时,海水中的珊瑚礁溶解的反应为: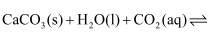
 C . 当大气中
C . 当大气中 浓度确定时,海水温度越高,则
浓度确定时,海水温度越高,则 浓度越低
D . 海水呈弱碱性,是铝、铁元素在海水中含量少,而在陆地含量高的原因
浓度越低
D . 海水呈弱碱性,是铝、铁元素在海水中含量少,而在陆地含量高的原因
最近更新
- 决定下列农业区位选择的主导因素分别是:①华南的双季稻种植;②宁夏平原的水稻种植;③新疆哈密盆地的瓜果生产;④上海郊区的乳
- 第二节:完形填空(共20小题;每小题1.5分,满分30分) 阅读下面短文,从短文后所给各题的四个选项(A、B、C
- 下图为反射弧模式图,则A.神经冲动在②和④上以局部电流的形式传导 B.兴奋传导方向是⑤→④→③→②→① C.②受损时,刺
- Computer programmer David Jones earns $35.000 a year designi
- 过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,
- 化学与生活密切相关. (1)日常生活中经常接触的金属材料多数是合金,当金属制成合金后,性能会发生改变.如黄铜制的钥匙能在
- 读“某城市某功能区内的日均地铁分时段客运量统计图”,回答下题。关于该功能区的说法正确的( ) A.工厂企业集中
- It was funny to see that the dog’s eyes immediately _______
- 已知函数f(x)=|x+1|,g(x)=2|x|+a. (1)当a=0时,解不等式f(x)≥g(x);(2)若存在x∈R
- 如图所示的电路,一灯泡和一可变电容器串联,下列说法正确的是 A.a、b端接稳恒直流电,灯泡发亮B.a、b端接交变电
- 如图所示,已知△OAB中,点C是以点A为中心的点B的对称点,点D是将分成2∶1的一个内分点,DC和OA交于点E,设=a,
- 武汉大学公共卫生学院罗琼博士等的一项最新研究发现,海带的提取物——海带多糖因抑制免疫细胞凋亡而具有抗辐射作用。对以上事实
- 阅读下面这首唐诗,完成后面题。 长门怨 齐浣 宫殿沉沉月欲分,昭阳①更漏②不堪闻。 珊瑚枕上千行泪,不是思君是恨君。 【
- 史载唐高宗在位时期处理的政务,将近300件,发现其中20多件有武则天参加,但大多是有关外戚和后宫的事务,而任命宰相、将领
- 根据拼音写汉字,并给加点的字注音。 人一辈子都在高潮——低潮中浮沉,惟有________(yōng)碌的人,生活才如死水
- 某烃分子结构中含一个苯环、两个碳碳双键和一个碳碳三键,它的分子式可能为A.C9H12 B.C12H
- 人们将一种叫“水葫芦”的植物引种到昆明滇池后,这种植物很快在滇池中蔓延,甚至威胁到其它生物的生存。这说明了( )A.
- 椭圆ax2+by2=1与直线y=1-x交于A、B两点,过原点与线段AB中点的直线的斜率为,则的值为( )A.
- 2021 年 7 月,河南省郑州、新乡等地因暴雨市区内涝严重,遭受重大损失。险情发生以后,中铝国际所属各建设等单位在豫项
- 阅读下面的古诗文,完成以下各题。(甲)东临碣石,以观沧海。水何澹澹,山岛竦峙。树木丛生,百草丰茂。秋风萧瑟,洪波涌起。日
 <AlO
<AlO 
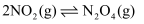 加压逆向移动
加压逆向移动