第四节 离子晶体 知识点题库
下列有关比较中,大小顺序排列错误的是( )
A . 热稳定性:NH3>PH3>H2S
B . 物质的熔点:石英>食盐>冰>干冰
C . 结合H+的能力:CO32﹣>CH3COO﹣>Cl﹣
D . 分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
下列物质属于含有共价键的离子化合物的是( )
A . Na2O2
B . H2O
C . MgCl2
D . N2
氮是地球上极为丰富的元素.填写下列空白.
(1)常温下,锂可与氮气直接反应生成Li3N,Li3N晶体中氮以N3﹣存在,基态N3﹣的电子排布式为: ,Li3N晶体属于 晶体(填晶体类型).
(2)CO与N2相似,分子中都存在一个共价叁键,CO含 个π键.
(3)根据下表数据,写出氮气与氢气反应生成氨气的热化学方程式.
化学键 | N﹣N | N=N | N≡N | N﹣H | H﹣H |
键能/kJ•mol﹣1 | 159 | 418 | 946 | 391 | 436 |
(4)氮化硅是一种高温陶瓷材料,它硬度大、熔点高、化学性质稳定.
①氮化硅晶体属于 晶体(填晶体类型);
②已知氮化硅晶体结构中,原子间都以共价键相连,且N原子与N原子,Si原子与Si原子不直接相连,同时每个原子都满足8电子结构,请写出氮化硅的化学式: .
(5)极纯的氮气可由叠氮化钠(NaN3)加热分解而得到.2NaN3(s)=2Na(l)+3N2(g),反应过程中,断裂的化学键是离子键和共价键,形成的化学键有
下列推论正确的( )
A . SiH4的沸点高于CH4 , 可推测pH3的沸点高于NH3
B . NH  为正四面体,可推测出PH
为正四面体,可推测出PH  也为正四面体结构
C . CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体
D . C2H6是碳链为直线型的非极性分子,可推测C3H8也是碳链为直线型的非极性分子
也为正四面体结构
C . CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体
D . C2H6是碳链为直线型的非极性分子,可推测C3H8也是碳链为直线型的非极性分子
 为正四面体,可推测出PH
为正四面体,可推测出PH  也为正四面体结构
C . CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体
D . C2H6是碳链为直线型的非极性分子,可推测C3H8也是碳链为直线型的非极性分子
也为正四面体结构
C . CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体
D . C2H6是碳链为直线型的非极性分子,可推测C3H8也是碳链为直线型的非极性分子
下列过程中离子键被破坏的是( )
A . HCl晶体溶于水
B . 在氧气中点燃氢气
C . 冰熔化为液态水
D . NaCl晶体受热熔化
下面的排序正确的是( )
A . 硬度由大到小:金刚石>碳化硅>晶体硅
B . 熔点由高到低:SiC>Si>SiO2>Ge
C . 沸点由高到低:NH3>PH3>AsH3>SbH3
D . 晶格能由大到小:NaI>NaBr>NaCl>NaF
下列物质属于分子晶体且是化合物的是( )
A . 石英
B . 食盐
C . 干冰
D . 碘
下列六种物质的变化中,将合适序号填写在下列空白中:
①干冰的升华; ②硫酸钾熔化; ③NaCl溶于水; ④HCl溶于水; ⑤液氨的受热蒸发; ⑥Na2O2溶于水
-
(1) 仅需要克服分子间作用力的是
-
(2) 发生离子键破坏,又发生共价键破坏的是
-
(3) 发生共价键破坏的是
-
(4) 发生离子键破坏的是.
下列说法正确的是( )
A . 离子键是阴、阳离子间存在的静电引力
B . 只有金属和非金属化合时才能形成离子键
C . 含有离子键的化合物一定是离子化合物
D . 第ⅠA族和第ⅦA族元素原子化合时,一定形成离子化合物
据报道美国准备试验绿色航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,结构如图,它比肼燃烧释放能量更高,更安全、环保。下列说法错误的是( )
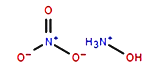
A . 羟基硝酸铵中各原子共平面
B . 固态时羟基硝酸铵是离子晶体
C . 羟基硝酸铵中含有离子键和共价键
D . 9.6g羟基硝酸铵中含有0.2NA个离子
钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法正确的是( )
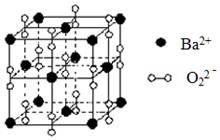
A . 与每个Ba2+距离相等且最近的Ba2+共有6个
B . 晶体中Ba2+的配位数为8
C . 晶体的化学式为Ba2O2
D . 该氧化物是含有非极性键的离子化合物
下列各组物质熔化或气化时,所克服的微粒间的作用力属同种类型的是( )
A . SiO2和CaO的熔化
B . 氧化钠和铁的熔化
C . 碘和干冰的气化
D . 晶体硅和晶体硫的熔化
氮化镓( 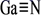 )材料具有低的热产生率和高的击穿电场,是制造大功率和高频微波电子器件的理想半导体材料。
)材料具有低的热产生率和高的击穿电场,是制造大功率和高频微波电子器件的理想半导体材料。
已知:①Ga和Al同主族且相邻,化学性质与铝相似;②在室温下,氮化镓不溶于水,硬度高,熔点高,能与热的碱溶液缓慢反应。
-
(1) 配平氮化镓制备的化学方程式:□Ga(l)+□NH3(g)⇌□GaN(s)+□H2(g)+QkJ(Q>0)
-
(2) 上述反应的平衡常数表达式K=;在恒温恒容密闭容器中制备氮化镓,下列有关说法正确的是
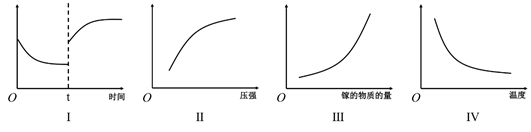
A.Ⅰ图像中如果纵坐标为正反应速率,则t时刻改变的条件可能是加压
B.Ⅱ图像中纵坐标可以为镓的转化率
C.Ⅲ图像中纵坐标可以为化学反应速率
D.Ⅳ图像中纵坐标可以为平衡常数
-
(3) Ga最外层电子的核外电子排布式,N核外能量最高的电子亚层上电子云空间伸展方向有种;
-
(4) 氮化镓的晶体类型,氮化铝和氮化镓晶体类型相同,且结构相似,比较两者熔点的高低并解释原因;
-
(5) 写出氮化镓溶于热的NaOH溶液的离子方程式。
下列说法正确的是( )
A . 氯气通入水中,有化学键的断裂与形成
B . HF、HCl、HBr、HI 的分子间作用力依次增大
C . CH4和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构
D . 某晶体固态时不导电,水溶液能导电,说明该晶体是离子晶体
三草酸合铁酸钾(  )是制备铁触媒的主要原料。该配合物在光照下发生分解:
)是制备铁触媒的主要原料。该配合物在光照下发生分解:  。下列说法错误的是( )
。下列说法错误的是( )
 )是制备铁触媒的主要原料。该配合物在光照下发生分解:
)是制备铁触媒的主要原料。该配合物在光照下发生分解:  。下列说法错误的是( )
。下列说法错误的是( )
A . Fe3+的最高能层电子排布式为 3d5
B .  中铁离子的配位数为 6
C .
中铁离子的配位数为 6
C .  中 C原子的杂化方式为 sp2
D . CO2 分子中σ键和π键数目比为1:1
中 C原子的杂化方式为 sp2
D . CO2 分子中σ键和π键数目比为1:1
 中铁离子的配位数为 6
C .
中铁离子的配位数为 6
C .  中 C原子的杂化方式为 sp2
D . CO2 分子中σ键和π键数目比为1:1
中 C原子的杂化方式为 sp2
D . CO2 分子中σ键和π键数目比为1:1
下列物质中含有共价键的离子化合物的是( )
A . KOH
B . Na2O
C . CaCl2
D . HCl
氧化锌在液晶显示器、薄膜晶体管、发光二极管等产品中均有应用,常用下列三种锌盐为原料经高温分解制备。
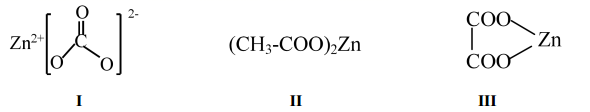
回答下列问题:
-
(1) Zn为30号元素,它在元素周期表中的位置是。
-
(2) 原料Ⅰ中阴离子空间结构为,其等电子体为(写出1种即可)。
-
(3) 原料Ⅱ、Ⅲ阴离子对应的酸沸点较高的是(写结构简式),原因是。
-
(4) 关于以上几种锌盐说法正确的是____。A . 化合物Ⅱ中电负性最大的元素是O B . 化合物Ⅱ中所有C原子的杂化形式均为sp3 C . 化合物Ⅲ中只存在离子键和极性共价键 D . 化合物Ⅰ阴离子中σ键和π键数目比为2:1
-
(5) ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,下图为这两种晶体的局部结构。
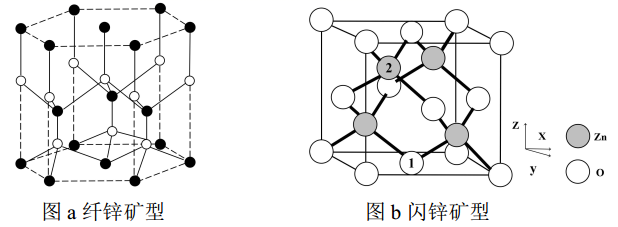
①图a不是纤锌矿型ZnO的晶胞单元,原因是。
②图b闪锌矿型属于立方晶胞,原子1的坐标为
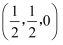 , 则原子2的坐标为。
, 则原子2的坐标为。③图
 的闪锌矿型ZnO晶体中离O距离最近的Zn原子数为,其晶胞参数为a nm,阿伏加德罗常数的值为NA , 则晶体密度为g/cm3(列出计算式)。
的闪锌矿型ZnO晶体中离O距离最近的Zn原子数为,其晶胞参数为a nm,阿伏加德罗常数的值为NA , 则晶体密度为g/cm3(列出计算式)。
Co3+的八面体配合物CoClm·nNH3中配离子的空间构型如图所示,其中数字处的小圆圈表示NH3分子或Cl,Co3+位于八面体的中心。若1mol配合物与足量AgNO3溶液作用生成1molAgCl沉淀,则n的值是( )
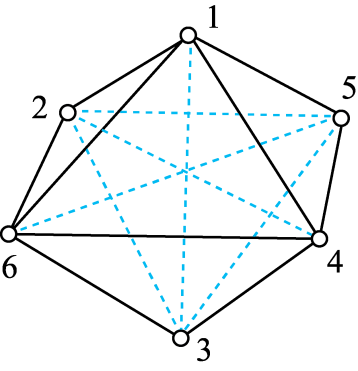
A . 2
B . 3
C . 4
D . 5
三氯化磷( )在农业、医药工业、染料工业有广泛应用。有关说法正确的是( )
)在农业、医药工业、染料工业有广泛应用。有关说法正确的是( )
 )在农业、医药工业、染料工业有广泛应用。有关说法正确的是( )
)在农业、医药工业、染料工业有广泛应用。有关说法正确的是( )
A .  的分子结构为正三角形
B .
的分子结构为正三角形
B .  分子中不含孤电子对
C .
分子中不含孤电子对
C .  中P为
中P为 杂化
D .
杂化
D .  是非极性分子
是非极性分子
 的分子结构为正三角形
B .
的分子结构为正三角形
B .  分子中不含孤电子对
C .
分子中不含孤电子对
C .  中P为
中P为 杂化
D .
杂化
D .  是非极性分子
是非极性分子
如图表示一些晶体中的某些结构,下列各项所述错误的是( )
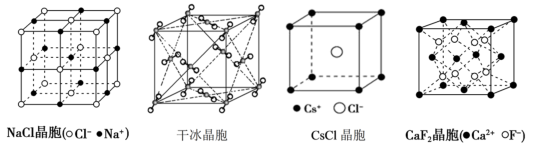
A . 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B . 干冰晶体中二氧化碳分子的取向不完全相同
C . 氯化铯晶体中,每个Cs+周围距离最近的Cs+个数为8个
D . 在CaF2晶体中,每个晶胞平均占有4个Ca2+
最近更新
- 小华在电话中问小明:“已知一个三角形三边长分别是4,9,12,如何求这个三角形的面积?小明提示说:“可通过作最长边上的高
- 2.把下列句子组成语意连贯的语段,排序最恰当的一组是 当然,好的故事在结尾的地方一定要给读者或观众一把开悟的钥匙,要让读
- 下列有关物质的用途,利用了物理性质的是() A.稀有气体用来制作电光源 B.氮气用于填充灯泡 C.双氧水用于制
- -Where's Shirley? -I saw her _______a few minutesago. A
- 制备乙酸乙酯的一条合成路线为: 下列说法错误的是 A.乙的结构简式为CH3COOCH2CH3
- 在恒容密闭容器中通入X并发生反应:2X(g)Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示
- 下列各项中,在适宜的外界条件下能够萌发的种子是A.收获不久的小麦种子 B.煮熟的小麦种子C.去掉胚乳的小麦
- 我国每个节日都是一道独特的风景线,请从下面两个节日中任选一个,仿用例句,各用一句话表现它们的特点。要求:内容符合节日特点
- 某同学设计了如图所示的装置来探究加速度与力的关系。弹簧秤固定在一合适的木板上,桌面的右边缘固定一支表面光滑的铅笔以代替定
- 阅读材料,完成问题: 2000年,全英几百万大中学生参加了一个调查——你认为在过去的一千年里,谁对全世界的贡
- (2011年四川绵阳,17题)相同质量的Mg、Fe分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸
- I’d been 16 for six days and was already prepared to deal wi
- 台湾著名诗人余光中在《乡愁》中写道:“小时候,乡愁是一枚小小的邮票,我在这头,母亲在那头;长大后,乡愁是一张窄窄的船票,
- (2009山东烟台质检,20)有人评价赫鲁晓夫“是徘徊在新旧时代十字路口的一名代表人物,他的一只脚跨进了新时代,而另一只
- 下列有关细胞的叙述中不正确的一项是( ) A.植物体内,分生组织的细胞能分化形成其他组织B.草履虫体内,物质
- M________a foreign language is a must in international trade
- made the school proud was morethan 90%of the s
- 我国的“三北”防护林是一项规模空前的生态建设工程,被誉为“绿色万里长城建设工程”。下列不属于植树造林在保护环境方面要求的
- 考点: 电容器的动态分析.专题: 电容器专题. 分析: 静电计测定电容器极板间的电势差,电势差越大,指针的偏角越大
- 下列各组词语中,加点的字读音全都相同的一组是( ) A.望风披靡 糜烂不堪 受人羁縻 弭除成见 B.恪守



