第一节 共价键 知识点题库
由原子轨道相互重叠形成的σ键和π键总称价键轨道,是分子结构的价键理论中最基本的组成部分。关于该理论下列有关认识不正确的是( )
A . σ键不属于共价键,是另一种化学键
B . s-sσ键与s-pσ键的对称性相同
C . 分子中含有共价键,则至少含有一个σ键
D . 含有π键的化合物与只含σ键的化合物的化学性质不同
下列物质中,化学键类型和分子空间构型皆相同的是( )
A . CO2和SO3
B . CH4和SiH4
C . BF3和PH3
D . HCl和NH4Cl
下列说法正确的是( )
A . NaCl固体中含有共价键
B . CO2分子中含有离子键
C .  、
、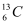 、
、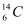 是碳的三种核素
D .
是碳的三种核素
D .  O,
O, 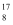 O,
O,  O含有相同的中子数
O含有相同的中子数
 、
、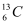 、
、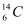 是碳的三种核素
D .
是碳的三种核素
D .  O,
O, 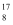 O,
O,  O含有相同的中子数
O含有相同的中子数
乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔.
-
(1) CaC2中C22﹣与O22+互为等电子体,O22+的电子式可表示为;
-
(2) 乙炔中C原子与H原子间共用电子对偏向C,SiH4中共用电子对偏H,则C、Si、H的电负性由大到小的顺序为.
-
(3) CaC2与水反应的化学方程式为.
下列各组物质中,只含有共价键的是( )
A . NH3、CO2
B . CaO、HCl
C . Na2S、MgO
D . H2O、Na2O2
下列物质只含有共价键的化合物是( )
A . N2
B . NaOH
C . H2O
D . Ar
6g某含氧衍生物在足量的氧气中完全燃烧,将产生的高温气体依次通过浓硫酸和氢氧化钠溶液,浓硫酸增重7.2g,氢氧化钠溶液增重13.2g。对该物质进行质谱分析,在所得的质谱图中有质荷比分别为27、29、31、44、50、58、60六条谱线,下图是该物质的核磁共振氢谱,并且峰面积比分别为1∶1∶6。
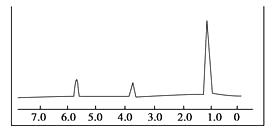
根据上述信息,完成下列问题:
-
(1) 确定该物质的分子式。
-
(2) 推测其结构,写出该物质的结构简式。
从能量变化看,有关  在
在  中燃烧说法错误的是()
中燃烧说法错误的是()
 在
在  中燃烧说法错误的是()
中燃烧说法错误的是()
A . 该反应是放热反应
B . 形成 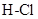 键放出能量
C . 燃烧时化学能转化成电能
D . 断裂
键放出能量
C . 燃烧时化学能转化成电能
D . 断裂 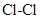 键吸收能量
键吸收能量
下列说法中正确的是 



A .  、
、  、
、  中,所有原子都满足最外层8电子的稳定结构
B . 在元素周期表中金属和非金属交界处可以找到半导体材料
C . 由非金属元素组成的化合物一定是共价化合物
D . 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键
中,所有原子都满足最外层8电子的稳定结构
B . 在元素周期表中金属和非金属交界处可以找到半导体材料
C . 由非金属元素组成的化合物一定是共价化合物
D . 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键
 、
、  、
、  中,所有原子都满足最外层8电子的稳定结构
B . 在元素周期表中金属和非金属交界处可以找到半导体材料
C . 由非金属元素组成的化合物一定是共价化合物
D . 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键
中,所有原子都满足最外层8电子的稳定结构
B . 在元素周期表中金属和非金属交界处可以找到半导体材料
C . 由非金属元素组成的化合物一定是共价化合物
D . 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键
已知:P4(s)+6Cl2(g)=4PCl3(g)△H=akJ/mol、P4(s)+10Cl2(g)=4PCl5(g)△H=bkJ/mol。P4具有正四面体结构,PCl5中P-Cl键的键能为ckJ/mol,PCl3中P-Cl键的键能为1.2ckJ/mol,下列叙述正确的是( )
A . P-P键的键能大于P-Cl键的键能
B . PCl3比PCl5更稳定
C . Cl-Cl键的键能 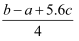 kJ/mol
D . P-P键的键能为
kJ/mol
D . P-P键的键能为 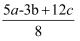 kJ/mol
kJ/mol
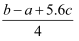 kJ/mol
D . P-P键的键能为
kJ/mol
D . P-P键的键能为 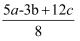 kJ/mol
kJ/mol
二茂铁分子[Fe (C5H5)2]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如图所示,下列说法正确的是( )
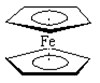
A . 二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键
B . 1mol环戊二烯( 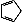 )中含有σ键的数目为5NA
C . 二茂铁分子中存在π键
D . Fe2+的电子排布式为1s22s22p63s23p63d44s2
)中含有σ键的数目为5NA
C . 二茂铁分子中存在π键
D . Fe2+的电子排布式为1s22s22p63s23p63d44s2
20世纪50年代科学家提出价层电子对互斥模型(简称VSEPR模型),用于预测简单分子立体结构.其要点可以概括为:
Ⅰ、用AXnEm表示只含一个中心原子的分子,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤对电子),(n+m)称为价层电子对数.分子中的价层电子对总是互相排斥,均匀的分布在中心原子周围的空间;
Ⅱ、分子的立体构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤对电子;
Ⅲ、分子中价层电子对之间的斥力的主要顺序为:
i、孤对电子之间的斥力>孤对电子对与共用电子对之间的斥力>共用电子对之间的斥力;
ii、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;
iii、X原子得电子能力越弱,A﹣X形成的共用电子对之间的斥力越强;
iv、其他.
请仔细阅读上述材料,回答下列问题:
-
(1) 根据要点I可以画出AXnEm的VSEPR理想模型,请填写下表:
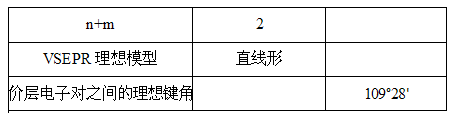
-
(2) H2O分子的立体构型为:,请你预测水分子中∠H﹣O﹣H的大小范围;
-
(3) SO2Cl2和SO2F2都属AX4E0型分子,S=O之间以双键结合,S﹣Cl、S﹣F之间以单键结合.请你预测SO2Cl2和SO2F2分子的立体构型:,SO2Cl2分子中∠Cl﹣S﹣Cl(选填“<”、“>”或“=”)SO2F2分子中∠F﹣S﹣F。
-
(4) 用价层电子对互斥理论(VSEPR)判断SO32﹣离子的空间构型:。
①PH3的分子构型为三角锥形,②BeCl2的分子构型为直线形,③CH4分子的构型为正四面体形,④CO2为直线形分子,⑤BF3分子构型为平面正三角形,⑥NF3分子结构为三角锥形。下面对分子极性的判断正确的是( )
A . ①⑥为极性分子,②③④⑤为非极性分子
B . 只有④为非极性分子,其余为极性分子
C . 只有②⑤是极性分子,其余为非极性分子
D . 只有①③是非极性分子,其余是极性分子
三价铬离子(Cr3+)是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等,回答下列问题:
-
(1) Cr的价电子排布式为;
-
(2) O、N、S的第一电离能由大到小的顺序为;
-
(3) SO2分子的VSEPR模型为,其中心原子的杂化方式为;
-
(4) CO和N2互为等电子体,两种物质相比沸点较高的是,其原因是;
-
(5) 化学式为CrCl3•6H2O的化合物有多种结构,其中一种可表示为[CrCl2(H2O)4]Cl•2H2O,该物质的配离子中提供孤电子对的原子为,配位数为;
-
(6) NH3分子可以与H+结合生成
 ,这个过程发生改变的是______(填序号)
A . 微粒的空间构型 B . N原子的杂化类型 C . H-N-H键角 D . 微粒的电子数
,这个过程发生改变的是______(填序号)
A . 微粒的空间构型 B . N原子的杂化类型 C . H-N-H键角 D . 微粒的电子数 -
(7) 由碳元素形成的某种晶体的晶体结构如图所示,若阿伏加德罗常数的值为NA , 晶体的密度为ρg•cm-3 , 则该晶胞的棱长为pm。
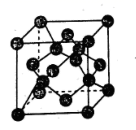
第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如图所示,下列说法中正确的是( )
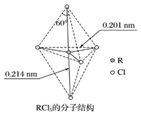
A . 每个原子都达到8电子稳定结构
B . 分子中形成5个等性杂化轨道但R-Cl 键键能可能不相同
C . R 最外层有5个未成对电子
D . 键角(Cl-R-Cl)有 90°、120°、180°三种
锆(  )和镉(
)和镉(  )是目前光电材料广泛使用的元素。
)是目前光电材料广泛使用的元素。 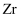 和
和 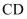 的晶胞分别如图甲、图乙所示:
的晶胞分别如图甲、图乙所示:
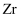 )和镉(
)和镉( 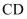 )是目前光电材料广泛使用的元素。
)是目前光电材料广泛使用的元素。 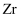 和
和 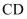 的晶胞分别如图甲、图乙所示:
的晶胞分别如图甲、图乙所示: 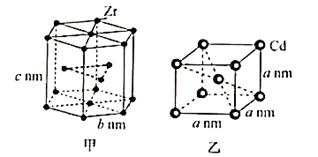
下列说法正确的是( )
A . 每个锆晶胞中含 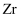 原子个数为8
B . 在镉晶胞中两个镉原子最近核间距为
原子个数为8
B . 在镉晶胞中两个镉原子最近核间距为 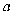
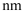 C . 在镉晶胞中
C . 在镉晶胞中 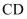 的配位数为4
D . 锆晶体的密度为
的配位数为4
D . 锆晶体的密度为 
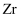 原子个数为8
B . 在镉晶胞中两个镉原子最近核间距为
原子个数为8
B . 在镉晶胞中两个镉原子最近核间距为 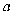
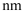 C . 在镉晶胞中
C . 在镉晶胞中 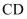 的配位数为4
D . 锆晶体的密度为
的配位数为4
D . 锆晶体的密度为 
根据π键的成键特征,判断C=C键的键能和C-C键的键能的关系是( )
A . 双键的键能等于单键的键能的2倍
B . 双键的键能大于单键的键能的2倍
C . 双键的键能小于单键的键能的2倍
D . 无法确定
某有机物的结构简式为HC≡CCH2CH=CH2 , 则该有机物分子中含有的  键和
键和  键的数目分别为( )
键的数目分别为( )
 键和
键和  键的数目分别为( )
键的数目分别为( )
A . 11、3
B . 10、3
C . 11、4
D . 10、4
为测定某有机化合物A的结构,通过实验得出以下数据:
①将有机化合物A置于氧气流中充分燃烧,实验测得生成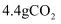 和
和 ;
;
②利用质谱仪测定出有机化合物A的相对分子质量为46;
③将4.6g该有机物与足量的金属钠反应,测得在标准状况下产生的氢气为1.12L;
下列有关A说法正确的是( )
A . A的一种同分异构体的结构简式: B . 46gA的分子结构中含有的C-H键数目为6NA
C . A与乙二酸可以通过缩聚反应生成高分子化合物
D . A中碳原子与氢原子的个数比是1:3,无法确定A中是否含有氧原子
B . 46gA的分子结构中含有的C-H键数目为6NA
C . A与乙二酸可以通过缩聚反应生成高分子化合物
D . A中碳原子与氢原子的个数比是1:3,无法确定A中是否含有氧原子
 B . 46gA的分子结构中含有的C-H键数目为6NA
C . A与乙二酸可以通过缩聚反应生成高分子化合物
D . A中碳原子与氢原子的个数比是1:3,无法确定A中是否含有氧原子
B . 46gA的分子结构中含有的C-H键数目为6NA
C . A与乙二酸可以通过缩聚反应生成高分子化合物
D . A中碳原子与氢原子的个数比是1:3,无法确定A中是否含有氧原子
随着科学技术的发展,人们可以利用很多先进的方法和手段来测定有机物的组成和结构。下列说法错误的是( )
A . 利用原子光谱上的特征谱线来鉴定元素,称为光谱分析
B . 红外光谱可以测定未知物中所含各种化学键和官能团,以此判断物质的结构
C . 质谱仪是通过分析最小的碎片离子测出分子的相对质量
D . 用X射线衍射摄取石英玻璃和水晶的粉末得到的图谱是不同的
最近更新
- 中国领导的多党合作和政治协商制度,适合我国国情,显示出强大生命力和显著优越性。在我国,多多合作的组织形式是 A.人大常委
- 我国对资本主义工商业社会主义改造实行的政策是
- 如图,在一个水池里有一个点光源S,SA是它发出的一条光线,在SA的行进方向上有一块平面镜,BC是SA经此平面镜反射后的反
- 真空中两点电荷Q1、Q2在如图所示的一条直线上,A、B是这条直线上的两点,一质量为m、电荷量为e的电子以速度经过点A向点
- 下图中AN、BN点属于两条相对的经线,N点为北极点,BC处于昼半球,且C正好是晨昏圈与某一纬线的切点,图中数据为纬度。读
- 已知:①R—NO2R—NH2;71~50) 下②+H2O; ③苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响
- (10分)1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数
- 已知方程的两根为、,则 .
- As is known to all his friends,_____ would ever discourage
- 有一道数学题:90%×90%×90%×90%×90%≈59%。它告诉我们,一项工作做到90%已经很不错了,但经过环环相扣
- 设某生物的体细胞中的DNA含量为2n,则它的精原细胞、初级精母细胞、次级精母细胞、精子细胞及精子中的DNA含量应依次为(
- — Can you help me to repair the motor now? — Sorry. I’m too
- 方苞,字灵皋,江南桐城人①。笃学修内行,治古文, 自为诸生,已有声于时。康熙三十八年,单人。四十五年,会试中试,将应殿试
- 某人骑自行车沿直线匀速旅行,先前进了a千米,休息了一段时间,又沿原路返回b千米(b<a),再前进c千米,则此人离起点的距
- 阅读下面的文章,完成14―17题。人,总要仰望点什么李兴濂①人生在世,不能总是低头觅食,那样会矮化得像动物一般。人,总要
- — I hope not toforget my promise to come to your party next
- 下列有关动物细胞有丝分裂的叙述,正确的是() A.染色单体形成于分裂前期,消失于分裂后期 B.分裂间期有DNA和中心体的
- I wonder if this red dress is ___________ in a larger size.
- 如图,立体图形由小正方体组成,这个立体图形有小正方体( )个.A.9个 B.10个
- 干干净净的傅雷公元1966年9月2日深夜,中国最伟大的翻译家傅雷与夫人朱梅携手同肩,双双自缢身亡。傅雷夫妇走得干干净净,



