第二节 原子结构与元素的性质 知识点题库
某原料经测定主要含有A、B、C、D、E五种原子序数依次增大的前四周期元素,其相关信息如下:
元素 | 元素性质或原子结构 |
A | 周期表中原子半径最小的元素 |
B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
C | 最外层p轨道半充满 |
D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
E | 位于ds区且原子的最外层电子数与A的相同 |
请回答下列问题(用A、B、C、D、E所对应的元素符号作答):
-
(1) B、C、D第一电离能由大到小的顺序为。
-
(2) E的二价离子的电子排布式为。
-
(3) A2B2D4常用作除锈剂,该分子中B的杂化方式为;1 mol A2B2D4分子中含有σ键与π键的数目之比为。
-
(4) 与化合物BD互为等电子体的阴离子的化学式为(任写一种)。
-
(5) B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是。
-
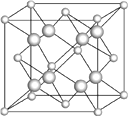
(6) 一种E和金(Au)形成的合金晶体具有面心立方最密堆积结构,其晶胞中E原子处于面心,Au原子处于顶点,则该合金中E原子与Au原子的个数之比为;若相临两个Au原子的最短距离为a厘米,则该合金的密度为g/cm3。又知上述晶体具有储氢功能,氢原子可进入到由E原子与Au原子构成的四面体空隙中。若将E原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(见图)的结构相似,该晶体储氢后的化学式应为。
请回答下列问题:(答题时,X、Y、Z、Q、R用所对应的元素符号表示)
-
(1) R的基态原子的电子排布式为。
-
(2) X、Y、Z三种元素第一电离能从大到小顺序为。
-
(3) 已知Y2Q2分子存在如下所示的两种结构(球棍模型,短线不一定代表单键):
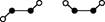
①该分子中两个Y原子之间的键型组合正确的是。
A.仅1个σ键
B.1个σ键和2个π键
C.1个σ键和1个π键
D.仅2个σ键
②该分子中Y原子的杂化方式是。
-
(4) X与Y元素可以形成一种超硬新材料,其晶体部分结构如下图所示,有关该晶体的说法正确的是。

A.该晶体属于分子晶体
B.此晶体的硬度比金刚石还大
C.晶体的化学式是X3Y4
D.晶体熔化时共价键被破坏,没有克服范德华力和氢键
-
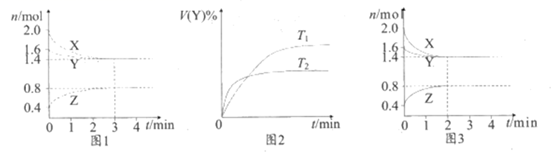
(1) Ⅰ.T℃时,在2L刚性密闭容器中,X(g)与Y(g)发生反应生成Z(g),反应过程中X、Y、Z的物质的量变化如图1所示。若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。
请回答下列问题:
容器中发生反应的方程式为。
-
(2) 正反应为反应(填“放热”或“吸热”)。
-
(3) 图1中,从反应开始到平衡用时3min,则0~3min内,v(X)=
-
(4) T℃时,该反应的平衡常数K=(保留小数点后两位)。
-
(5) 若只改变一个反应条件,使反应进程如图3所示,则改变的条件为。
-
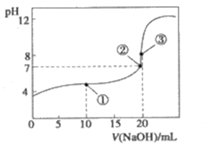
(6) Ⅱ.常温下,用0.1000ml•L-1NaOH溶液滴定20.00mL0.1000ml•L-1CH3COOH溶液,溶液的pH与滴入NaOH溶液体积的关系如图所示。
请回答下列问题:
实验过程中不需要的仪器或用品是(填序号)。
A 100mL容量瓶 B 锥形瓶 C 滴定管夹 D 玻璃棒 E.滴定管
-
(7) 如图点①所示溶液中离子浓度由大到小的顺序是。
-
(8) 如图点①②③所示溶液中,水的电离程度最大的是(填序号),c(Na+)=c(CH3COO-)的是(填序号)。
-
(9) 已知Ka(CH3COOH)=1.8×10-5 , 当滴定过程中c(CH3COOH):c(CH3COO-)=5:9时,溶液pH=。
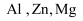 和
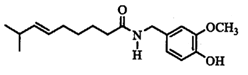
和 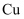 )几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
-
(1)
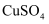 和
和 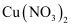 中阳离子基态核外电子排布式为,
中阳离子基态核外电子排布式为, 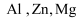 三种元素的第一电离能由大到小为;
三种元素的第一电离能由大到小为;
-
(2) 以
 和抗坏血酸为原料,可制备
和抗坏血酸为原料,可制备  。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为,推测抗坏血酸在水中的溶解性:(填“难溶于水”或“易溶于水”),一个
。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为,推测抗坏血酸在水中的溶解性:(填“难溶于水”或“易溶于水”),一个  晶胞(见图2)中,
晶胞(见图2)中, 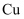 原子的数目为;
原子的数目为; 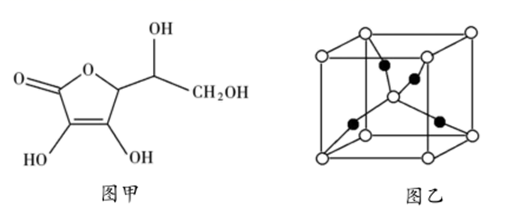
-
(3)
 和
和 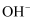 等配体都能与
等配体都能与  形成配离子。
形成配离子。 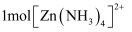 含
含 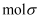 键,中心离子的配位数为;
键,中心离子的配位数为;
-
(4)
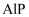 因杀虫效率高、廉价易得而被广泛应用。已知
因杀虫效率高、廉价易得而被广泛应用。已知  的熔点为2000℃,其晶胞结构如图所示。
的熔点为2000℃,其晶胞结构如图所示。 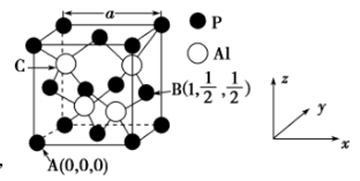
①磷化铝的晶体类型为,
②A、B点的原子坐标如图所示,则C点的原子坐标为,
③磷化铝的晶胞参数
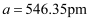 ,其密度为
,其密度为 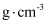 (列出计算式即可,用
(列出计算式即可,用  表示阿伏加德罗常数的值);
表示阿伏加德罗常数的值); -
(5)
 具有对称的立体构型,
具有对称的立体构型,  中的两个
中的两个  被两个
被两个  取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则  的空间构型为。
的空间构型为。
回答下列问题:
-
(1) 基态硼原子价电子排布式为;与硼同周期,且第一电离能小于硼的基态原子为 (填元素符号)。
-
(2) B、Al、Ga同主族,三种元素的氯化物的熔点如下表:
氯化物
BCl3
AlCl3
GaCl3
熔点/℃
-107
194
77.9
①BCl3的熔点低于GaCl3的原因为。
②AlCl3易形成多聚物,所以熔点较高,其中AlCl3的双聚分子的结构简式为 (配位键用“→”表示)。
-
(3) 某有机硼化物的结构简式如图所示。
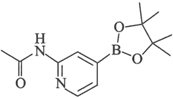
①该有机物中其他中心原子与B原子杂化类型相同的元素有。
②组成该有机物的第二周期元素电负性由大到小的顺序为。
-
(4) 立方氮化硼的晶胞结构如图所示。
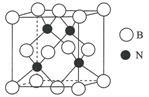
①晶胞中B原子的配位数为。
②若该晶胞的参数为acm,NA为阿伏加德罗常数的值,则该晶胞的密度为g/cm3(列出算式)。
 将2个
将2个 分子、2个
分子、2个 甲酸丁酯吡啶分子及2个
甲酸丁酯吡啶分子及2个 分子利用配位键自组装的超分子结构如图所示。
分子利用配位键自组装的超分子结构如图所示。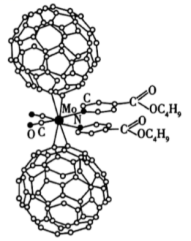
-
(1)
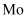 位于第5周期ⅥB族,基态原子核外电子排布与
位于第5周期ⅥB族,基态原子核外电子排布与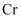 相似,则基态
相似,则基态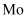 原子的价电子排布式为;核外未成对电子数为。
原子的价电子排布式为;核外未成对电子数为。
-
(2) 该超分子中存在的化学键类型有____(填字母)。A .
 键
B . π键
C . 离子键
D . 氢键
键
B . π键
C . 离子键
D . 氢键
-
(3) 配体
 中提供孤电子对的原子是(填元素符号);
中提供孤电子对的原子是(填元素符号);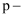 甲酸丁酯吡啶配体中C原子的杂化方式有。
甲酸丁酯吡啶配体中C原子的杂化方式有。
-
(4) 从电负性角度解释
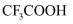 的酸性强于
的酸性强于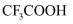 的。
的。
-
(5)
 与金刚石互为同素异形体,从结构与性质的关系角度解释
与金刚石互为同素异形体,从结构与性质的关系角度解释 的熔点远低于金刚石的原因。
的熔点远低于金刚石的原因。
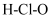 B . 虚线表示邻羟基苯甲醛的分子间氢键:
B . 虚线表示邻羟基苯甲醛的分子间氢键: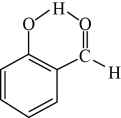 C . 醛基的碳氧双键有极性:
C . 醛基的碳氧双键有极性: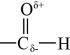 D . 组成天然蛋白质的氨基酸可以表示为:
D . 组成天然蛋白质的氨基酸可以表示为:- _______ name is Mike._______ is in China. A. He; His
- 对性腺组织细胞进行荧光标记,等位基因A、a都被标记为黄色,等位基因B、b都被标记为绿色,在荧光显微镜下观察处于四分体时期
- 方程2x-y=3与3x+2y=1的公共解是( ).(A) (B) (C)
- I hope _______ a good job in a foreigncompany after I gradu
- 下列有关文学常识的表述,不正确的一项是 A.加西亚·马尔克斯是魔幻现实主义最杰出的代表作家、诺贝尔文 学
- 1.依次填入下列各句横线处的词语,最恰当的一组是( ) (1)平时,只要看到老两口忙不过来,村民们都会主动前去帮忙,
- 如图,在△ABC中,AB=AC,D、A、E在直线m上,∠ADB=∠AEC=∠BAC. (1)求证:DE=DB+EC; (
- 下列词语中加点字读音有错误的一组是() A.牛虻(méng)______氓隶(méng) 魍魉(wǎng)
- 破坏臭氧层的主要污染源是( ) A.工厂、家用炉灶燃烧矿物能源 B.汽车尾气 C.有色金属冶炼工业排放废气
- —Have you heard of the severe drought in North China? —Yes,
- —Please the CDs here tomorrow. I need them.— OK,
- 加强中小学校园文化建设是优化育人环境的需要。随着改革开放的不断深入,社会文明呈现多元化发展态势,对中小学校园文化产生了重
- –Can’t you see thesigh ? It ________ “No smoking !” –Oh , So
- 某企业为了解下属某部门对本企业职工的服务情况,随机访问50名职工,根据这50名职工对该部门的评分,绘制频率分布直方图(如
- 函数若函数上有3个零点,则m的取值范围为 ( )
- What a pity ! He worked hard all his life but without much _
- 下列各句中,没有语病的一句是( ) A.国家已十几次对药品进行了降价,但老百姓“看病贵”的问题仍未得到解决,原因是
- 40%of the health problems skin and weight problems. A.
- ......
- 有下列几种溶液中发生的氧化还原反应① ②③ ④其中氧化性由强到弱的顺序



