第二章 化学反应与能量 知识点题库
由反应物X转化为Y和Z的能量变化如图所示。下列说法正确的是( )
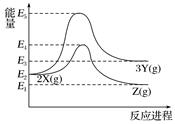
A . 由X→Y反应的ΔH=E5-E2
B . 由X→Z反应的ΔH>0
C . 降低压强有利于提高Y的产率
D . 升高温度有利于提高Z的产率
下列热化学方程式中△H的绝对值表示可燃物燃烧热的是( )
A . CO(g)+  O2(g) = CO2(g) △H=-283.0 kJ•mol-1
B . CH4(g)+ 2O2(g) = CO2(g)+2H2O(g) △H=-802.3 kJ•mol-1
C . 2H2(g)+ O2(g) = 2H2O(l) △H=-571.6kJ•mol-1
D . C(s)+
O2(g) = CO2(g) △H=-283.0 kJ•mol-1
B . CH4(g)+ 2O2(g) = CO2(g)+2H2O(g) △H=-802.3 kJ•mol-1
C . 2H2(g)+ O2(g) = 2H2O(l) △H=-571.6kJ•mol-1
D . C(s)+  O2(g) = CO(g) △H=-110.5kJ•mol-1
O2(g) = CO(g) △H=-110.5kJ•mol-1
 O2(g) = CO2(g) △H=-283.0 kJ•mol-1
B . CH4(g)+ 2O2(g) = CO2(g)+2H2O(g) △H=-802.3 kJ•mol-1
C . 2H2(g)+ O2(g) = 2H2O(l) △H=-571.6kJ•mol-1
D . C(s)+
O2(g) = CO2(g) △H=-283.0 kJ•mol-1
B . CH4(g)+ 2O2(g) = CO2(g)+2H2O(g) △H=-802.3 kJ•mol-1
C . 2H2(g)+ O2(g) = 2H2O(l) △H=-571.6kJ•mol-1
D . C(s)+  O2(g) = CO(g) △H=-110.5kJ•mol-1
O2(g) = CO(g) △H=-110.5kJ•mol-1
在容积一定的密闭容器中,置入一定量的NO(g)和足量C(s),发生反应C(s)+2NO(g)  CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )
CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )
 CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )
CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( ) 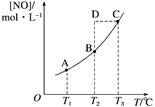
A . 该反应的ΔH>0
B . 若该反应在T1、T2时的平衡常数分别为K1、K2 , 则K1<K2
C . 在T2时,若反应体系处于状态D,则此时一定有v正<v逆
D . 在T3时,若混合气体的密度不再变化,则可以判断反应达到平衡状态C
下图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中正确的是( )
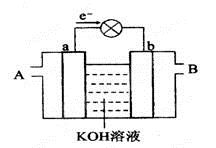
A . A处通入空气,B处通入水煤气
B . a电极的反应式包括:CO+4OH--2e-= CO32-+2H2O
C . a电极发生还原反应,b电极发生氧化反应
D . 如用这种电池电镀铜,当镀件增重6.4g,则消耗标准状况下的水煤气4.48 L
氢氧熔融碳酸盐燃料电池是一种高温电池(600~700℃),具有效率高、噪音低、无污染、燃料多样、余热利用价值高等优点。氢氧熔融碳酸盐燃料电池的工作原理如图所示。下列有关该电池的说法正确的是( )
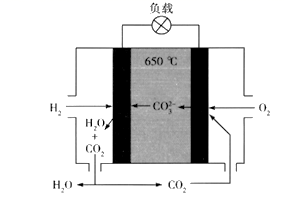
A . 电池工作时,熔融碳酸盐只起到导电的作用
B . 负极反应式为H2 -2e- +CO32-=CO2+H2O
C . 该电池可利用工厂中排出的CO2 , 减少温室气体的排放
D . 电池工作时,外电路中流过0.2 mol电子,消耗3.2 g O2
将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后,测得D浓度为0.5mol•L﹣1 , 此时A、B的浓度之比为c(A):c(B)=1:3,已知C的平均反应速率为0.05mol•(L•min)﹣1 , 求:
-
(1) 5分钟后A的浓度为;反应开始前放入容器B的物质的量为。
-
(2) 5min内B的平均反应速率为。
-
(3) x的值为。
NO2 是大气污染的主要污染物之一,硝酸盐是水体污染的污染物之一,电化学降解酸性 NO3-的原理如图所示,下列说法正确的是( )
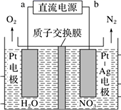
A . 电源正极为 b
B . 阴极电极反应式为 2NO3-+ 6H2O +10e-= N2↑+12 OH-
C . 两电极上产生的气体物质的量之比 n(O2):n(N2) = 5:2
D . 将阳极换成铜电极,反应不发生变化
下列说法正确的是( )
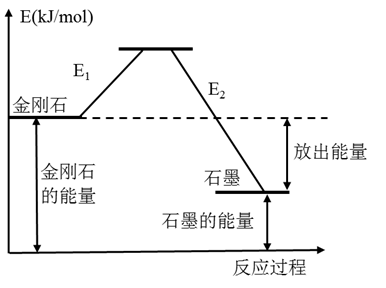
A . 如图所示,金刚石比石墨稳定
B . 需要加热才能进行的反应一定是吸热反应
C . 已知健能:H-H=436kJ/mol; I-I=151 kJ/mol;H-I=299 kJ/mol,因此反应H2(g) +I2(g)  2HI (g) 是放热反应
D . 已知2SO2+O2
2HI (g) 是放热反应
D . 已知2SO2+O2  2SO3为放热反应,因此SO2的能量一定高于SO3的能量
2SO3为放热反应,因此SO2的能量一定高于SO3的能量
 2HI (g) 是放热反应
D . 已知2SO2+O2
2HI (g) 是放热反应
D . 已知2SO2+O2  2SO3为放热反应,因此SO2的能量一定高于SO3的能量
2SO3为放热反应,因此SO2的能量一定高于SO3的能量
近日,我国学者在Science报道了一种氧离子介导的电化学合成方法,能将乙烯高效清洁、选择性地转化为环氧乙烷,电化学反应的具体过程如图所示。在电解结束后,将阴、阳板电解液输出混合,便可反应生成环氧乙烷。下列说法错误的是( )
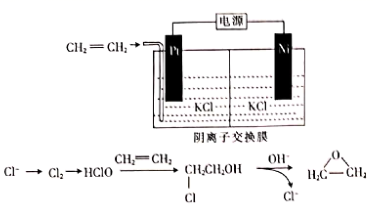
A . Ni电极与电源负极相连
B . 工作过程中阴极附近pH减小
C . 该过程的总反应为CH2=CH2 +H2O 
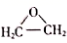 +H2
D . 电流由电源经Pt电极、KCl溶液、Ni电极回到电源
+H2
D . 电流由电源经Pt电极、KCl溶液、Ni电极回到电源

下列变化过程,属于放热反应的是( )
①浓H2SO4稀释;②碳与CO2化合;③H2在Cl2中燃烧;④固体NaOH溶于水;⑤液态水变成水蒸气;⑥酸碱中和反应。
A . ①③④⑥
B . ③⑥
C . ②③④
D . ①③⑤
氨气是一种重要的化工原料。
-
(1) I.已知 298K、101kPa 下,合成氨反应的能量变化如图1所示(ad表示被催化剂吸附,反应历程中粒子均为气态)。
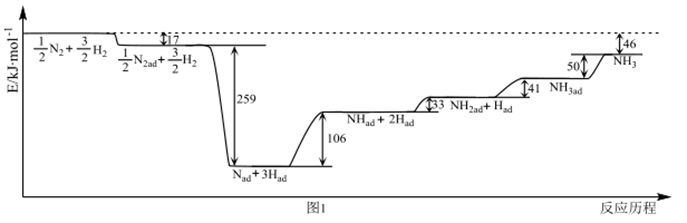
该条件下,N2(g)+3H2(g)
 2NH3 (g) ΔH =。
2NH3 (g) ΔH =。 -
(2) 反应历程中决定合成氨反应速率的一步反应的热化学方程式为。
-
(3) 改变下列某一条件,既能加快合成氨反应速率又能提高氮气的平衡转化率的是___________(填字母)。A . 升高温度 B . 增大压强 C . 增加 N2的量 D . 及时分离氨气
Ⅱ.以氨气作还原剂,可除去烟气中的氮氧化物。其中除去 NO 的反应原理如下:4NH3 (g)+6NO(g)
 5N2 (g)+6H2 O(g) ΔH= −1980 kJ/mol
5N2 (g)+6H2 O(g) ΔH= −1980 kJ/mol -
(4) 反应速率与浓度之间存在如下关系:v正=k正 c4 (NH3 )·c6 (NO),v逆 =k逆 c5 (N2 )·c6 (H2O) 。k正 、k逆 为速率常数,只受温度影响。350℃时,在 2L 恒容密闭容器中,通入 0.9mol NH3(g)和 1.2mol NO(g)发生反应,保持温度不变,平衡时 NO 的转化率为 50%,则此温度下
 ;当温度升高时,k正增大 m 倍,k逆增大 n 倍,则m n(填“>”、“<”或“=”)。
;当温度升高时,k正增大 m 倍,k逆增大 n 倍,则m n(填“>”、“<”或“=”)。
-
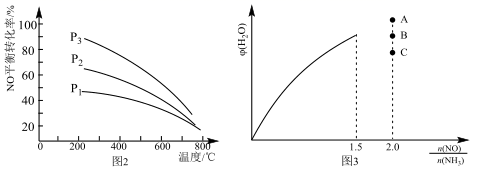
(5) 初始投料量一定,平衡时 NO 的转化率与温度、压强的关系如图 2 所示,则 P1、P2、P3 由大到小的顺序为,原因是。
-
(6) 保持温度不变,在恒容密闭容器中按一定比充入 NH3(g)和NO(g)发生反应,达到平衡时H2O(g)的体积分数 φ(H2O)随
 的变化如图 3 所示,当
的变化如图 3 所示,当  时,达到平衡时 φ(H2O)可能是 A,B,C 三点中的(填“A”、“B”或“C”)。
时,达到平衡时 φ(H2O)可能是 A,B,C 三点中的(填“A”、“B”或“C”)。
一定温度的恒容密闭容器中进行如下可逆反应A(s)+2B(g)⇌2C(g),下列叙述中,能说明反应已达到化学平衡状态的是( )
A . A,B,C的分子数之比为1:2:2
B . 混合气体的密度不再变化
C . 容器内的压强不再变化
D . 单位时间内生成amolA,同时消耗2amolC
下列关于反应能量的说法正确的是( )
A . 已知2C(s)+O2(g)=2CO(g) ΔH,ΔH表示碳的燃烧热
B . 若C(s,石墨)=C(s,金刚石) ΔH>0,则石墨比金刚石稳定
C . 已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g) = 2CO(g) ΔH2 , 则ΔH1>ΔH2
D . H+(aq)+OH−(aq)=H2O(l) ΔH=-57.3 kJ·mol−1 , 含1mol NaOH的氢氧化钠溶液与含0.5mol H2SO4的浓硫酸混合后放出57.3kJ的热量
“蓝天保卫战”需要持续进行大气治理,有效处理 SO2 、NO2 等大气污染物。化学研究为生产、生活处理废气,防止大气污染做出重要贡献。已知反应:SO2 (g)+NO2 (g)  SO3 (g)+NO(g) △H= - 41.8 kJ·mol -1 ,标准状况下,SO2 (g)+NO2 (g)
SO3 (g)+NO(g) △H= - 41.8 kJ·mol -1 ,标准状况下,SO2 (g)+NO2 (g)  SO3 (s)+NO(g) △H。下列有关说法错误的是( )
SO3 (s)+NO(g) △H。下列有关说法错误的是( )
 SO3 (g)+NO(g) △H= - 41.8 kJ·mol -1 ,标准状况下,SO2 (g)+NO2 (g)
SO3 (g)+NO(g) △H= - 41.8 kJ·mol -1 ,标准状况下,SO2 (g)+NO2 (g)  SO3 (s)+NO(g) △H。下列有关说法错误的是( )
SO3 (s)+NO(g) △H。下列有关说法错误的是( )
A . 升高反应温度可提高废气转化率
B . 该反应的△H< - 41.8 kJ·mol -1
C . 若V(SO2 ) 生成 =V(NO2 )消耗 ,则该反应到达平衡状态
D . 该反应的△S<0
相同温度和压强下,有如下热化学方程式,下列叙述正确的是( )

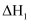


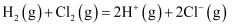
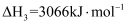
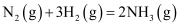

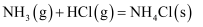

A . 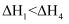 B .
B . 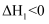 ,
,  C . H-Cl键键能为1533
C . H-Cl键键能为1533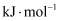 D .
D . 
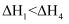 B .
B . 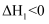 ,
,  C . H-Cl键键能为1533
C . H-Cl键键能为1533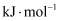 D .
D . 
实验室用石墨电极电解含有酚酞的饱和NaCl溶液,装置如右图所示,下列说法错误的是( )
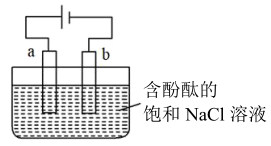
A . a极为电解池的阳极
B . a极发生的电极反应为:2Cl--2e-=Cl2↑
C . 在电场作用下Cl-、OH-向阴极移动
D . b极酚酞变红的原因是:H+放电,导致H2O⇌H++OH-正向移动,c(OH-)>c(H+)
科学家采用碳基电极材料设计了一种新的电解氯化氢回收氯气的工艺方案,原理如图所示。下列说法不正确的是( )
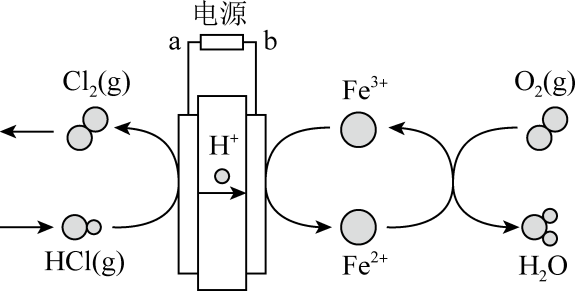
A . a是电源的正极
B . 阴极的电极反应式为:Fe2+-e-=Fe3+
C . 电路中每转移1mole-理论上可以回收氯气11.2L(标准状况)
D . 该工艺涉及的总反应为4HCl+O2=2Cl2+2H2O
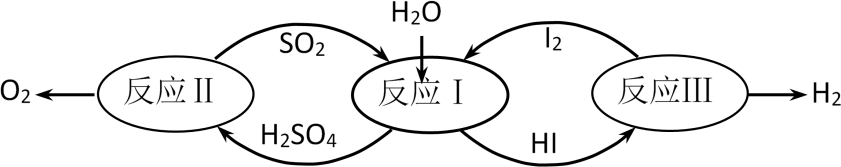
氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示:
-
(1) 反应Ⅰ的化学方程式是。
-
(2) 反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550kJ•mol-1。该反应自发进行的条件是(填“高温”、“低温”或“任意温度”),理由是。
反应Ⅱ由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177kJ•mol-1
ii.SO3(g)分解。则SO3(g)分解的热化学方程式为。
-
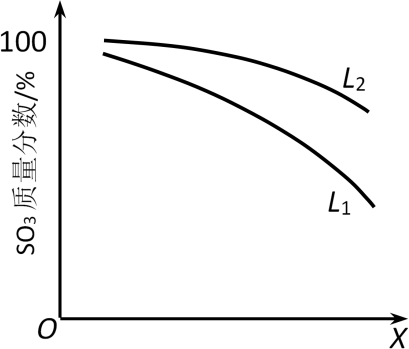
(3) L(L1、L2)、X可分别代表压强或温度。如图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
①X代表的物理量是。
②判断L1、L2的大小关系,L1L2 , 并简述理由:。
-
(4) 煤炭燃烧过程中会释放出大量的SO2 , 严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H1=218.4kJ•mol-1(反应Ⅰ)
CaO(s)+SO2(g)+CO2(g) △H1=218.4kJ•mol-1(反应Ⅰ)CaSO4(s)+4CO(g)
 CaS(s)+4CO2(g) △H2=-175.6kJ•mol-1(反应Ⅱ)
CaS(s)+4CO2(g) △H2=-175.6kJ•mol-1(反应Ⅱ)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v1>v2 , 请画出反应体系中c(SO2)随时间
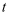 变化的总趋势图。
变化的总趋势图。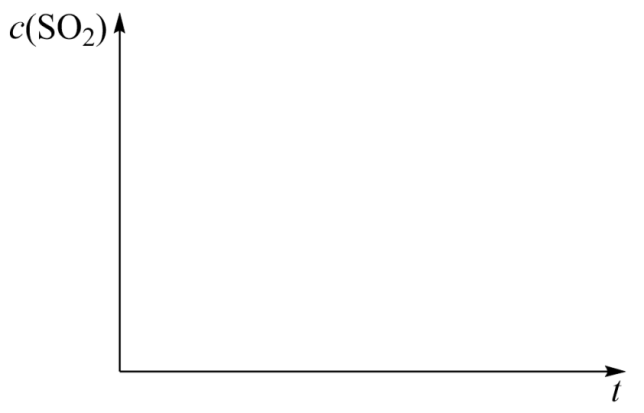
-
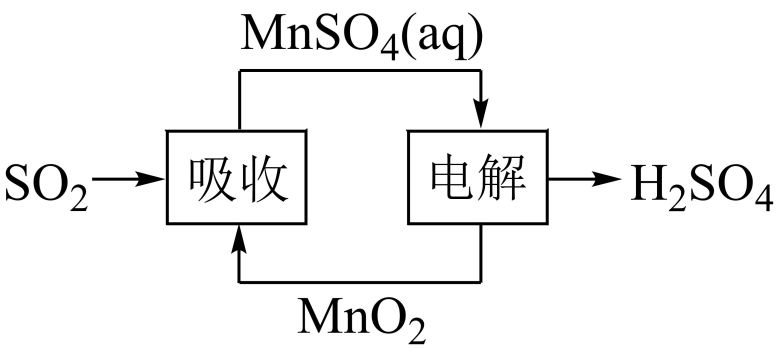
(5) 工业生产中产生的SO2废气也可用如图方法获得H2SO4。写出电解的阳极反应式。
某兴趣小组设计的水果电池装置如图所示。该电池工作时,下列说法正确的是( )
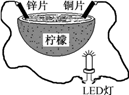
A . 将电能转化为化学能
B . 电子由锌片经导线流向铜片
C . 铜片作负极
D . 锌片发生还原反应
依据如下有关铝的三个装置图,回答问题。
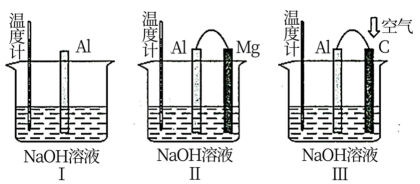
-
(1) 三个装置同时开始反应,单位时间内温度计示数最高的是(填“图Ⅰ”“图Ⅱ”或“图Ⅲ”)。
-
(2) 写出图Ⅱ装置Al电极的电极反应式:;写出图Ⅲ装置正极的电极反应式:;写出图Ⅲ装置的总反应化学方程式:。
-
(3) 图Ⅰ装置中为使生成氢气的速率加快,下列方法可行的是(填序号)。
①适当升高温度②把铝棒加粗
③将NaOH溶液换成浓硫酸④用铝碳合金代替铝棒
-
(4) 某同学欲收集
 和碘蒸气,在某绝热且体积固定的密闭容器中发生反应:
和碘蒸气,在某绝热且体积固定的密闭容器中发生反应: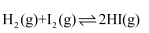 , 下列叙述能证明该反应达到化学平衡状态的是(填序号)。
, 下列叙述能证明该反应达到化学平衡状态的是(填序号)。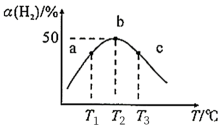
A.容器内温度不变
B.混合气体密度不变
C.混合气体平均相对分子质量不变
D.HI的体积分数不变
E.1mol
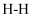 键断裂的同时有2mol
键断裂的同时有2mol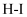 键生成现向容积为1L密闭容器中充入0.10mol
键生成现向容积为1L密闭容器中充入0.10mol 和0.15mol
和0.15mol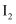 , 在不同温度下测定同一时刻
, 在不同温度下测定同一时刻 的转化率,结果如图。当温度为
的转化率,结果如图。当温度为 ℃时,从反应开始经过2min达到b点,用
℃时,从反应开始经过2min达到b点,用 表示这段时间的反应速率为,此时
表示这段时间的反应速率为,此时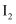 的转化率为(保留2位有效数字)。
的转化率为(保留2位有效数字)。
最近更新
- 在农业3.0时代到来之际,全国第一家网上农资商城——云农场,运用感知化、物联化、智能化等手段,实现了对传统农业生产和流通
- 下列关于原子结构、元素性质的说法正确的是() A.非金属元素组成的化合物中只含共价键 B.ⅠA族金属元素是同周期中金属性
- 用线将科学家和他们的科学成就联结起来,下列各项中错误的是 A.孟德尔——发现分离定律和自由组合定律
- Very generally, grammar is ______ with the relations between
- 金属小球a和金属小球b的半径之比为1:3,所带电量之比为1:7.两小球间距远大于小球半径且间距一定时,它们之间相互吸引力
- 室温下向10 mL0.1 mol·L-1NaOH溶液中加入0.1mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。
- 补写出下列名篇名句中的空缺部分。(任选1题。5分,每空1分) (1) ,可以无悔矣,其孰
- 1931年初,苏联接受外国技术援助的项目已达124项,大部分是美、德两国提供的,同年,苏联向外国购买的机器设备约占世界设
- 6.向存在大量Na+、Cl-的溶液中通入足量的NH3后,该溶液中还可能大量存在的离子组是 A.K+、Br-、
- 对自然界物质循环起最大作用的是( ) A.病原菌 B.寄生的细菌和真菌 C.腐
- 隋唐实行三省六部制,下列关于该制度的评述正确的是() ①分散相权以加强皇权 ②形成严密的封建官僚机构体系 ③有利于减少中
- Children’s brains can’t develop properly_______ they lack pr
- 若函数f(x)=﹣x3+x2+2ax在[,+∞)上存在单调递增区间,则a的取值范围是
- 若正三棱锥的侧面都是直角三角形,则侧面与底面所成二面角的余弦值是() A.
- 分析下列各物质的物理性质,可判断其固态不属于分子晶体的是( ) A.碳化铝,黄色晶体,熔点2200℃
- (11分)图表法、图象法是常用的科学研究方法。阅读下列图表回答问题:(1)第三周期某主族元素M的电离能情况如图(A)所示
- (10龙岩市18). 金属氢化物如氢化钙(CaH2)、氢化钠(NaH)是一种重要的制氢剂,与水接触时,分别发生如下反应:
- 如图所示,真空室内存在宽度为d=8cm的匀强磁场区域,磁感应强度B=0.332T,磁场方向垂直于纸面向里;ab、cd足够
- 史料是研究历史的重要载体。研究五四运动爆发的直接原因,可以查阅的文献史料是 A.《联合国家宣言》 B.《慕尼黑协定》
- 下列四个城市6月22日白昼时间最长的是( ) A 北京 B广州



