第三节 硫和氮的氧化物 知识点题库
化学是一门中心学科,与社会发展的需要有密切的关系。下列说法正确的是( )
A . 无论是风力发电还是潮汐发电,都是将化学能转化为电能
B . 绿色化学的核心是在化学合成中将原子充分利用,转化为新的原子
C . 为防止月饼等富脂食品氧化变质,常在包装袋内放人生石灰
D . 城市停车场安装催化光解设施,可将汽车尾气中的CO和NOx转化为无毒气体
工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO2转化为有用的副产品。请按要求回答下列问题:
-
(1) 将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:、。
-
(2) 在尾气与氨水反应所得到的高浓度溶液中,按一 定比例加入氨水或碳酸氢铵,此时溶液的温度会自行降低,并析出晶体。①导致溶液温度降低的原因可能是;②析出的晶体可用于造纸工业,也可用于照相用显影液的生产。已知该结晶水合物的相对分子质量为134,则其化学式为。
下列过程,观察不到颜色变化的是( )
A . NO气体暴露在空气中
B . 往FeCl3溶液中滴入KSCN溶液
C . Cl2通过湿润的有色布条
D . 往NaOH溶液中通入CO2
下列有关物质的组成、性质、用途的说法.正确的是( )
①Na2O2中的阳离子和阴离子个数比为1:1
②常温下铝制容器可储运浓硫酸或浓硝酸
③盐酸既有氧化性又有还原性
④NO2 , Fe(OH)3 , FeCl2都能直接通过化合反应制备
⑤H2S能使酸性高锰酸钾溶液褪色.所以它具有漂白性.
A . ②③④
B . ①②③
C . ①②③④
D . ①②③⑤
下列叙述不正确的是( )
A . 低碳生活(low﹣carbon life)是一种时尚的生活理念,倡导减少温室气体排放,CO2、CH4等是常见的温室气体
B . 新型无机非金属材料用途广泛,人造刚玉用做高温炉管、氮化硅陶瓷可用于制造柴油机发动机部件
C . 推广可利用太阳能、风能的城市照明系统,积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料,利于发展低碳经济、循环经济
D . “显世闻名”的奶粉事件中污染物为三聚氰胺(结构如图),其摩尔质量为126g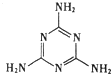

有关硫及其化合物的说法合理的是( )
A . 可用酒精洗刷做硫磺性质实验的试管
B . SO2具有很强的还原性,在化学反应中只能作还原剂
C . 浓硫酸具有强氧化性,常温下与铜反应可制取SO2
D . 1mol硫与其他物质完全反应,转移的电子数不一定是2mol
检验下列物质的试剂、现象都正确的是( )
| 选项 | 被检验的物质 | 使用的试剂或方法 | 实验现象 |
| A | Fe3+ | KSCN溶液 | 溶液出现血红色沉淀 |
| B | SO2 | 品红溶液 | 品红溶液褪色,加热不能复原 |
| C | Na+ | 用铂丝蘸取少量溶液在火焰上灼烧 | 透过蓝色钴玻璃看到紫色火焰 |
| D | NH4+ | NaOH溶液、石蕊试纸 | 加入NaOH溶液后加热,产生的气体使湿润的红色石蕊试纸变蓝 |
A . A
B . B
C . C
D . D
常温下,二氯化二硫(S2Cl2)为橙黄色液体,遇水易水解,工业上用于橡胶的硫化。某学习小组用氯气和硫单质合成S2Cl2的实验装置如图所示.下列说法正确的是( )
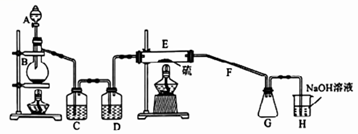
A . 实验时需先点燃E处的酒精灯
B . C,D中所盛试剂为饱和氯化钠溶液、浓硫酸
C . 二氯化二硫(S2Cl2)水解反应产物为:S、H2S、HCl
D . G中可收集到纯净的产品
实验室进行二氧化硫制备与性质实验的组合装置如图所示,部分夹持装置未画出。
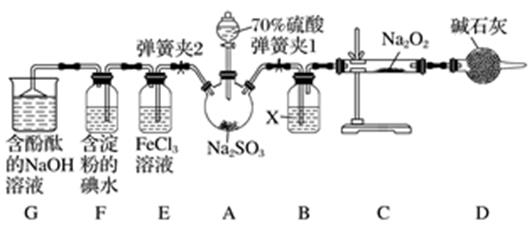
请回答下列问题:
-
(1) 在组装好装置后,首先要进行的实验操作为。
-
(2) 为检验SO2与Na2O2的反应是否有氧气生成,装置B中盛放的试剂X应为,装置D中碱石灰的作用是。
-
(3) 关闭弹簧夹2,打开弹簧夹1,注入70%的硫酸至浸没三颈烧瓶中的固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是。
-
(4) 关闭弹簧夹1,打开弹簧夹2,残余气体进入装置E、F、G中,能说明I-的还原性弱于SO2的现象为。发生反应的离子方程式是。
-
(5) 为了验证装置E中SO2与FeCl3发生了氧化还原反应,某学生设计了如下实验:取少量装置E中的溶液于试管中,向其中加入稀硝酸酸化的BaCl2溶液,产生白色沉淀,并由此判断SO2与FeCl3发生了氧化还原反应。上述方案是否合理?(填“合理”或“不合理”),原因是。
向FeCl3和BaCl2的混合溶液中通入SO2 , 有沉淀生成,此沉淀是( )
A . Fe(OH)3
B . FeS
C . S
D . BaSO4
下列说法错误的是( )
A . 氢气在氯气中可以安静燃烧产生淡蓝色火焰
B . 磁性氧化铁粉末在空气中长时间存放会变红
C . 溴化钠和硝酸银溶液混合会产生浅黄色沉淀
D . 足量SO2通入Ba(NO3)2溶液中产生白色沉淀
NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
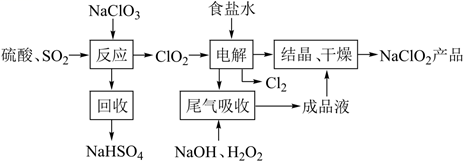
已知电解总反应为:  ,回答下列问题:
,回答下列问题:
-
(1) 从物质分类角度来看,NaHSO4是(填字母代号)。
a.酸 b.酸式盐 c.电解质 d.非电解质 e.离子化合物 f.共价化合物
-
(2) 写出“反应”步骤中生成ClO2的化学方程式。
-
(3) “电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+ , 要加入的试剂分别为、。
-
(4) “尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂(ClO2)与还原剂(H2O2)的物质的量之比为。
在探究某地刚落下的酸雨成分的实验中,下列根据实验现象得出的结论正确的是( )
A . 每隔1h测定酸雨试样的pH,其pH先变小后不变,说明刚落下的酸雨中一定含有SO2
B . 将酸雨试样浓缩后加入Cu和浓H2SO4 , 试管口有红棕色气体,逸出说明酸雨中可能含  C . 在酸雨试样中加入Ba(NO3)2溶液有白色沉淀,说明酸雨中一定含
C . 在酸雨试样中加入Ba(NO3)2溶液有白色沉淀,说明酸雨中一定含  D . 用玻璃棒蘸取酸雨,在酒精灯上灼烧,火焰呈黄色,说明酸雨中一定存在Na+
D . 用玻璃棒蘸取酸雨,在酒精灯上灼烧,火焰呈黄色,说明酸雨中一定存在Na+
 C . 在酸雨试样中加入Ba(NO3)2溶液有白色沉淀,说明酸雨中一定含
C . 在酸雨试样中加入Ba(NO3)2溶液有白色沉淀,说明酸雨中一定含  D . 用玻璃棒蘸取酸雨,在酒精灯上灼烧,火焰呈黄色,说明酸雨中一定存在Na+
D . 用玻璃棒蘸取酸雨,在酒精灯上灼烧,火焰呈黄色,说明酸雨中一定存在Na+
用中子轰击 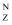 X原子产生α粒子(即氮核
X原子产生α粒子(即氮核 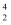 He)的核反应为:
He)的核反应为: 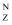 X+
X+  n→
n→  Y+
Y+ 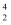 He。已知元素Y在化合物中呈+1价。下列说法正确的是( )
He。已知元素Y在化合物中呈+1价。下列说法正确的是( )
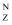 X原子产生α粒子(即氮核
X原子产生α粒子(即氮核 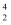 He)的核反应为:
He)的核反应为: 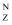 X+
X+  n→
n→  Y+
Y+ 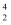 He。已知元素Y在化合物中呈+1价。下列说法正确的是( )
He。已知元素Y在化合物中呈+1价。下列说法正确的是( )
A . H3XO3可用于中和溅在皮肤上的NaOH溶液
B . Y单质在空气中燃烧的产物是Y2O2
C . X和氢元素形成离子化合物
D . 6Y和7Y互为同素异形体
亚硝酰氯(NOCl)的沸点为-5.5℃,易水解生成两种酸,常用于有机合成。学习小组在实验室中对NO与  制备NOCl的反应进行了探究。回答下列问题:
制备NOCl的反应进行了探究。回答下列问题:
 制备NOCl的反应进行了探究。回答下列问题:
制备NOCl的反应进行了探究。回答下列问题:
-
(1) 出于安全和环保考虑,制备反应的实验操作需在(条件)下进行。
-
(2) NO与
 反应,装置如图所示(已知
反应,装置如图所示(已知  溶液可以吸收NO)。
溶液可以吸收NO)。 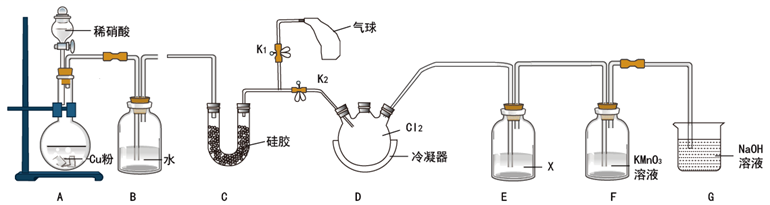
①关闭
 ,打开
,打开 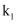 和分液漏斗活塞,至气球膨胀,目的为;连接B的目的为。
和分液漏斗活塞,至气球膨胀,目的为;连接B的目的为。②关闭
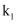 ,打开
,打开  ,向D中通入气体,至黄绿色完全消失。D中反应的化学方程式为。
,向D中通入气体,至黄绿色完全消失。D中反应的化学方程式为。 -
(3) 装置E中的试剂X为,作用为。
-
(4) 测定NOCl的纯度。
已知:实验前,D中
 的体积为
的体积为 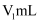 (已换算为标准状况)。取实验后D中所得溶液,加入适当过量NaI溶液,酸化后充分反应(杂质不参加反应,还原产物为NO);以淀粉为指示剂,用
(已换算为标准状况)。取实验后D中所得溶液,加入适当过量NaI溶液,酸化后充分反应(杂质不参加反应,还原产物为NO);以淀粉为指示剂,用 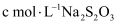 标准液滴定,达到滴定终点时消耗标准液体积为
标准液滴定,达到滴定终点时消耗标准液体积为  。
。①NaI发生反应的离子方程式为。
②达到滴定终点的现象为。
③本实验中NOCl的产率为。
臭氧已成为夏季空气污染的元凶,地表产生臭氧的机理如图所示,NA代表阿伏加德罗常数的数值。下列说法正确的是( )
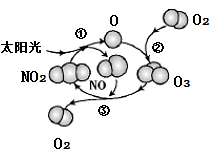
A . 反应①、②、③都是氧化还原反应
B . 16 O3和O2的混合气体,所含质子数为16NA
C . 0.5mol NO2溶于水形成1L溶液,可得到0.5 mol∙L−1的硝酸溶液
D . 标准状况下,11.2L的NO和O2混合气体所含的原子数为NA
工业上由含铜废料(含有Cu、CuS、CuSO4等)制备硝酸铜晶体的流程如图:
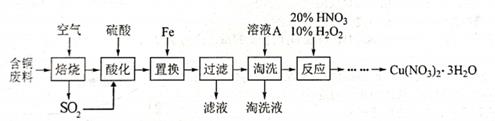
-
(1) 写出CuS“焙烧”生成SO2和CuO的化学反应方程式:。
-
(2) 图中SO2经转化生成的硫酸可用于“酸化”,转化反应中SO2与O2的物质的量比为。
-
(3) “过滤”后需洗涤沉淀,请设计实验证明已洗涤干净。
-
(4) “淘洗”所用的溶液A应选用(填序号)
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
-
(5) “反应”步骤加10% H2O2可以避免污染性气体的产生,写出该反应的离子方程式:,也可以用气体(填化学式)代替双氧水。
-
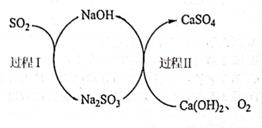
(6) 大量排放SO2容易造成酸雨等环境问题,工业上可用双碱法脱硫法处理废气,过程如图所示,其中可循环使用的试剂是,写出双碱法脱硫法的总反应方程式:。
化学与生产、生活和环境都息息相关。下列说法正确的是( )
A . CO2、NO2或SO2都会导致酸雨的形成
B . 嫦娥五号探测器的太阳能帆板的主要材质是二氧化硅
C . 铝制容器不能长期盛装酸性、碱性或咸的食品
D . 袋装食品中常放入硅胶,是为了防止食物被氧化变质
化学与社会生产和生活密切相关,下列叙述中错误的是( )
A . 缺铁性贫血患者服用补铁剂时,与维生素C同时服用效果更好
B . 咳嗽产生的飞沫分散到空气中形成气溶胶
C . 用于新版人民币票面文字等处的油墨中所含有的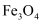 是一种磁性物质
D . 嫦娥5号带回的“快递”——“月壤”中含有珍贵的3He,它与4He互为同素异形体
是一种磁性物质
D . 嫦娥5号带回的“快递”——“月壤”中含有珍贵的3He,它与4He互为同素异形体
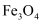 是一种磁性物质
D . 嫦娥5号带回的“快递”——“月壤”中含有珍贵的3He,它与4He互为同素异形体
是一种磁性物质
D . 嫦娥5号带回的“快递”——“月壤”中含有珍贵的3He,它与4He互为同素异形体
化学与人类社会生产、生活有着密切联系。下列叙述中错误的是( )
A . 维生素C可用作水果罐头的抗氧化剂
B . 温度越高,酶的催化效率越高
C . 葡萄酒中添加入适量的 可以起到保质的作用
D . 高温、75%酒精、84消毒液(含NaClO)都可使新冠病毒蛋白质变性
可以起到保质的作用
D . 高温、75%酒精、84消毒液(含NaClO)都可使新冠病毒蛋白质变性
 可以起到保质的作用
D . 高温、75%酒精、84消毒液(含NaClO)都可使新冠病毒蛋白质变性
可以起到保质的作用
D . 高温、75%酒精、84消毒液(含NaClO)都可使新冠病毒蛋白质变性
最近更新
- 计算:-(-)0+(-1)2012.
- 五带中,四季变化最明显的是 ①热带 ②北温带 ③北寒带 ④南温带 ⑤南寒带 A.
- 实验室用下图所示装置制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4。已知K
- 下列说法正确的是 A、城市化的主要动力是人口增长迅速 B、世界城市化水平在不断下降 C、一般来说,城市化水平体
- 设是两条不同的直线,是一个平面,则下列命题不正确的是 若,,则 若,∥,则 若,,则∥
- 有一根镍铬合金线,两端电压为6伏时,通过合金线的电流为0.3安,则合金线的电阻是________欧;若两端电压减小一半,
- 下列关于生物遗传物质的叙述中,正确的是() A. 细胞核内的遗传物质是DNA,细胞质内的遗传物质是RNA
- 已知函数, (1)当时,求不等式的解集; (2)当时, 函数与轴围成的三角形面积为6,求的值.
- Going to bed early and getting up early_______ considered t
- Her face was pale and ill–looking, she had been wit
- 已知椭圆C: +=1(a>b>0)的长轴长为2,右焦点F(1,0),过F作两条互相垂直的直线分别交椭圆G于点A,B和C,
- 下列物质性质与应用对应关系正确的是 A.氨气具有碱性,可用作制冷剂 B.二氧化硅能与氢氟酸反应,可用于生产光导纤维 C.
- _____ the news, so far, has been good, there may be days ahe
- 甲、乙、丙三辆小车同时、同地向同一方向运动,它们运动的图像如图所示,由图像可知:运动速度相同的小车是 和
- 下图实线为等压线,虚线为风向轨迹图,④是稳定风向,回答29~30题。29.该地的水平气压梯度力方向是 ( ) A.
- 近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。下图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛
- CO(g)+NO2(g)⇌CO2(g)+NO(g)△H<0,若其他条件不变,只改变下列条件,能使混合气体颜色变深的是(
- 为探究培养液中酵母菌种群数量的动态变化,有人进行了如下操作。其中操作正确的是() A.将适量干酵母放入装有清水的锥形瓶中
- 如图所示,在处于O点的点电荷+Q形成的电场中,试探电荷q由A点移到B点,电场力做功为W1;以OA为半径画弧交于OB于C,
- 我市连续7天的最高气温为28℃,27℃,30℃,33℃,30℃,30℃,32℃,这组数据的平均数和众数分别是( ) A.



