第三节 用途广泛的金属材料 知识点题库
下列说法正确的是 ( )
A . 所有不锈钢都只含有金属元素
B . 我国流通的硬币材质是金属单质
C . 广东打捞的明代沉船上存在大量铝制餐具
D . 镁合金的硬度和强度均高于纯镁
生铁的熔点是1100℃~1200℃,则纯铁的熔点可能是( )
A . 1055℃
B . 1100℃
C . 1200℃
D . 1535℃
化学与生活、社会密切相关.下列说法不正确的是( )
A . 为了防止污染环境,废弃的塑料应焚烧处理
B . 误食重金属盐后,应采取的有效应急措施是喝大量的豆浆或牛奶
C . 为防止电池中的重金属元素污染土壤和水体,应积极开发废电池的综合利用技术
D . 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
下列说法不正确的是( )
A . 生铁的熔点低于纯铁
B . 运输酒精的车辆所帖标志应是  C . 漂白粉能在空气中长期存放
D . 氢氧化铝可作胃酸的中和剂
C . 漂白粉能在空气中长期存放
D . 氢氧化铝可作胃酸的中和剂
 C . 漂白粉能在空气中长期存放
D . 氢氧化铝可作胃酸的中和剂
C . 漂白粉能在空气中长期存放
D . 氢氧化铝可作胃酸的中和剂
金属材料在日常生产生活中有着广泛的应用,请回答下列问题:
-
(1) 人类最早使用的合金是,目前使用量最大的金属是.
-
(2) 铁和铁合金是日常生活中的常用材料,下列叙述正确的是 .A . 纯铁的硬度比生铁高 B . 纯铁耐腐蚀性强,不易生锈 C . 不锈钢是铁合金,只含金属元素 D . 铁在一定条件下,可与水蒸气反应 E . 铁在冷的浓硫酸中会钝化
-
(3) 向沸水中滴入几滴饱和FeCl3溶液,加热至液体呈透明的红褐色,该反应的离子方程式为,形成的分散系中分散质的微粒直径范围是.
-
(4) 向硫酸亚铁溶液中加入过氧化钠,有红褐色沉淀生成,如果加入的Na2O2与生成的O2的物质的量之比为3:1,请写出发生的离子反应方程式.
-
(5) 电子工业需要用30%的FeCl3溶液腐蚀绝缘板上的铜,制造印刷电路板.请写出FeCl3 溶液与铜反应的离子方程式:,向腐蚀后的废液中加入一定量的铁粉充分反应后,无固体剩余,则反应后的溶液中一定含有的离子是,可能含有的离子是.如果从腐蚀后的废液中回收铜并重新获得FeCl3溶液,现有下列试剂:①氯气②铁粉③浓硝酸④浓盐酸⑤烧碱⑥浓氨水.需要用到的一组试剂是.
A.①②④B.①③④⑥C.②④⑤D.①④⑥
-
(6) 高铁酸钠(Na2FeO4)是一种新型净水剂.高铁酸钠的制备方法之一是:在碱性条件下用NaClO氧化Fe3+ , 请写出该反应的离子反应方程式.
-
(7) 有一种铁的氧化物样品,用5mol/L盐酸140mL,恰好完全溶解,所得溶液还能吸收标况下0.56L氯气,恰好使其中Fe2+全部转化成Fe3+ , 该氧化物的化学式是.
材料是人类赖以生存的重要物质基础.材料种类很多,通常可分为金属材料、无机非金属材料(包括硅酸盐材料)、高分子合成材料及复合材料.
-
(1) 合金是被广泛应用的金属材料.
①下列有关合金性质的说法正确的是(填字母).
A、合金的熔点一般比它的成分金属高
B、合金的硬度一般比它的成分金属低
C、组成合金的元素种类相同,合金的性能就一定相同
D、合金与各成分金属相比,具有许多优良的物理、化学或机械性能
②铁锈蚀主要发生的是腐蚀,其负极反应式为.
-
(2) 无机非金属材料包括玻璃、水泥和.
-
(3) 合成塑料、合成橡胶和是常说的三大合成材料.下列属于塑料制品的是.
A、汽车轮胎 B、涤纶 C、聚乙烯制品 D、玻璃钢.
某探究小组在实验室中用铝土矿(主要成分为Al2O3 , 还含有Fe2O3、SiO2)提取氧化铝.回答下列问题:
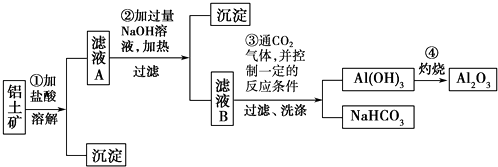
-
(1) 在实验中需用1mol•L﹣1的NaOH溶液480mL,配制该溶液已有下列仪器:托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器.在灼烧操作中用到下列仪器中的一种,其名称是
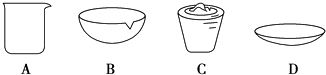
-
(2) 写出步骤①中发生反应的离子方程式.
-
(3) 操作③中的洗涤操作如何进行?
-
(4) 甲同学在实验室中用如图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象.
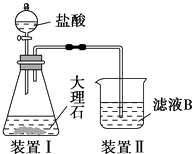
乙同学分析认为:甲同学通入CO2的量不足是导致实验失败的原因之一,你认为乙的分析是否合理?.若合理,请用离子方程式解释其原因 (若你认为不合理,该空不作答).
丙同学分析认为:甲同学通入的CO2中含有HCl气体,也是导致实验失败的原因,在实验中增加某装置可解决这个问题.请帮助丙同学画出该装置图,并注明试剂名称.
合金是一类用途广泛的金属材料,下列物质中属于合金的是( )
A . 钢
B . 水银
C . 金刚石
D . 四氧化三铁
工业生产中常将两种或多种金属(或金属与非金属)在同一容器中加热使其熔合,冷凝后得到具有金属特性的熔合物﹣﹣合金.这是制取合金的常用方法之一.根据下表数据判断,不宜用上述方法制取合金的是( )
| 金属 | Na | Al | Cu | Fe |
| 熔点(℃) | 97.81 | 660 | 1083 | 1535 |
| 沸点(℃) | 883 | 2200 | 2595 | 3000 |
A . Fe﹣Cu合金
B . Cu﹣Al合金
C . Al﹣Na合金
D . Cu﹣Na合金
下列说法错误的是( )
A . 镁的氧化物熔点很高,是优质的耐高温材料
B . 工业上采用热还原法来冶炼金属铁
C . 二氧化硫因具有还原性,可以用来漂白纸浆
D . 晶体硅是一种重要的半导体材料,是手机芯片中的主要成分
化学与人类生产、生活、社会可持续发展密切相关。下列说法正确的是( )
A . 自来水厂常用明矾作消毒杀菌剂
B . 高铁车用大部分材料是铝合金,铝合金材料具有强度大、质量轻、抗腐蚀能力强等优点
C . 硅胶可作瓶装药品的干燥剂及催化剂载体,也是重要的半导体材料
D . 使用肥皂洗手可预防病毒,肥皂的主要成分硬脂酸钠溶于水显酸性
改革开放40周年取得了很多标志性成果,下列说法错误的是( )
A . “中国天眼”的镜片材料为SiC,属于新型无机非金属材料
B . “蛟龙”号潜水器所使用的钛合金材料具有强度大、密度小、耐腐蚀等特性
C . 北斗导航专用ASIC硬件结合国产处理器打造出一颗真正意义的“中国芯”,其主要成分为SiO2
D . 港珠澳大桥设计使用寿命120年,水下钢柱镶铝块防腐的方法为牺牲阳极保护法
金属材料在日常生活中应用广泛,下列描述错误的是( )
A . 日常生活中的  金中金的含量接近100%
B . 随含碳量升高,碳钢的硬度增加、韧性下降
C . 铝合金可制作飞机零件和承受载重的高级运动器材
D . 钾钠合金的熔点很低
金中金的含量接近100%
B . 随含碳量升高,碳钢的硬度增加、韧性下降
C . 铝合金可制作飞机零件和承受载重的高级运动器材
D . 钾钠合金的熔点很低
 金中金的含量接近100%
B . 随含碳量升高,碳钢的硬度增加、韧性下降
C . 铝合金可制作飞机零件和承受载重的高级运动器材
D . 钾钠合金的熔点很低
金中金的含量接近100%
B . 随含碳量升高,碳钢的硬度增加、韧性下降
C . 铝合金可制作飞机零件和承受载重的高级运动器材
D . 钾钠合金的熔点很低
大国重器彰显中国实力,化学材料助力科技成果转化运用。下列说法正确的是( )
A . “蛟龙号”载人潜水器使用的钛合金是金属材料
B . “C919”大飞机使用的氮化硅陶瓷是传统硅酸盐材料
C . “玉兔二号”月球车使用的太阳能电池板材料是二氧化硅
D . “山东舰”航母使用的碳纤维是一种新型有机高分子材料
沈括在《梦溪笔谈》中写道:“古以剂钢为刃,柔铁为茎干,不而则多断折。剑之钢者,刃多毁缺”。其中“剂钢”即合金钢,“柔铁”即熟铁,下列说法正确的是( )
A . “剂钢”是混合物,“柔铁”是纯净物
B . 合金都由两种或两种以上的金属熔合而成
C . 改变合金中某种元素的含量可制得不同性能的合金
D . “剂钢”和“柔铁”的强度、硬度和熔点均比纯铁的高
下列关于合金的说法正确的是( )
①合金只能由两种或两种以上的金属组成 ②合金具有金属特性 ③碳钢和生铁的主要成分相同,故性能相同 ④改变原料的配比及生成合金的条件,可得到具有不同性能的合金
A . ②③
B . ②④
C . ①②
D . ①④
下列物质不属于合金的是( )
A . 奥运金牌
B . 青铜器
C . 生铁
D . 水银
新材料的蓬勃发展彰显化学学科的魅力。下列说法错误的是( )
A . 太阳能电池光电转换材料的主要成分是二氧化硅
B . 火星车的热控材料纳米气凝胶能发生丁达尔效应
C . 液冷散热技术使用的石墨烯属于无机非金属材料
D . 深海载人潜水器外壳使用的钛合金属于金属材料
《厉害了,我的国》展示了中国在探索太空、开发深海、开发5G技术等领域取得的举世瞩目的成就。它们与化学有着密切联系,下列对应关系错误的是( )
A . 5G手机芯片的关键材料——二氧化硅
B . 神舟飞船航天员穿的航天服的材料——多种合成纤维
C . 制造“蛟龙”号载人潜水器的耐压球壳采用的钛合金——金属材料
D . 神州飞船返回舱外表面使用的高温结构陶瓷的主要成分——新型无机非金属材料
下列描述错误的是( )
A . 可用检验加热是否产生CO2的方法鉴别碳酸钠和碳酸氢钠
B . 向碳酸钠固体中加入少量水,碳酸钠结块变成晶体,并伴随着吸热现象
C . 游泳池可用臭氧、漂粉精进行消毒
D . 青铜是我国使用最早的合金,其主要成分为铜和锡
最近更新
- 如图是某同学家中的电能表,现用它测量一只灯泡的实际功率.他关掉其他电器只让该灯泡工作,电能表转盘转过30转用时10min
- 分析下列省级行政区中,容易发生黄河凌汛的一组是A.宁夏回族自治区、山东省 B.山东省、河北省C.青海省、陕西省
- X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示。Z元素原子核外K层与M层电子数相等。下列说法
- 在人类历史上最早应用实验证明空气是由氮气和氧气组成的科学家是() A. 普利斯特里和舍勒 B. 道尔顿 C. 拉瓦锡 D
- 无机化学命名委员会(国际组织)在1989年作出规定:把长式周期表原先的主、副族及族号取消,由左到右改为18列,如氢和碱金
- There isthing as failure. Failure is just life trying to mo
- 单子叶和双子叶植物两个纲的植物最重要的区别是种子中子叶的数目。但在许多情况下,也可以利用叶子的形态进行区别。在校园植物调
- 依照画线句子,完成续写,要与画线句构成排比句。(4分)人生的意义在于奉献而不在于索取。如果你是一棵大树,就撒下一片阴凉;
- He has written some very good poems, but he is ________ kno
- 26.阅读下面的文字,根据要求作文。(60分) 把梦想当作一个温暖的藏身洞穴,就无法面对现实和生活的风雨。——meiya
- 细胞增殖是生物体的重要生命特征,下列相关叙述中正确的是() A.细菌不能进行有丝分裂,只能通过无丝分裂而增殖 B.利用放
- 作家萧伯纳说:人生有两大悲剧,一是没有得到你心爱的东西,另一是得到你心爱的东西。学者周国平则说:人生有两大快乐,一是没有
- (7分)在探究“动能大小与哪些因素有关”的活动中,提供以下器材:中间有沟槽的木质轨道(如图甲,其中AB部分倾斜并与平直部
- 下列有关实验操作的说法错误的是( ) A.中和滴定时盛待测液的锥形瓶中有少量水对滴定结果无影响 B.在酸碱中和滴定实验中
- 2007年6月28日,在新西兰召开第31届世界文化遗产大会上,“开平___与村落”历史性地载入《世界遗产名录》。自此,广
- 下述哪种情况下,单摆的周期会增大( ) A.增大摆球质量 B.缩短摆长 C.减小单摆振幅
- 根据下图有关信息判断,下列说法错误的是 A.镁离子(Mg2+)核内有12个质子B.镁的相对原子质量为24.31
- 甲、乙两人约好在“五、一”长假时间去天水市石马坪南山牡丹园观花游玩,决定在早晨7点半到8点半之间在石马坪的惠民商场门口会
- 司马迁,字子长,别称太史公,简称史迁。与 并称“史界两司马”,与 并称“班马”。主要作品为
- 某班九名同学在篮球场进行定点投篮测试,每人投篮子次,投中的次数统计如下: 4,3,2,4,4,1,5,0,3,则这级数据



