第三章 金属及其化合物 知识点题库
下列说法不正确的是( )
A . 金属单质和盐溶液的反应不一定是置换反应
B . “水滴石穿”是因为CaCO3与CO2、水发生了化学反应
C . 纯碱是制作面包等糕点的膨松剂,也是治疗胃酸过多的一种药剂
D . 少量液溴可用水封存,防止溴挥发
下列有关Si、Cl、N、S等非金属元素化合物的说法正确的是( )
A . 过量的铁粉与氯气反应生成FeCl2
B . 少量SO2通入Ca(ClO)2 溶液生成CaSO3沉淀
C . 常温下,1 mol Fe与足量浓硝酸反应,转移2NA个电子
D . 硅酸钠的水溶液是制备硅胶和木材防火剂的原料
下列物质中既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的化合物是( )
①Al ②Al2O3③Al(OH)3④AlCl3⑤NaHCO3 .
A . ①③④
B . ②③⑤
C . ②③④
D . 全部
下列原子构成的单质中既能与稀硫酸反应又能与烧碱溶液反应且都产生H2的是( )
A . 核内无中子的原子
B . 外围电子排布为3s23p3
C . 最外层电子数等于倒数第三层的电子数的原子
D . N层上无电子,最外层的电子数等于电子层数的金属原子
下列各项反应对应的图象正确的是( )
A . 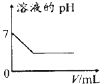 25℃时,向亚硫酸溶液中通入氯气
B .
25℃时,向亚硫酸溶液中通入氯气
B . 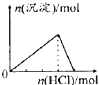 向 Na[Al(OH)4]溶液中通入 HCl气体
C .
向 Na[Al(OH)4]溶液中通入 HCl气体
C . 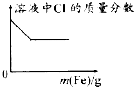 向少量氯化铁溶液中加入铁粉
D .
向少量氯化铁溶液中加入铁粉
D . 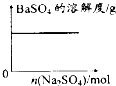 向BaSO4饱和溶液中加入硫酸钠
向BaSO4饱和溶液中加入硫酸钠
 25℃时,向亚硫酸溶液中通入氯气
B .
25℃时,向亚硫酸溶液中通入氯气
B .  向 Na[Al(OH)4]溶液中通入 HCl气体
C .
向 Na[Al(OH)4]溶液中通入 HCl气体
C . 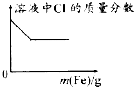 向少量氯化铁溶液中加入铁粉
D .
向少量氯化铁溶液中加入铁粉
D . 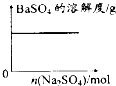 向BaSO4饱和溶液中加入硫酸钠
向BaSO4饱和溶液中加入硫酸钠
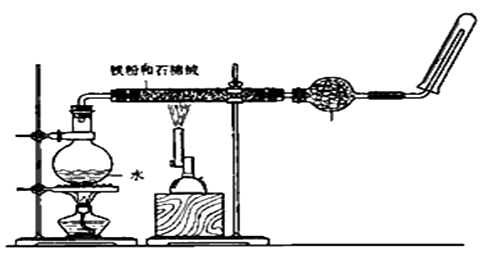
如图,在玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,用试管收集产生的经干燥的水蒸气,并靠近火焰点燃。
-
(1) 写出该反应的化学方程式 ,四氧化三铁是(填“氧化产物”还是“还原产物”) 。
-
(2) 加热烧瓶的作用是。
-
(3) 烧瓶底部放了几片碎瓷片,其作用是。
下列各组物质混合后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液
②过量NaOH溶液和明矾溶液
③过量生石灰投入到少量饱和NH4HCO3溶液
④Na2O2投入FeCl2溶液
A . 只有①
B . 只有③
C . 只有②③
D . 只有①③④
向前者的溶液中逐滴加入后者的溶液,不能看到先浑浊后澄清现象的是( )
A . 苯酚钠溶液、稀硫酸
B . AlCl3溶液、NaOH溶液
C . Fe(OH)3溶胶、稀硫酸
D . Na[Al(OH)4]溶液、稀盐酸
加热 42gNaHCO3和Na2CO3固体混合物,至没有气体放出时,剩余的固体质量是 35.8g。那么原固体混合物中Na2CO3的质量是()
A . 25.2g
B . 16.8 g
C . 10.6 g
D . 24.8g
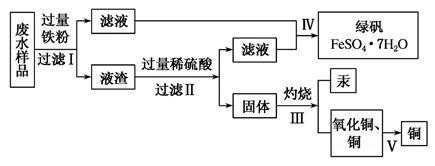
工业生产需要大量原料,消耗大量能源,在得到所需产品同时产生了大量废气、废水、废渣。某工厂排放的废水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,准备回收废水中的铜和汞,同时得到绿矾。他们设计了如下实验方案:
-
(1) 现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的玻璃仪器是设计简单实验检验绿矾是否变质,简述你的操作:。
-
(2) 步骤Ⅰ中加入过量铁粉的目的是,步骤Ⅱ中(填“能”或“不能”)用盐酸代替硫酸。
-
(3) 步骤V利用氧化铜制取铜有如下四种方案:
方案甲:利用氢气还原氧化铜;
方案乙:利用一氧化碳还原氧化铜;
方案丙:利用炭粉还原氧化铜;
方案丁:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。
从安全角度考虑,方案不好;从产品纯度考虑,方案不好。
-
(4) 写出步骤Ⅱ中涉及反应的离子方程式:;步骤Ⅳ得到绿矾的操作蒸发浓缩、。
下列根据实验操作和现象所得出的结论错误的是()
选项 | 实验操作 | 实验现象 | 结论 |
A | 在AlCl3溶液中逐滴滴入NaOH溶液至过量,然后通入CO2气体 | 先出现白色沉淀,后沉淀消失,最后又出现白色沉淀 | Al(OH)3是两性氢氧化物,但不能溶解在某些弱酸中 |
B | 向浓度均为0.1mol/L的MgCl2、CuCl2混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
C | 向Na2CO3溶液中加入浓盐酸,将产生的气体通入硅酸钠溶液中 | 产生白色浑浊 | 酸性:盐酸>碳酸>硅酸 |
D | 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液 | 前者溶液变蓝色,后者有黄色沉淀 | KI3溶液中存在I3- |
A . A
B . B
C . C
D . D
今有甲、乙、丙、丁、戊5种物质,在一定条件下,它们能按下图方式进行转化:
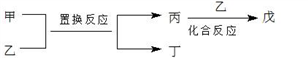
其推断正确的是( )
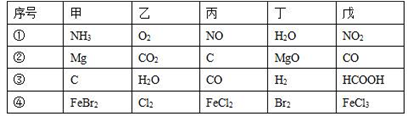
A . ①
B . ②
C . ③
D . ④
下列有关铝元素的说法正确的是( )
A . 铝粉可与氧化镁粉在高温条件下发生铝热反应
B . 铝粉与稀硝酸能反应产生氢气
C . 实验室中通常将氢氧化钠溶液滴入氯化铝溶液制取氢氧化铝
D . 氯化铝溶液中不断滴入氨水的过程中会先生成白色沉淀
下列各组物质混合时,前者过量和不足时,发生不同化学反应的是( )
A . NaOH溶液和AlCl3溶液
B . 稀H2SO4与Al(OH)3
C . Al和NaOH溶液
D . 氨水与Al2(SO4)3溶液
五种短周期元素A、B、C、D、E原子序数依次增大。B的最外层电子数是其电子层数的3倍;C、D、E的最高价氧化物对应水化物两两均可反应;A的单质在E的单质中能安静地燃烧,产生苍白色火焰。回答下列问题:
-
(1) B元素在元素周期表中的位置是,B、C、D形成的简单离子的半径由大到小的顺序是(用化学符号表示)。
-
(2) B与C能形成一种淡黄色的固体,其电子式为,它能用于呼吸面具的原因是(用其中一个化学方程式表示)。
-
(3) D的单质常用于焊接钢轨,请用化学方程式表示其反应原理。D、E的最高价氧化物对应水化物之间发生反应的离子方程式为。
下列“类比”合理的是( )
A . Fe与S反应生成FeS,则Cu与S反应生成Cu2S
B . C在足量的O2中燃烧生成CO2 , 则S在足量的O2中燃烧生成SO3
C . Cl2与水反应生成HCl和HClO,则F2与水反应生成HF和HFO
D . Na2O2与CO2反应生成Na2CO3和O2 , 则Na2O2与SO2反应生成Na2SO3和O2
《厉害了,我的国》展示了中国探索太空,开发深海,建设世界第一流的高铁、桥梁、码头,5G技术联通世界等取得的举世瞩目的成就。它们与化学有着密切联系。下列说法正确的是( )
A . 制造手机芯片的关键材料是二氧化硅
B . “神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐
C . 我国提出网络强国战略,光缆线路总长超过三千万公里,光缆的主要成分是晶体硅
D . C919大型客机使用了大量先进复合材料、铝锂合金等,铝锂合金可减轻机身自重
下列叙述正确的是( )
①发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
②过氧化钠和氧化钠都是碱性氧化物,两种氧化物均可作潜艇中的供氧剂
③碳酸钠在医疗上是治疗胃酸过多的一种药剂
④氧化铁常用于制作红色油漆和涂料
⑤铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物
⑥焰色试验体现的是化合物的物理性质
⑦雾霾天,汽车车灯照出通路的现象属于丁达尔效应
A . ①③⑤⑦
B . ①④⑤⑦
C . ①③④⑤
D . ②③⑤⑥
下列说法中正确的是( )
A . 碳酸氢铵常用作氮肥,不可与碱性肥料混用
B . 明矾净水是因为可以生成杀菌消毒的物质
C . 铝制品的耐腐蚀性强,说明铝的化学性质不活泼
D . 氮气性质稳定,可用于工业制镁的冷却剂
16.8g NaHCO3和7.8gNa2O2在密闭容器中灼烧,充分反应后,将密闭容器保持温度为500℃,最后容器内物质是( )
A . Na2CO3 , CO2 , O2
B . Na2CO3 , O2 , 水蒸气
C . Na2CO3 , CO2 , O2 , 水蒸气
D . NaHCO3 , Na2CO3 , O2
最近更新
- 寂寞红柳 (14分) 山谷 ①车一过托克逊,就进入了塔克拉玛干大沙漠,除脚下一条黑色的柏油路,两旁和天尽头都是浩瀚无际的
- O. Henry was a pen name used by an American writer of short
- 右面漫画告诉我们 A.市场调节具有滞后性、盲目性 B.要树立以人为本的思想 c.必须提高劳动者的职业技能
- 点P0(-1,2)到下列直线的距离:(1)2x+y-10=0;(2)3x=2.
- 下列句子没有语病的一项是( ) A、昭通的秋天是令人向往的季节,市民们都在这时纷纷步出户外,登高望远,一览秋天
- (08年浙江卷文)用1,2,3,4,5,6组成六位数(没有重复数字),要求任何相邻两个数字的奇偶性不同,且1和2相邻,这
- 不能引起消化道传染病的途径是( ) A.饮用水 B、餐具 C.血液 D、瓜
- 用嘴吹灭燃着的生日蜡烛,利用的主要灭火原理是( ) A.隔绝空气 B.降低可燃物的着火点 C.清除可燃物 D.使
- 2011年8月12日至8月23日,第26届世界大学生夏季运动会在深圳举行。深圳市政府为此开通了相关网站,通过网上征求意见
- 政府的管理和服务是否被人民认可和接受,是区分政府有无权威的标志。一个政府是否有这种权威,从根本上讲是由________决
- 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: ①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶
- 在△ABC中,a,b,c分别是角A,B,C所对的边,若(a+b+c)(sinA+sinB-sinC)=3asinB,则C
- 如图所示,物块和斜面体的质量分别为m.M,物块在平行于斜面的推力F作用下沿斜面加速度a向上滑动时,斜面体仍保持静止.斜面
- 今年4月,在部分省市发现某些厂商用工业明胶来生产药用胶囊,严重危害患者的身体健康.工业明胶中含有毒的重铬酸钠(Na2Cr
- (4分)将一个带电量为1.0×10-8C的点电荷从A点移到B点,电场力做功是2.0×10-6J,则A、B两点的电势差为_
- 向含有FeBr2、FeI2的溶液中通入一定量的氯气后,再向溶液中滴加KSCN溶液,溶液变为红色,则下列叙述不正确的是 A
- 在森林中设防火道的目的是 A.隔绝空气 B.便于运水 C.降低温度 D.隔离可燃
- 若圆锥的侧面展开时一个弧长为l6的扇形,则这个圆锥的底面半经是
- Don't be angry with the girl.She made the mistake ________.
- —Can we finish the work with ______ moneyand ______ people?



