第二节 化学计量在实验中的应用 知识点题库
将2.3克钠投入W克水中,所得溶液中Na+与水分子个数之比1:100,溶液密度为1.2g.ml-1 , 下列有关说法不正确的是( )
A . W=181.8
B . 此过程中,水被还原,共得到0.1NA个电子
C . 所得溶液中溶质质量分数约为2.174%
D . 仅据上述条件无法求算所得溶液的物质的量浓度
由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO2、H2和CO的体积比为( )
A . 29:8:13
B . 22:1:14
C . 13:8:29
D . 26:15:57
将50g密度ρ=0.98g/mL的10%的氨水和100g密度ρ=0.93g/mL的40%的氨水混合,得到ρ=0.95g/mL氨水溶液,求所得氨水的物质的量浓度是多少?
下列溶液中,H+的物质的量浓度为1mol/L的是( )
A . 将1 mol HCl溶于1 L水中得到的溶液
B . 将1 mol SO3溶于1 L水中得到的溶液
C . 将1 mol H2SO4溶于水制成的体积1 L的溶液
D . 将0.5 mol SO3溶于水制成的体积1 L的溶液
用固体氢氧化钠配制一定物质的量浓度溶液时,下列操作能导致溶液浓度偏高的是( )
A . 在烧杯中溶解时,有少量液体溅出
B . 样品中混有碳酸钠固体
C . 容量瓶使用前未经干燥
D . 定容时俯视容量瓶刻度线
质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水.得到的溶液每毫升质量为q g,物质的量浓度为c.则溶质的分子量(相对分子质量)为( )
A . 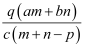 B .
B . 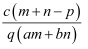 C .
C . 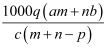 D .
D . 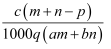
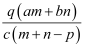 B .
B . 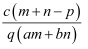 C .
C . 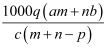 D .
D . 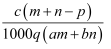
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是:( )
A . 甲的分子数比乙的分子数多
B . 甲的摩尔体积比乙的摩尔体积小
C . 甲的物质的量比乙的物质的量少
D . 甲的相对分子质量比乙的相对分子质量小
把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀,该混合溶液中钾离子浓度为( )
A . 10 (b-2a)mol·L-1
B . 5(b-2a)mol·L-1
C . 2(b-a)mol·L-1
D . 10(2a-b)mol·L-1
现有1 L的 Al2(SO4)3溶液,含Al3+ 216 g,取250 mL溶液稀释到4 L,则稀释后溶液中的SO42-物质的量浓度是。
下列说法错误的是( )
A . 保存FeCl2溶液时,应在试剂瓶中加入少量铁粉
B . 焰色反应时,铂丝需用稀硫酸洗净,并在火焰上灼烧至无色
C . 蒸馏时加入沸石的目的是为了防止暴沸
D . 使用容量瓶配制溶液定容时仰视刻度线会使得所配溶液浓度偏小
相同质量的下列各烃,完全燃烧后生成二氧化碳最多的是()
A . 丁烷
B . 乙烯
C . 乙炔
D . 甲苯
现用物质的量浓度为0.100 0 mol·L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:
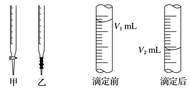
-
(1) 用标准NaOH溶液滴定时,应将标准NaOH溶液注入(填“甲”或“乙”)中。
-
(2) 某学生的操作步骤如下:
A.移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴部分充满溶液;
D.取标准NaOH溶液注入碱式滴定管至“0”刻度以上 2~3 mL;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
正确操作步骤的顺序是→→→→A→(用字母序号填写)。判断到达滴定终点的实验现象是
-
(3) 右上图是碱式滴定管中液面在滴定前后的读数, c(HCl)= mol·L-1。
-
(4) 由于错误操作,使得上述所测盐酸溶液的浓度偏高的是________(填字母)。A . 中和滴定达终点时俯视滴定管内液面读数 B . 酸式滴定管用蒸馏水洗净后立即取用25.00 mL待测酸溶液注入锥形瓶进行滴定 C . 碱式滴定管用蒸馏水洗净后立即装标准溶液来滴定 D . 用酸式滴定管量取待测盐酸时,取液前有气泡,取液后无气泡
草酸晶体的组成可表示为H2C2O4•xH2O,通过下列实验测定x值,步骤如下:
①称取6.30 g草酸晶体配成100 mL水溶液。
②取25.00mL所配草酸溶液置于锥形瓶中,加入适量稀硫酸,用0.5000mol•L-1KMnO4溶液进行滴定,到达滴定终点时,消耗KMnO4溶液10.02mL。
③重复②步骤2次,消耗KMnO4溶液的体积分别为11.02mL和9.98mL。已知:H2C2O4 +MnO4- +H+ → CO2 ↑+Mn2++H2O (方程式未配平)
-
(1) 步骤①配制草酸溶液时,需用的玻璃仪器:烧杯、玻璃棒和;
-
(2) 判断到达滴定终点的实验现象是;
-
(3) 其它操作正确的情况下,以下操作会使测定的x值偏小的是______;A . 滴定管水洗后未用KMnO4溶液润洗 B . 锥形瓶用蒸馏水洗净之后,用草酸溶液润洗 C . 开始滴定时滴定管尖嘴处有气泡,滴定结束气泡消失 D . 滴定终点读数时,俯视滴定管的刻度
-
(4) 根据以上实验数据计算x值 。 (写出计算过程)
“质量摩尔浓度”也是一种表示溶液组成的物理量,溶质B的质量摩尔浓度是用单位质量的溶剂中所含溶质B的物质的量来表示溶液组成的物理量,单位为mol·kg-1或mol·g-1。已知20℃时质量分数为20%的NaOH溶液的密度为1.16g·cm-3 , 则该溶液的质量摩尔浓度为( )
A . 6.25mol·kg-1
B . 4.25mol·kg-1
C . 6.25mol·g-1
D . 4.25mol·g-11
现有Ag某结晶水合物(R·xH2O)受热后失去全部结晶水,质量变为ag,则R相对原子质量是( )
A . 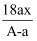 B .
B . 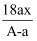 C .
C . 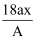 D .
D . 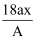
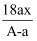 B .
B . 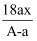 C .
C . 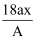 D .
D . 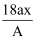
-
(1) I.氨和硝酸都是重要的工业原料,标准状况下,将640L氨气溶于水形成1L氨水,则此氨水的物质的量浓度为mol/L(保留三位有效数字).将体积为12mL的试管充满NO2气体后,倒立于水槽中(保持同温同压),液面稳定后,保持相同条件下再通入O2 , 若要液面仍在原来的位置,则通入O2的体积为mL。
-
(2) 工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH- =NO2-+NO3-+H2O和NO+NO2+2OH- =+H2O(配平该方程式)。
-
(3) Ⅱ.在标准状况下,分别取30mL相同浓度的盐酸依次装入①②③试管中,然后分别慢慢加入组成相同的镁铝混合物,相同条件下,测得有关数据如表所示(反应前后溶液体积不发生变化)。
实验序号
①
②
③
混合物质量/mg
255
510
1020
气体体积/mL
280
336
336
①组实验中,盐酸,(填过量或不足);②组实验中,盐酸,(填过量或不足)。
盐酸的物质的量浓度为mol/L。
混合物中Mg和Al的物质的量之比为。
一定质量铜和适量的浓硝酸反应,随着反应的进行,所生成的气体颜色逐渐变浅,当铜反应完毕后,共收集到11.2L气体(标况),将该气体与0.325 mol O2混合溶于水,恰好无气体剩余。则反应中消耗硝酸的物质的量( )
A . 1.2mol
B . 1.1mol
C . 1.8 mol
D . 1.6mol
以物质类别为横坐标,化合价为纵坐标可以绘制某一元素的价类图。氮元素的价类图如图所示,下列有关说法错误的是( )
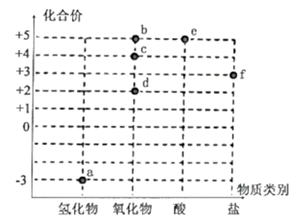
A . 实验室用铜制取d,生成标准状况下5.6L气体d时,消耗铜的质量为24g
B . 从 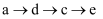 的转化过程中,必须向每个步骤中提供氧化剂
C . c、d同时通入
的转化过程中,必须向每个步骤中提供氧化剂
C . c、d同时通入  溶液中仅生成f一种盐,反应的离子方程式为
溶液中仅生成f一种盐,反应的离子方程式为 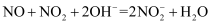 D . a与c在一定条件下反应生成无污染的物质,该反应中氧化剂与还原剂的物质的量之比为3:4
D . a与c在一定条件下反应生成无污染的物质,该反应中氧化剂与还原剂的物质的量之比为3:4
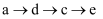 的转化过程中,必须向每个步骤中提供氧化剂
C . c、d同时通入
的转化过程中,必须向每个步骤中提供氧化剂
C . c、d同时通入  溶液中仅生成f一种盐,反应的离子方程式为
溶液中仅生成f一种盐,反应的离子方程式为 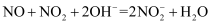 D . a与c在一定条件下反应生成无污染的物质,该反应中氧化剂与还原剂的物质的量之比为3:4
D . a与c在一定条件下反应生成无污染的物质,该反应中氧化剂与还原剂的物质的量之比为3:4
实验室中下列做法正确的是( )
A . 中和滴定时,滴定管用所盛装的溶液润洗 2~3次
B . 配制 FeCl 3 溶液时,将 FeCl 3 固体加入适量蒸馏水中,搅拌使其完全溶解
C . 进行中和热的测定中,为了使反应完全,必须保证酸和碱恰好完全反应
D . 向容量瓶转移液体时,直接将溶液注入容量瓶中
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 12g金刚石和石墨混合物中含有的共价键数目为2NA
B . 用铜电极电解饱和食盐水,若线路中通过NA个电子,则阳极产生11.2L(标准状况)气体
C . 常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA
D . 6.8g液态KHSO4中含有0.1NA个阳离子
最近更新
- 9. 下列句子中不包含通假字的一项是(3分) A. 祖母刘今年九十有六 B. 而刘夙婴疾病,常在床蓐 C. 臣以险衅,夙
- Don’t leave your work . done half B. half done C. a hal
- 下图是某城市内部和对外联系路线图,据图回答下列问题。24.从地租水平看 A.甲>乙>丙>丁 B.乙>甲>丙>
- 李某想购买一辆标价为10万元的汽车,在已有4万元存款的同时,李某又向银行贷款6万元.其中10万元是这车的( )
- 某静电场沿x方向的电势分布如图所示,则( ) A.在0—x1之间不存在沿x方向的电场B.在0—x1之间存在着沿x方
- 选出下列各项中字形不合规范的一项:( ) A. 惮精竭虑 门可罗雀同仇敌忾 原形毕露 B.暴殄天物
- 下面漫画所反映的情况()A.可以增强国有经济的主导作用 B.会削弱公有制经济的主体地位 C.是国有企业改革中的必然现象
- ----What’s the noise? ----Oh, my neighbour’s house ________
- 下列变化中,属于化学变化的是() A. 胆矾研碎 B. 品红扩散 C. 酚酞变红 D. 干冰升华
- 质量为m1和m2的两个物体,由静止从同一高度下落,运动中所受的空气阻力分别是F1和F2.如果发现质量为m1的物体先落地,
- 蓝藻属于自养型生物是因为 (
- 设Sn是等差数列{an}前n项和,且S10=110,a10-a6=8,Cn=.(1)求数列{Cn}的通项公式;(2)设f
- 下列物质不能跟金属钠反应的是 ( ) A.甲醇 B.乙醚 C.福尔马林 D.乙二醇
- Why do people buy art? To answer this question, ask yourself
- 燃烧法是测定有机物化学式的一种重要方法,现在完全燃烧0.1mol某烃,燃烧产物依次通过浓硫酸和浓氢氧化钠溶液,实验结束后
- 有一些部门和地方,电子政务的要领概念常被“简单化”,官方网站既无必要的经费,也无专门的技术维护人员,网站“一建了之”“长
- 溶液、胶体和浊液这三种分散系的根本区别是 A.是否是大量分子或离子的集合体 B
- (共5小题;每小题2 分,满分10 分) 根据短文内容,从短文后的选项中选出能填入空白处的最佳选项。选项中有
- 隋朝大运河,连接淮河和长江的一段是( ) A.永济渠 B.江南河 C.通济渠 D.
- “有志者事竟成,破釜沉舟百二秦关终属楚;苦心人天不负,卧薪尝胆三千越甲可吞吴。”此对联所涉及的历史事件分别发生在(



