单元2 金属的性质 知识点题库
选项 金属 盐溶液 | A | B | C | D |
ZnSO4溶液 | ﹣ | Fe | Fe | Ag |
FeSO4溶液 | Zn | Ag | ﹣ | Zn |
AgNO3溶液 | Fe | ﹣ | Fe | ﹣ |

-
(1) 同学们经过观察很快将四种金属分为两组.他们的分组依据是
-
(2) A在空气中灼烧的现象是;B与稀盐酸反应的化学方程式为.
-
(3) 用上述方法区分金属的同时,还可以验证金属活动性顺序.由Ⅱ组可以获知的活动性顺序是;若要验证Cu、Ag的活动性顺序,还需补做一个实验,写出实验中能发生反应的化学方程式.
-
(4) 回收废弃电器、电子产品中的金属材料既可以减少环境污染,又可以保护金属资源.保护金属资源的途径还有(写一条即可).
资料:铁、镍均能被磁铁吸引。镍在化合物中显+2价。

-
(1) 三种金属的活动性由强到弱的顺序是:Zn Fe (H) Cu,推断镍在其中的位置,并写出判断依据。
-
(2) 写出步骤Ⅱ中发牛的反应的化学方程式。
-
(3) 如何确定镍的质量?简述原理。
 B . 向一定质量饱和石灰水中加入氧化钙
B . 向一定质量饱和石灰水中加入氧化钙  C . 用等质量、等质量分数的H2O2溶液来制取O2
C . 用等质量、等质量分数的H2O2溶液来制取O2  D . 将过量的、等质量的镁和锌分别加入到等质量、等质量分数的稀硫酸中
D . 将过量的、等质量的镁和锌分别加入到等质量、等质量分数的稀硫酸中 

-
(1) 烧渣在浸取前要研磨成粉末状,其目的是。
-
(2) 用稀硫酸浸取烧渣时发生的化学反应都属于反应(填写基本反应类型)。
-
(3) 在滤液中加入适量Fe时发生的化合反应的方程式为。
-
(4) 若在实验室中进行操作①,该操作主要包括、降温结晶、过滤等,其中两次操作中都用到的玻璃仪器是,得到的(NH4)2SO4晶体在农业上可以用作。
-
(5) 操作②中得到的X可以循环利用,则X为。

-
(1) 下列金属制品中,利用金属导热性的是(填字母)。
A 金属硬币 B 铝制导线 C 铜制火锅
-
(2) 波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成。不能用铁质容器配制波尔多液的原因是 (用化学方程式表示)。
-
(3) 防止金属锈蚀是保护金属资源的有效途径之一。洁净的铁钉在下列情况下容易生锈的是(填字母)。
A 在干燥的空气中 B 在潮湿的空气中 C 浸没在植物油中
-
(4) 铝具有很好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化。氧化铝难溶于水,却能溶于酸。写出氧化铝与稀硫酸反应的化学反应化学方程式。
-
(5) 向铁粉和氧化铜粉末的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,得滤渣和滤液。向滤液中加一洁净铁片,未看到铁片有任何变化。则滤液中含有的溶质是 (填化学式),滤渣中一定含有的物质是(填化学式)
| 选项 | 实验目的 | 实验方法 |
| A | 鉴别H2和 CO | 分别点燃,在火焰上方罩一干冷烧杯 |
| B | 比较Fe、Ag、Cu金属活动性 | 将Fe和Cu分别放入AgNO3溶液中 |
| C | 检验一瓶气体是否为 CO2 | 将燃着的木条伸入瓶中 |
| D | 鉴别H2SO4溶液和 NaCl 溶液 | 分别滴加酚酞试液 |
(查阅资料)Fe的活动性比Cu强。
-
(1) (进行猜想)对三种金属的活动性顺序做出以下猜想:
猜想一:R>Fe>Cu
猜想二:
猜想三:Fe>Cu>R
-
(2) (收集证据)为了验证哪一种猜想成立,甲乙丙三位同学分别进行了实验探究。
主要操作
主要现象
实验结论
甲
将打磨好的R丝插入盛有硫酸铜溶液的试管中
猜想一正确
乙
将粗细相同打磨好的R丝、Fe丝分别插入装有等量稀盐酸的两支试管中
R丝表面产生气泡速率比铁丝表面产生气泡速率(填“快”或“慢”)
丙
将粗细相同打磨好的R丝,铁丝分别在空气中点燃
R丝在空气中剧烈燃烧,铁丝在空气中
-
(3) 写出铁与盐酸反应的化学方程式。
-
(4) 铝制品一般抗腐蚀性好的原因是 。

已知: 
下列说法正确的是( )
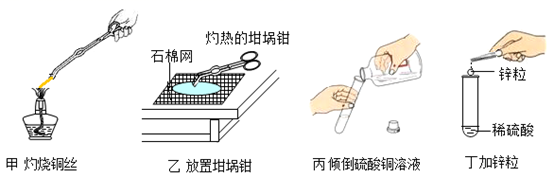
 CuO,属于化合反应
B . 图乙中观察到黑色的铜丝变红
C . 在一只盛有少量稀盐酸的试管中,先后添加足量的铁丝、锌片、银丝,该方案可以探究出锌、铁、银的金属活动顺序
D . 上述操作有一处不符合题意,是丁图所示操作
CuO,属于化合反应
B . 图乙中观察到黑色的铜丝变红
C . 在一只盛有少量稀盐酸的试管中,先后添加足量的铁丝、锌片、银丝,该方案可以探究出锌、铁、银的金属活动顺序
D . 上述操作有一处不符合题意,是丁图所示操作
-
(1) 支撑“中国天眼”的角钢塔架中含有锰(Mn),锰可以与稀盐酸发生置换反应,生成物中锰元素显+2价。则锰与稀盐酸反应的化学方程式为。
-
(2) 利用催化剂可消除室内装修材料释放的甲醛,其反应微观示意图如下:

①甲醛分子由构成。
②该反应过程中两种生成物的质量比为。

已知:加热的条件下,Zn、Cu都可以与氧气反应生成相应的金属氧化物。
-
(1) 烟泥最初处理需要除油污,用洗涤剂除油污的过程中发生了现象。步骤①产生的废气B中,一定含有的有害气体是(填化学式)。环保处理最好采用的试剂是(填字母序号)。
A浓硫酸 B食盐水 C石灰乳
-
(2) 写出步骤④中得到铜的化学方程式,它属于基本反应类型中的反应。
-
(3) 步骤③和④中主要操作的名称是。
-
(4) 我国古代就制得了一种外观似金子的锌和铜的合金,也就是黄铜,它的硬度比纯铜(填“高”或者“低”)。
-
(5) 取少量的溶液C,往其中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液。往滤渣中加入稀盐酸有气泡产生,则滤液中一定没有(填字母序号)。
A硫酸镁 B硫酸锌 C硫酸铜 D硫酸铜和硫酸锌
-
(1) 取少量光亮的镁条于试管中,向其中加入稀盐酸,观察到的现象可推断二者发生了化学反应;
-
(2) 若验证镁与稀盐酸反应后的溶液中有盐酸剩余,下列实验设计可行的是______;A . 取生锈的铁钉于试管中,加入反应后的溶液 B . 取少量反应后的溶液于试管中, 滴加AgNO3溶液 C . 取少量反应后的溶液于试管中,滴加稀氢氧化钠溶液
-
(3) 向镁条中加入过量稀盐酸,完全反应后,再加入过量氢氧化钠溶液,生成5.8g氢氧化镁沉淀。
①写出加入氢氧化钠溶液时,生成氢氧化镁沉淀的化学方程式;
②计算镁条与稀盐酸完全反应后生成MgCl2的质量为g。
-
(1) 镁条在空气中能直接点燃,说明镁的金属活动性比铁(填“强”、“弱”)。
-
(2) 小明设计了如下探究实验。
①取一支试管,放入一根镁条,加入一定量稀盐酸,观察到有无色气体产生,发生反应的化学方程式为;将镁条换为铁丝,重复上述操作,可观察到产生气体的速率(填“变快”、“变慢”或“不变”)。
②另取一支试管,放入一根镁条,加入一定量硫酸铜溶液,观察到镁条表面有少量气泡产生,且有黑色物质生成。
-
(3) 镁条与硫酸铜溶液反应的现象让小明感到困惑,他去图书馆查到相关资料:
资料1:硫酸铜溶液在配制时加入了少量硫酸;
资料2:当金属粉末颗粒很小时,容易成为黑色;:
资料3:实验过程中发生了一系列复杂的反应,生成的黑色粉末可能是CuO、Cu中的一种或两种。
①镁条与硫酸铜溶液反应的实验中产生的气体可能为。
②小明进一步设计实验确定黑色粉末的成分,请在下表中补全实验方案,
实验操作
实验现象
结论
将黑色粉末过滤、晾干后,分成两份
将其中一份装入硬质玻璃管中,向其中通入CO后,加热,并将生成的气体通入澄清石灰水中
澄清石灰水变浑浊
结论1
将另一份置于坩埚中,称其质量为m1 , 在空气中加热一段时间后冷却,称其质量为m2
现象1
黑色粉末中含Cu
表中,结论1是;现象1是m1m2(填“大于”、“小于”或“等于”)。
①一定有锌、②一定有铁、③一定有铜、④可能有锌、⑤可能有铁、⑥可能有铜。
- PCR技术的操作步骤依次是 A.高温变性、中温延伸、低温复性 B.高温变性、低温
- 想当年,金戈铁马, 。(辛弃疾《京口北固亭怀古》)
- 在含有Fe3+、Fe2+、Al3+、NH4+的溶液中,加入足量的Na2O2固体并加热,充分反应后,再加入过量的稀盐酸,完
- 中国古代天文发达,近代欧洲天文成就斐然,近代自然科学就是以这个领域的革命为开端。下列有关评述正确的是①二者的兴起都是由于
- 向含 l mol HCl和l mol MgSO4的混合溶液中加入1mol•L-1 Ba(OH)2溶液,产生沉淀的 物质
- 人体内缺碘元素易导致 A.侏儒症 B.佝偻病 C.贫血症 D
- 19世纪末20世纪初,美、英、俄、德的议会制度都得到发展,但英美的议会政治远比俄德成熟。形成这种局面的历史根源是 A.资
- 如图所示,ABCD为竖直放在场强为E=104V/m的水平匀强电场中的绝缘光滑轨道,其中轨道的BCD部分是半径为R的半圆环
- 2009年12月7日,中共中央政治局召开会议,分析研究2010年经济工作。回答1-2题。 1会议指出,明年要保持宏观经济
- 人类最早使用的合金是由铜、锡形成的青铜,我国的锡储量占世界第一位。明代宋应星所著《天工开物》记载的炼锡方法基本上就是现代
- 一列横波沿x轴传播,波速为12m/s,在x轴上有A、B两点,它们各自的坐标分别为,,当A点在正的最大位移时,B点恰好在平
- 反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙
- 关于电流通过导体时产生的热量,下列说法中正确的是 A.根据可知,时间相同,电阻越大,电流产生的热量越少B.根据
- 秦统一后,全国统一使用的规范文字是 A.甲骨文 B.金文 C.小篆 D.
- 阅读下面这首唐诗,然后回答问题。 喜达行在所(其二) 杜甫 秋思胡笳夕,凄凉汉苑春。生还今日事,间道暂时人。 司隶章初睹
- 卫星电话信号需要通过地球卫星传送。如果你与同学在地面上用卫星电话通话,则从你发出信号至对方接收到信号所需要最短时间最接近
- 第二次工业革命的首要标志是 A.科学技术的发展突飞猛进 B.人类跨入电子计算机时代 C.新发明促进了生
- 如图,⊙O的半径为2,C1是函数y =x2的图象,C2是函数y=﹣x2的图象,则阴影部分的面积是 .
- .如图,图中x的值为( )A.50 B.60 C.70
- “快来扒一扒是谁在规划十三五?党中央国务院,还有各级部委办,工人农民企业家,专家教授你我他,中国的十三五,大伙儿来做主



