第四单元 金属 知识点题库

-
(1) 在上图汽车的部件中主要由有机合成材料制成的是;
-
(2) 在汽车的电路中主要使用的是铜线,这是利用了铜的性;
-
(3) 汽车表面的烤漆不仅美观,还能起到的作用
-
(4) 化石燃料的大量使用,带来了环境的污染和资源的枯竭等问题。我市自2018年开始推广使用车用乙醇汽油,到2019年实现全市全覆盖。乙醇(C2H5OH)燃烧的化学方程式是,推广使用乙醇汽油的好处是 , (写出两条即可)。
 见图
见图 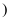 ,请根据图象信息判断,下列说法正确的是
,请根据图象信息判断,下列说法正确的是 
A.四种金属与酸反应的速率: 
B.四种金属的活动性顺序: 
C.同质量的四种金属与足量酸反应得到氢气的质量: 
D.同质量的Al、Mg、Fe、Zn四种金属与足量酸反应得到氢气的质量比:

-
(1) 写出ab段发生反应的化学方程式。
-
(2) cd段溶液质量为什么增大?
-
(3) e点得到的固体中有什么物质?

-
(1) 该实验取用的样品质量为:g;
-
(2) 样品中铁的质量分数为:;
-
(3) 小王不慎在反应结束后,向烧杯中多加了20g稀硫酸,此时,溶液中亚铁离子在溶液总质量中的质量分数为:,若在该图象中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填“上方”、“下方”或“线上”).

 。
。 试计算:
-
(1) Cu2S 中铜的质量分数。
-
(2) 现有含Cu2S 80%的铜矿400t,理论上能炼出多少铜?
A
测定空气中O2的含量  B 稀释浓硫酸
B 稀释浓硫酸 
C 铁丝在空气中的变化  D 一氧化碳还原氧化铁
D 一氧化碳还原氧化铁 
-
(1) 上述实验中不能达到实验目的是(填字母),理由是;
-
(2) A中可燃物应取过量的原因是;
-
(3) B中玻璃棒的作用是;
-
(4) 一段时间后,C中的实验现象为;
-
(5) D中硬质玻璃管内发生反应的化学方程式为,酒精灯的作用是。

-
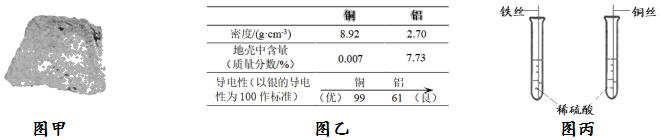
(1) 图甲所示赤铁矿的主要成分是(填化学式);
-
(2) 家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据图乙的信息分析,其原因是;
-
(3) 在空气中,铝具有很好的抗腐蚀性,其原因用化学方程式表示为;
-
(4) 为探究铁、铜的金属活动性,分别将铁丝、铜丝插入稀硫酸中(图丙),说明铁比铜的金属活动性更强的实验现象是,反应的化学方程式是。
 Si+2CO↑下列说法正确的是( )
Si+2CO↑下列说法正确的是( )

①从图象可得出,镁比铁的活动性强②从图象可得出,a点时消耗两种金属质量相同③若硫酸有剩余,两种金属产生的氢气质量相同④若两种金属有剩余,两者消耗硫酸的质量相同
-
(1) 有镁、锌、银三种金属,与同浓度稀硫酸发生反应,最剧烈的是(填化学式)。
-
(2) 合金比纯金属有更广泛的用途,下列属于合金的(填字母)。
A 不锈钢 B 水银 C 黄铜 D 金刚石
-
(3) 为验证Zn、Cu、Ag三种金属的活动性顺序,某同学选用如下试剂组进行实验,其中不合理的一组(填序号)。
①Zn、Ag、CuSO4溶液 ②Cu、AgNO3溶液、ZnSO4溶液 ③Ag、Cu、ZnSO4溶液
-
(4) 已知金属单质的活泼性Fe>Cu,则Fe+CuSO4=Cu+FeSO4 , 非金属单质与金属单质有类似性质,活泼性Cl2>Br2 , 将Cl2通入NaBr溶液中发生反应的化学方程式为。

-
(1) CaCl2的作用是。
-
(2) 为保证实验成功,实验前需进行的一项操作是。
-
(3) 一周后,两支具支试管中的现象分别是,玻璃管中红墨水的变化是。
 总书记考察南通长江生态,对壮阔的长江留下深刻的印象,对南通的发展给了充分的肯定。
总书记考察南通长江生态,对壮阔的长江留下深刻的印象,对南通的发展给了充分的肯定。
-
(1) 长江的水美,空气清新。
①澄清透明的长江水属于(填“纯净物”或“混合物”),检验南通濠河水是软水还是硬水,可向水样中加入,搅拌,观察现象。
②高铁酸钾(K2FeO4)是一种常用的净水剂,其中铁的化合价为。
-
(2) 南通地铁的建造和运行对经济发展带来深远的影响。
①修建地铁需要大量的钢铁,写出用一氧化碳和赤铁矿(主要成分Fe2O3)高温炼铁的化学方程式。在列车上刷油漆的目的是为了防止铁与发生反应而生锈。
②建造时,包装材料所用的聚乙烯属于塑料(填写“热塑性”或“热固性”)。
③地铁运营后,将会给乘客准备丰富的食物,包括米饭、牛排、海带、豆腐干、水果、面包等,其中富含蛋白质的食物是。
-
(1) 近年来,我省多地纷纷开展文明城市创建工作,垃圾分类回收是其中一项重要举措。通常用金属做街道垃圾桶的内筒,请你说出使用铝合金做内筒的优点是(写出一点即可);空易拉罐应放入(填“可回收”或“不可回收”)筒中。
-
(2) 垃圾桶外筒用铁制,铁制品易锈蚀,下列措施能防止铁制品锈蚀的是 (填字母)。A . 涂油、喷漆 B . 用盐水清洗 C . 久置于酸性环境 D . 镀耐腐蚀的铬层
-
(3) 将一定质量的铁粉加入Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。
①写出往溶液中加入铁粉后能够发生的反应的化学方程式:(写一个即可)。
②下列有关说法正确的是(填字母)。
A.若滤液为浅绿色,则滤渣中一定含有铁、铜、银
B.若滤液为蓝色,则滤渣中一定含有银,可能含有铜
C.若滤渣中含有银、铜,则滤液中一定含有Al3+、Fe3+
D.若滤渣中加入稀盐酸无气泡产生,则滤液中一定含有Al3+、Fe2+、Ag+、Cu2+

-
(1) 采矿1 图:“水锡……其质黑色……愈经淘取”是指水中淘取锡砂(锡矿石),锡砂主要成分为 SnO2 , (填“易”或“难”)溶于水,水中淘取锡砂的分离过程化学上称之为,SnO2中锡元素与氧元素的质量比为。
-
(2) 冶炼2 图:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(鼓入空气)熔化。”
①高温下,木炭会把锡从锡砂(SnO2)中还原出来,反应的化学方程式为。
②炼锡时,有关键的一步“点铅勾锡”,即加铅能使锡较易熔化流出,其原因是。
-
(3) 使用:
①锡是大名鼎鼎的“五金”——金、银、铜、铁、锡之一。金属单质由构成。
②古代锡器常用来饮酒喝茶,很少装酸性物质,原因是。
- 李克强担任总理后,面对地方债隐现危机、贸易壁垒增加、热钱出逃、银行钱荒等严峻考验,在他的“新政”中,挤水分、调结构、简政
- Being young means having all kinds of possibilities, so you
- 如图表示绿色开花植物的有性生殖过程,下列叙述正确的是() A. 图中所示的传粉方式是异花传粉 B. 受精是①中的精子和③
- 世界最高峰珠穆朗玛峰海拔8844米,我国陆地最低的吐鲁番盆地在海平面以下155米,两地相对高度是 A.8693米
- 马克思主义哲学的直接理论来源是( ) A.黑格尔的辩证法和费尔巴哈的唯物主义B.以李嘉图为代表的古典经济学 C
- 在做“验证牛顿第二定律”的实验中 (1)本实验备有下列器材:电磁打点计时器、秒表、天平(带有一套砝码)、纸带、复写纸、细
- 如图9-44,在一次实践活动中,小兵从A地出发,沿北偏东45°方向行进了5千米到达B地,然后再沿北偏西45°方向行进了5
- Parents are ________ to be invited to this year’s New Year
- 有学者指出:在(20世纪)五十年代兴起的经济全球化实际上只是“半球化”,只有到八九十年代经济全球化浪潮才真正具有全球性。
- It was because of bad weather _____ the football match had t
- 读甲、乙两地气温、降水量的月份分配图(图4-9),回答21~22题。21.甲种气候类型主要分布在( )A.回归线附近的
- 用NA表示阿伏加德罗常数的值,下列叙述中正确的是()A.1mol氯气参加氧化还原反应,转移的电子数一定为2NAB.在同温
- 成年男性的某一细胞处于减II后期时,正常情况下细胞中染色体的形态有 A.23种 B.24种
- . —__________ Mr.White was appointed director of our departm
- I _____ her not to walk on the thin ice but she would not li
- 对于化学反应,我们不但要考虑加入的试剂,还要考虑环境中的其他物质对化学反应的影响.教材中“木炭还原氧化铜”的实验(如图)
- (08年河南实验中学期中)某电路中电场随时间变化的图象如下图所示,能发射电磁波的电场是哪一种?
- 某电解池,如果在1s钟内共有5×1018个二价正离子和1.0×1019个一价负离子通过某截面,那么通过这个截面的电流是
- 结构简式为的有机物,不能发生的反应是 A. 消去反应 B. 加成反应 C.酯化
- 在一幅比例尺为l:500000的地图上,两点间距离为5厘米,则这两地间为 A.5千米 B



