第二单元 浩瀚的大气 知识点题库
-
(1) (实验回顾)图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置,写出红磷燃烧的符号表达式 。
-
(2) (实验过程1)甲组同学使用图1进行实验,步骤如下:
①检查装置的气密性
②加入药品,用弹簧夹夹紧橡皮管
③点燃燃烧匙内的红磷,立即伸入瓶中并塞紧塞子
④
⑤观察并记录水面的变化情况

-
(3) (问题提出)
①请将上述实验步骤填充完整。
②有资料表明,燃烧过程中当氧气体积分数小于7%时,红磷就无法燃烧,因此通过上述实验测量结果与理论值相比(填“偏高”或“偏低”)
-
(4) (实验改进1)
(查阅资料)铁生锈原理:铁和氧气、水反应生成红色物质(铁锈)。
Ⅰ.乙小组同学根据铁在空气中生锈的原理设计图2实验装置,再次测定空气中氧气的含量。(已知:装置中的食盐水和活性炭的作用是加速铁生锈)
Ⅱ.8分钟后测得的实验数据如表
实验前的体积
实验后的体积
集气瓶内空气
烧杯内蒸馏水
烧杯内剩余蒸馏水
131.0ml
90.0ml
63.6ml
(交流表达)①铁生锈是一个复杂过程,首先是铁与氧气、水反应生成氢氧化亚铁化学式:Fe(OH)2 , 写出该反应的符号表达式。
②根据表中数据计算,改进试验后测得的空气中氧气的体积分数是 (消耗的水的体积忽略不计,计算结果保留一位小数)
-
(5) (实验反思)与燃烧红磷法相比,乙小组方法测定空气中氧气含量的优点是。
-
(6) (实验再改进)在乙组实验的基础上,丙组同学设计了图3装置进行实验。实验前应先进行的操作是。

-
(7) (实验过程2)
步骤1:在注射器中装有足量铁粉、活性炭粉的浸有食盐水的纸袋,封闭。
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹。
步骤3:不断轻轻晃动注射器,当,计算得出氧气约占空气总体积的1/5
-
(1) 化学变化中的最小粒子是;
-
(2) 带正电荷的是;
-
(3) 不显电性的是;
-
(4) 质量最小的是;

-
(1) 在实验加热过程中,交替缓慢推动两个注射器活塞的目的是:。
-
(2) 写出该实验中反应的文字表达式:。
-
(3) 小强测得实验结果如下:
反应前注射器内气体总体积
反应后注射器内气体总体积
25m1
22m1
由此数据可以推算出他测定空气中氧气的体积分数(填<、>、=)造成该实验出现误差的原因可能是。(填序号)
①没有交替缓慢推动两个注射器活塞
②读数时没有冷却至室温
③加入铜丝量太少
④加入铜丝量太多
-
(1) 2个铝原子。
-
(2) 4个二氧化碳分子。
-
(3)
 表示的粒子符号。
表示的粒子符号。
-
(4) 标出二氧化硫中硫元素的化合价。
-
(5) KCl的名称是。
-
(1) (实验一)如图是教材中“测定空气中氧气体积分数”实验装置。
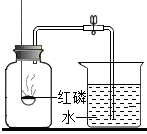
当集气瓶冷却至室温时,打开止水夹,可观察到的现象是。
-
(2) 实验也证明氮气的化学性质是。
-
(3) (实验二)如图是用蜡烛来代替红磷进行测定氧气体积分数实验。

蜡烛燃烧文字表达式为。
-
(4) 实验(填“可”或“否”)得出接近事实的结论,理由是。
-
(5) (实验三)“测定空气中氧气体积分数”成功的关键在于装置的密闭性和药品的合理选择。下图所示为兴趣小组同学对用“暖贴”实验可行性的探究方案。将装有过量铁粉的暖贴吊在集气瓶中,在装置的上方连接了氧气传感器,电脑实时读数,同时绘制出浓度变化曲线。
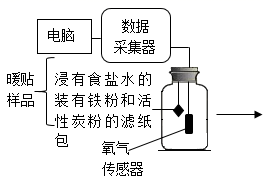
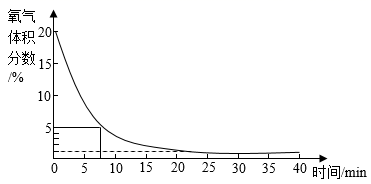
选择使用铁粉实验的理由是。
-
(6) 用食盐水浸滤纸包的目的是。
-
(7) 在实验过程中,氧气浓度变化的趋势为;反应前装置内氧气浓度为21.1%,35min时氧气浓度读数约为。
通过观察发现:若用铁粉实验时间会稍长,但消耗氧气更彻底,所得数据会更接近于事实。
-
(8) (拓展思维)
综上研究。请你另谈一点对教材上“空气中氧气含量测定”实验的具体改进意见是。
-
(1) 从宏观知微观。
①50mL水与50mL乙醇混合后,溶液体积小于100mL,微观解释为。
②气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是(填微粒符号)。
-
(2) 从微观知宏观
单质硫、硫化氢燃烧时会生成同种有毒的气体。请回答下列问题。
①如下图1是硫原子的结构示意图,其中x=,在化学反应中该原子容易(“得到”或“失去”)电子。
硫化氢在空气中燃烧的微观示意图如下图2:

②硫化氢中硫元素的化合价是。
③生成的有毒气体中各元素的质量比为。
④写出上述反应的文字表达式。
分析微观示意图。你能获得的信息有(各写一条即可):
⑤宏观方面:;
⑥微观方面:。

氢能
2022年3月23日,国家发展改革委公布该委与国家能源局联合印发的《氢能产业发展中长期规划(2021一2035年)》。《规划》明确了氢的能源属性,并阐述氢能产业的发展定位。氢能是未来国家能源体系的重点发展方向。在北京冬奥会上氢燃料汽车成为一抹亮色。
冬奥会举办期间,气温低至零下三十多摄氏度,给新能源汽车的启动、续航等提出更高要求。氢燃料电池汽车能更好地适应高海拔、低气温和山地起伏大的环境,能在零下三十多摄氏度环境中实现快速冷启动,真正实现“全气候运行”。我国自主研发的锂离子动力电池系统产品一一全气候动力电池,可以在极寒环境下提供强劲动能,为新能源汽车装上一颗抗冻“心脏”。
通过学习化学我们知道,氢分子通过燃烧与氧分子结合产生热能和水。氢燃料电池通过液态氢与空气中的氧结合而发电,根据此原理而制成的氢燃料电池可以发电用来推动汽车,提供家庭或工业用电或作为手机电池。
传统储氢方法:1。高压钢瓶(氢气瓶)储存法,但钢瓶储存氢气的容积小,而且还有爆炸的危险;2液态氢储存法,但液体储存箱非常庞大,且需要极好的绝热装置来隔热。新型储氢方法:储氢合金(金属氢化物)来储存氢气。如:镍氢电池,该电池具有容量大、安全无毒和使用寿命长等优点。
氢能作为一种清洁、高效、安全、可持续的能源,被视为21世纪最具发展潜力的清洁能源。
依据文中内容和所学知识,回答下列问题:
-
(1) 根据 Li 的原子结构示意图,写出锂离子的化学符号;

-
(2) 依次写出氢分子和氢离子的化学符号;
-
(3) 氢分子通过燃烧与氧分子结合产生热能和水,写出该反应的化学方程式;
-
(4) 用氢气瓶储氢的缺点是;
-
(5) 镍氢电池的优点是。

| 实验编号 | 催化剂 | 催化剂的质量(g) | 完全反应所需时间(s) |
| Ⅰ | MnO2 | 2.0 | 25.0 |
| Ⅱ | FeCl3 | 2.0 | 35.0 |
-
(1) 实验前需准备不同浓度的H2O2溶液。若要配制20g溶质质量分数为3.4%的H2O2溶液,需取溶质质量分数为20%的H2O2溶液g(精确到0.1)。
-
(2) 根据实验探究目的,从上表中的实验数据中,可得出结论是。
-
(3) 计算实验Ⅰ条件下H2O2完全分解所得氧气的质量,并写出具体计算过程。
-
(4) 在题图2中画出实验II过程中生成O2的曲线图。
-
(1) (一)常见气体的制取:

仪器a的名称是。
-
(2) 实验室用装置A制取O2 , 选用的白色药品是(填名称),该反应的化学方程式是;用装置C收集O2 , 气体应该从导管口(选填“b”或“c”)通入。
-
(3) 实验室用装置B制取CO2 , 若用仪器D取代仪器a后,装置的优点是。
-
(4) (二)对含有MgCl2的粗盐进行提纯,步骤如图:


步骤②中,玻璃棒的作用是。
-
(5) 步骤④中,滤纸上的滤渣除含有泥沙等杂质外还有(填化学式)。
-
(6) 步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是______(填字母)。A . 稀硫酸 B . 稀盐酸 C . 硫酸铜 D . 稀硝酸
-
(7) 步骤⑥中当时,停止加热。
-
(1) 氧化汞受热时的变化可用图表示(
 表示汞原子,
表示汞原子, 表示氧原子):
表示氧原子):

①由图可知分子和原子的本质区别为。
②物质汞是由构成的,氧气是由构成的。
-
(2) 如图表示氢气和氯气反应的示意图,试回答:

①在反应中,氢分子分裂成氢原子,氯分子分裂成氯原子,原子再相互结合成新的分子。
②氢气和氯气的化学性质不同的原因是
【查阅资料】I、某品牌茶垢清洁剂主要成分是过碳酸钠(Na2CO4),过碳酸钠溶于水时生成碳酸钠和过氧化氢。该茶垢剂的其他成分与水、与稀盐酸反应均不生成气体。
II、
-
(1) 【任务一】茶垢清洁剂溶于水产生的气体是什么?
【提出猜想】小林:该气体可能是CO2、O2、CO、H2、N2。
小明:不可能含有N2 , 因为。
小涵:不可能含有CO和H2 , 因为从药品安全角度考虑,H2易燃易爆,CO。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
-
(2) 【进行实验】取少量该茶垢清洁剂于试管中,向其中加入适量60~70℃的热水,塞上带导管的橡皮塞,将生成的气体通入澄清石灰水,发现澄清石灰水;打开橡皮塞,向其中伸入,观察到预期的现象,证实气体是O2。
-
(3) 【任务二】测定该茶垢剂中过碳酸钠的纯度。
根据资料Ⅱ学习小组设计并完成了如下图实验。

【讨论交流】小芳认为测定产物中O2的体积即可测定样品的纯度。
①装置③的作用是:。
②装置④中的水若有少量未装满(填“是”或“否”)影响测定O2的体积。
③小晨认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度。但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是。
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
④请你再设计一种新方案来测定该茶垢剂中过碳酸钠的纯度:。
- 推广使用节能灯对节能降耗意义重大。如果我国所有家庭都将白炽灯替换为节能灯,年节电总量接近三峡水库一年的发电量。由于节能灯
- 下列各组溶液中,用括号内的试剂及物质间相互反应不能鉴别的一组是A. Ba(OH)2 NaCl Mg(NO3)2 (FeC
- 下列离子中,所带电荷数与该离子的核外电子层数相等的是( ) A.Al3+ B.Mg2+
- 据说,天上有颗星星,名为北极星。由于北极星最靠近正北的方位,千百年来地球上的人们靠它的星光来导航。而我的心中也有一颗星,
- 下列词语中共有4个错别字,找出并改正在田字格里。(要求书写工整、规范、美观) (1)竣工 (2)急不瑕择
- 下列物质中既有离子键又有共价键的是 A.CaCl2 B. H2O C. K2O D. NaOH
- 某些植物根能分泌一些化学物质用于抑制别种植物在其周围生长,这称为他感作用。最近,科学家试图往大麦等农作物转入控制合成这些
- 生活中处处有化学。请根据你所学过的化学知识,判断下列说法中错误的是 A.医疗上常用体积分数为75%的酒精作消毒剂 B.
- 浙江省从20l0年4月1日起对全省最低月工资标准进行调整,其中最高一档的最低月工资标准提高至1 100元:实行最低工资标
- —Do you know when Phil's coming? —He ______ 4: 00. A.says
- 青少年遇到非正义的事情,既要勇敢,又要机智。下列做法中不可取的是A.设法稳住歹徒,记住歹徒的相貌,巧妙借助社会力量将歹徒
- 已知圆直线. (1)圆的圆心到直线的距离为? (2)圆上任意一点到直线的距离小于的概率为多少?
- Lifecomes in a package. This package includes happiness and
- 下列图象与对应选项关系合理的是()A. 稀释一定溶质质量分数的氢氧化钠溶液 B. 向一定溶质质量分数的盐酸中滴加氢氧化钠
- 阅读漫画 “被就业”。一系列用同样方法构成的新词“被××”在互联网上广为流行,中国网民借“被捐款”、“被代表”、“被小康
- 高等动物运动时,所需要的动力来自于( ) A.长骨 B.关节
- 小明学习了浮力知识以后,对热气球运动产生 了兴趣,他在网上收集了许多关于热气球的知识及类似图2所示的图片。以下是他对热气
- 分析说明题(2009年7月10日《人民日报》发表了《牢牢把握社会主义先进文化前进方向,着力提升国家中心城市文化软实力》的
- 设a=lg2+lg 5,b=ex(x<0),则a与b大小关系为(). A.a>b
- 下列句子中,没有语病的一项是 (



