第九单元 溶液 知识点题库
下图为四种物质的溶解度曲线,下列说法正确的是( )

A . 0℃时,在100g水中加入40g(NH4)2HPO4 , 搅拌,完全溶解,再增加1g该物质不能溶解。结论:溶质增加后溶解度降低
B . 30℃时,物质溶解度关系为①>②>③>④
C . 若NH4H2PO4中混有少量NaCl杂质,可在较高温度配成饱和溶液,再降温结晶
D . 要将接近饱和的Ce2(SO4)3溶液变成饱和溶液,操作措施有:加溶质或降温
A,B,C三种物质的溶解度曲线如图所示,请回答:

-
(1)

对于物质A而言,点P的含义为; -
(2) t3℃时,A,B,C三种饱和溶液中,溶质质量分数由大到小的排列为;
-
(3) 若A,B,C三种物质中有一种是易溶于水的气体,则其溶解度曲线是;
-
(4) 若A中混有少量的B,提纯A的方法是.
分析右图溶解度曲线,判断下列说法错误的是( )

A . t2℃时,硝酸钾的溶解度为110g
B . 硝酸钾中含有少量氯化钠时,可以用冷却热饱和溶液的方法提纯硝酸钾
C . 将t2℃时硝酸钾的饱和溶液降温到t1℃,一定会析出(110-a)g晶体
D . t2℃时,等质量的两种物质的饱和溶液中,含硝酸钾的质量一定比含氯化钠的质量大
向5个烧杯的液体中分别加入固体充分溶解,结果如下图所示。

-
(1) A溶液一定是(填“饱和”或“不饱和”)溶液。
-
(2) 能比较食盐和蔗糖溶解性强弱的是(填序号)。
-
(3) 对比C和D,得出的结论是。
在一次实验操作考查时,老师给出了三组考签:A 氧气的实验室制取和性质;B 二氧化碳的实验室制取和性质;C 配制50g15%的氯化钠溶液。每个同学抽取一个考签进行实验。
-
(1) 小桦同学抽签后来到实验室,发现本组实验桌上准备了下列仪器和药品:

①小桦同学抽到的考签应该是(填“A”“B”或“C”)组实验。
②该实验无须用到的仪器是(填仪器名称),制取该气体的化学方程式为。
-
(2) 小芬同学抽到的是“配制50g 15%的氯化钠溶液”的考签。通过计算,她需要称量NaCl的质量为g,量取水时,当加入量筒中的水的体积接近所需的体积时,应进行的下一步操作是。
理化知识与人类的生活、生产及发展息息相关。
-
(1) 防毒面具里滤毒罐中的活性炭具有作用。
-
(2) 用洗涤剂除去衣服上的油污,利用了洗涤剂的作用。
-
(3) 可利用氦气代替氢气充灌气球,其优点是。
-
(4) 农业上可用_____(选填序号)改良酸性土壤。A . 氢氧化钠 B . 熟石灰 C . 氯化钙
-
(5) 生活中可以降低水的硬度的方法是。
将12.5g石灰石(杂质不与酸反应也不溶于水),加入到装有100g稀盐酸的烧杯中。恰好完全反应后,烧杯中物质的总质量为108.1g。请计算。
-
(1) 生成二氧化碳的质量为g。
-
(2) 求稀盐酸中溶质的质量分数(写出计算过程)。
12gA物质完全溶解在36g水中,计算:
-
(1) 所得溶液中溶质的质量分数
-
(2) 该溶液能配制多少质量分数为10%的A溶液?
配制一定溶质质量分数的NaCl溶液时,会导致结果偏大的是( )
A . 向烧杯中转移氯化钠时有撒落
B . 用量筒量取水时俯视读数
C . 烧杯用水洗涤后未干燥就使用
D . 转移配好的溶液时有少量溅出
硝酸钾、氯化钾的溶解度曲线如图1所示。

-
(1) P点的含义是。
-
(2) 当温度 时,氯化钾的溶解度大于硝酸钾的溶解度。
-
(3) t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液的是,其溶液的溶质质量分数为(结果精确到0.1%)。
-
(4) 图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为 。
-
(5) 下列有关说法不正确的是 。A . ①与②的溶质质量可能相等 B . ②与③的溶质质量分数一定相等 C . 等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾 D . 等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
在化学实验技能考试做完“二氧化碳的制取和性质”实验后,废液桶中有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质)。为避免污染环境并回收利用废液,化学兴趣小组做了如下实验:
取废液桶上层清液共11.88kg,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液pH与加入的碳酸钠溶液的质量关系如图所示:
-
(1) 通过如图可知当碳酸钠溶液质量加到千克时,废液恰好处理完(盐酸与氯化钙的混合溶液完全转化成氯化钠溶液)。
-
(2) 求此时沉淀的质量(写出计算过程)。
-
(3) 此时所得溶液(填“能”或“不能)用于该校生物兴趣小组的小麦选种液。(选种液要求氯化钠的溶质质量分数在10%﹣20%之间)。

某化学小组需要用到质量分数为10%的氢氧化钠溶液来做实验,但实验室的氢氧化钠刚好用完。同学们提出用熟石灰与碳酸钠反应制取氢氧化钠,再配成溶液来做实验。
下表是氢氧化钙和氢氧化钠的溶解度数据
|
温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
|
溶解度 (g/100gH2O) |
氢氧化钙 |
0.19 |
0.17 |
0.14 |
0.12 |
0.09 |
0.08 |
|
氢氧化钠 |
31 |
90 |
111 |
129 |
313 |
336 |
|
请回答问题:
-
(1) 制备氢氧化钠。写出制取氢氧化钠反应的化学方程式。反应后过滤,蒸发结晶得到固体氢氧化钠。小明提出这样制得的氢氧化钠可能含有少量杂质,
其理由是。
-
(2) 提纯氢氧化钠。将上述制得的氢氧化钠(含少量氢氧化钙)在60℃时配成饱和溶液,降温、结晶、过滤,对滤渣和滤液成分的分析,正确的是________(双选)。A . 滤渣中只有氢氧化钠 B . 滤渣中主要是氢氧化钠,可能有少量氢氧化钙 C . 滤液中一定有氢氧化钙,可能有氢氧化钠 D . 滤液中一定有氢氧化钠和氢氧化钙 E . 滤液中只有氢氧化钙
-
(3) 配制氢氧化钠溶液。配制50克10%氢氧化钠溶液,需要氢氧化钠固体的质量为g,称取时必须将氢氧化钠固体放在里进行称量。
-
(4) 进行实验。完全中和40g上述配得的氢氧化钠溶液,用去了稀硫酸的质量为20克,则稀硫酸的质量分数为(精确到0.1%)
下列图像分别对应四个变化过程,能正确反应对应变化关系的是( )
A .  是向等质量的氧化锌和氢氧化锌中分别加入相同浓度的稀盐酸至过量
B .
是向等质量的氧化锌和氢氧化锌中分别加入相同浓度的稀盐酸至过量
B .  是用氯酸钾和二氧化锰混合加热制取氧气
C .
是用氯酸钾和二氧化锰混合加热制取氧气
C .  是气体物质的溶解度与温度和压强的关系
D .
是气体物质的溶解度与温度和压强的关系
D .  是在恒温条件下,将饱和氯化钠溶液蒸发适量水
是在恒温条件下,将饱和氯化钠溶液蒸发适量水
 是向等质量的氧化锌和氢氧化锌中分别加入相同浓度的稀盐酸至过量
B .
是向等质量的氧化锌和氢氧化锌中分别加入相同浓度的稀盐酸至过量
B .  是用氯酸钾和二氧化锰混合加热制取氧气
C .
是用氯酸钾和二氧化锰混合加热制取氧气
C .  是气体物质的溶解度与温度和压强的关系
D .
是气体物质的溶解度与温度和压强的关系
D .  是在恒温条件下,将饱和氯化钠溶液蒸发适量水
是在恒温条件下,将饱和氯化钠溶液蒸发适量水
20℃时,将18.5g硝酸钠放入50g中,充分搅拌后全部溶解,则20℃时硝酸钠的溶解度为(单位g/100g水)( )
A . 37.0
B . 18.5
C . 9.25
D . 无法计算
如图是A、B两种固体物质的溶解度曲线。

-
(1) t1℃时,A、B的饱和溶液中溶质的质量分数相等的原因是。
-
(2) t2℃时,60gA溶于100g水中,所得溶液(填“是”或“不是”)饱和溶液,溶液的质量g。该温度下要配制溶质质量分数相等的A、B溶液,(填“A”或“B")溶液一定是不饱和溶液。
-
(3) 分别将A、B的饱和溶液从t2℃降低温度至t1℃,有晶体析出的是溶液。
某同学取110g K2CO3溶液于烧杯中,向其中加入CaCl2溶液。反应过程中加入CaCl2溶液与生成沉淀的质量关系如图所示。

请计算:
-
(1) m的值是。
-
(2) 恰好完全反应时,所得溶液的溶质质量分数是多少?(写出计算过程,结果精确到0.01%)。
甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是( )
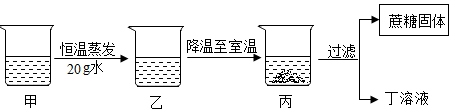
A . 甲一定是不饱和溶液
B . 丙和丁一定是饱和溶液
C . 乙的溶质质量分数一定比甲大
D . 甲和丙的溶质质量分数一定不相等
如图是甲、乙两种物质的溶解度曲线。

-
(1) M点的含义。
-
(2) 甲中混有少量乙,提纯甲的方法是。
-
(3) 将接近饱和的乙溶液变成饱和溶液可采用(填“升温”或“降温”)的方法。
-
(4) 等质量甲、乙物质分别配成t2℃时的饱和溶液,所需溶剂质量最多的是。
-
(5) N点是甲的不饱和溶液,若想使其变成M点的饱和溶液,方法是。
在t℃时,分别取甲、乙两种固体的溶液,恒温蒸发水分,得到蒸发水的质量(X)与析出晶体质量(Y)的关系如图所示(析出的晶体不含结晶水)。

-
(1) t℃时,在0点乙的溶液是(填“饱和”或“不饱和”)溶液。
-
(2) t℃时,甲、乙的溶解度大小关系为甲(填“<”“>”或 “=”)乙。
-
(3) 用析出的甲配制一定溶质质量分数的溶液时,若所配制溶液溶质的质量分数偏大,则可能是量取水时(填“俯视”或“仰视”)量筒读数所致。
放入水中能形成溶液的是( )
A . 麻油
B . 蔗糖
C . 淀粉
D . 牛奶
最近更新
- 完形填空 ,阅读下列短文,从每小题所给的A、B、C、D四个选项中选出一个最佳选项。 A rich man loved h
- “画饼充饥”、“望梅止渴”共同说明了 A.意识活动依赖于人体的生理过程 B.意识对于人体的生理活动
- 2.下列各句中,没有语病的一句是( )A.近年来,通过北京国际图书博览会、东京国际书展、首尔国际图书展等平台,使中国
- 已知抛物线的焦点与双曲线的右焦点重合,抛物线的准线与轴的交点为,点在抛物线上且,则的面积为 ( )
- 在城市规划、设计时,在利用气候资源方面主要考虑的是 A.日光和降水B.降水和风向C.日光和风向D.风向和云量
- 图中小推车靠着墙,请根据力的作用效果,用平行四边形定则画出小推车所受重力的两个分力:
- 钟表8时30分时,时针与分针所成的角的度数为 ( ) (A)30° (B)60° (
- 一次实验课上,细心的小红,小敏同学同时发现盛有NaOH溶液的试剂瓶塞外有少量白色粉末. 【提出问题】白色粉末是什么呢?
- 海葵附着在蟹壳上生活,借助蟹得以快速转移并得到氧气和食物,而蟹借附着在身上的海葵掩护自己。它们之间这种互惠互利的关系属于
- 已知棱长为1的正方体ABCD A1B1C1D1中,E是A1B1的中点,则直线AE与平面ABC1D1所成角的正弦值为__
- 如图甲左侧的调压装置可视为理想变压器,负载电路中 R= 55 Ω,为理想电流表和电压表。若原线圈接入如图乙所示的正弦交变
- 以下为一些同学用调节好的天平测量牛奶密度实验中的一些步骤:①测出空烧杯的质量m1;②向烧杯中倒入一些牛奶,测出烧杯和牛奶
- 回旋加速器是加速带电粒子的装置,其核心部分是分别与高频交流电极相连接的两个D形金属盒,两盒间的狭缝中形成周期性变化的电场
- 用“/”给下列文段断句。 异 史 氏 日 贫 而 好 客 饮 博 浮 荡 者 优 为 之 异 者 独 其 妻 耳 受 之
- 利用自制多硫化钠可测定空气中氧气含量。实验步骤如下:① 取 1gNaOH 固体和 1g 硫磺粉末充分研磨后加热,可制得多
- 某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含
- 心不厌细:《舌尖上的中国》为什么这样红 杨葵 ①一部纪录片红成这样,出乎很多人意料,包括总导演陈晓卿,他反复在公开或私下
- 20世纪20年代初,苏俄农民喊出了“打倒列宁和马肉,恢复沙皇统治和猪肉”的口号,对此理解正确的是
- 红星中学高一(2)班将召开“畅想奥运”的主题班会。下面是主持人开场白的开头和结尾,请你补出中间部分。要求紧扣主题、言简意
- 近年来,国际形势风云激荡、丰富多彩,地区热点问题不断,恐怖主义时常发动袭击,伊、朝核问题依然牵动大国关系和世界安全神经。



