高考二轮复习知识点:铁及其化合物的性质实验
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 实验探究题 | 详细信息 |
|
某小组同学在实验室中研究+2和+3价铁的硝酸盐的化学性质.
|
|
| 2. 综合题 | 详细信息 | |||||||||||||||||||||
|
用零价铁(Fe)去除水体中的硝酸盐(NO3﹣)已成为环境修复研究的热点之一.
|
||||||||||||||||||||||
| 3. 综合题 | 详细信息 |
|
某班同学用如下实验探究Fe2+、Fe3+的性质.回答下列问题:
|
|
| 4. 综合题 | 详细信息 |
|
如图所示装置工作时均与H2有关.
|
|
| 5. 单选题 | 详细信息 |
|
铁及其化合物与生产生活密切相关。下列说法错误的是( )
A . 可用铁制槽车装运浓H2SO4
B . 不锈钢就是铁碳合金
C . FeCl3可以用作净水剂
D . 铁可用于制作磁性材料
|
|
| 6. 单选题 | 详细信息 |
|
亚硝酸亚铁Fe(NO2)2易分解,若分解产物之一是红色粉末Fe2O3 , 则另一分解产物可能是( )
A . NO
B . N2O3
C . NO2
D . N2O5
|
|
| 7. 单选题 | 详细信息 |
|
如图所示,硫酸铁与M、N、P、Q反应产生不同的现象。则各符号对应的试剂错误的是( )
A . M:硫氰化钾溶液
B . N:铁粉
C . P:氢氧化钡溶液
D . Q:氨水
|
|
| 8. 单选题 | 详细信息 |
|
研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是( )
A . 反应总过程是放热的
B . Fe+作为催化剂改变了反应途径,提高了反应速率
C . Fe++N2O→FeO++N2、FeO++CO→Fe++CO2 两步反应均为放热反应
D . 若反应在恒容密闭容器中进行,温度越高,反应速率一定越快
|
|
| 9. 实验探究题 | 详细信息 | |||||||||||||||
|
硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]是一种稳定的还原剂,常用作分析化学中的滴定剂。某课题组采用下列方案制备该晶体,并对其热稳定性进行了如下实验。
|
||||||||||||||||
| 10. 综合题 | 详细信息 |
|
草酸亚铁晶体(
 )常用于晒制蓝图。某研究性学习小组对其进行了系列探究。 )常用于晒制蓝图。某研究性学习小组对其进行了系列探究。
|
|
- 2016-2017学年福建省莆田二十五中高三上学期期中化学试卷
- 高中必修一化学结业考试模拟题
- 广东省汕头市金山中学2019-2020学年高三下学期化学6月理综试卷
- 人教版化学高二选修6第一单元实验1-2氯气的生成及其性质的微型实验实验同步练习
- 黑龙江省宾县第一中学2019-2020学年高二下学期化学期末考试试卷
- 2016-2017学年江苏省徐州市高二上学期期末化学试卷(必修)
- 2015-2016学年浙江省金华市东阳二中高一上学期第一次调研化学试卷
- 人教版化学高二选修1第三章第一节合金同步练习
- 江西省鹰潭市2018-2019学年高二上学期化学期末考试试卷
- 2017年高考化学押题预测卷 (新课标Ⅲ卷)
- 广西钦州市2019-2020学年高一下学期化学期末考试试卷(理)
- 2018-2019学年高一上学期12月月考 化学试题
- 概括下面两段文字的主要内容,不超过33个字。(3分) 传世画作《蒙娜丽莎》的原型一直是个谜,现在多数学者认为她是佛
- 下列叙述错误的是 A.13C和14C属于同一种元素,它们互为同位素 B.1H和2H是不同的核素,它们的质子数相等 C.1
- 下列有关文学常识的表述,有错误的一项是 ( ) A.《诗经》是我国最早的一部诗歌总集,收录了从西周初年至春
- 我国宪法规定:“中华人民共和国公民对于任何国家机关和国家工作人员,有提出批评和建议的权利” 。 回答下列问题: (1)宪
- 有氧呼吸过程中的CO2产生于( ) A.丙酮酸分解时 B.葡萄糖刚要分解时 C
- 下图是探究酵母菌呼吸作用方式的实验装置。以下说法中不正确的是A.装置一中NaOH的作用是吸收CO2 B.提取装置二中d瓶
- 在古代有一个人,他不出国,就能游览整个地中海沿岸各地的风光。你认为他生活在下列哪一个国家?( ) A.罗马共和国
- 阅读下面的材料,完成后面题目。 无论怎样成功的艺术家,必有他的短处。泰戈尔也逃不出这条公例。 哲理本不宜入诗,哲理诗之
- 进行一氯取代反应后,只能生成三种沸点不同的产物的烷烃是--------------------------( )
- [矩阵变换] 求圆C:在矩阵对应变换作用下的曲线方程,并判断曲线的类型.
- 下列关于转基因植物的叙述。正确的是 A.转入到油菜的抗除草剂基因,可能通过花粉传人环境中 B.转抗虫基因的植物.不会导致
- .西方某历史学家认为:历史学家要当地理学家,也要当法学家,还有社会学家与心理学家。这个观点反映的是
- 已知则的值为 .
- 图4是“世界主要石油运输路线图”,读图回答14—15题。图4 14、目前石油储量、生产量最大,输出石油最多的地区是A.
- 某学生用0.1 mol/L的KOH标准溶液滴定未知浓度盐酸,其操作分解为如下几步:A.移取20 mL待测盐酸溶液注入洁净
- 下列几种动物中,生殖方式与人类最接近的是 ( ) A.鲫鱼 B.白鳍豚 C.龟 D.青蛙
- 国际上有一条公认的企业法则“马特莱法则”(又称二八法则):告诉企业的经营者不应该面面俱到,而应侧重抓关键的人、关键的环节
- 如图,⊙O中,弦BA,DC的延长线交于点P,AD,BC相交于点E,则图中相似三角形共有 。
- 观察下列图片,回答问题 (10分) 图一
- 下图表示山谷的是 ( )






 FeSO4溶液
FeSO4溶液  结晶
结晶  硫酸亚铁铵晶体
硫酸亚铁铵晶体

 尾气处理装置。
尾气处理装置。 ,其目的是。
,其目的是。 ,依据的实验现象为。
,依据的实验现象为。 受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,
受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时, 
 溶液为显色剂,写出
溶液为显色剂,写出  与
与  杂质测定其纯度的步骤如下:
杂质测定其纯度的步骤如下: 草酸亚铁晶体样品溶于稀
草酸亚铁晶体样品溶于稀 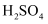 中,配成
中,配成  溶液;
溶液; ,用
,用  ,标准液滴定至终点消耗标准液
,标准液滴定至终点消耗标准液  ;
; 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 



