高考二轮复习知识点:电解池工作原理及应用2
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 实验探究题 | 详细信息 |
|
CO2的资源化利用能有效减少CO2排放,充分利用碳资源。
|
|
| 2. 单选题 | 详细信息 |
|
采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图所示。忽略温度变化的影响,下列说法错误的是( )
A . 阳极反应为
 B . 电解一段时间后,阳极室的pH未变
C . 电解过程中,H+由a极区向b极区迁移
D . 电解一段时间后,a极生成的O2与b极反应的O2等量
B . 电解一段时间后,阳极室的pH未变
C . 电解过程中,H+由a极区向b极区迁移
D . 电解一段时间后,a极生成的O2与b极反应的O2等量
|
|
| 3. 多选题 | 详细信息 |
|
双极膜(BP)是阴、阳复合膜,在直流电作用下,阴、阳膜复合层间的H2O解离成H+和OH-。利用双极膜电渗析法和惰性电极电解食盐水可获得淡水、NaOH溶液和盐酸,其工作原理如下图所示,M、N为离子交换膜。下列说法错误的是( )
A . M膜为阴离子交换膜
B . 出口2的产物是盐酸
C . 若去掉双极膜(BP),阳极室会有Cl2生成
D . 电路中每转移1 mol电子,两极共得到0.5 mol气体
|
|
| 4. 多选题 | 详细信息 |
|
硼酸(H3BO3或B(OH)3)是一元弱酸,常用于医药玻璃等工业,并用作食物防腐剂和消毒剂,工业上通过电解法制备硼酸。其工作原理如图所示,下列说法正确的是( )
A . Pt(I)为阴极,电解一段时间后,该极区pH减小
B . 产品室发生的反应为B(OH)
 +H+=H3BO3+H2O
C . Pt(I)极区加入氢氧化钠是为了增强溶液的导电性
D . 膜x是阴离子交换膜 +H+=H3BO3+H2O
C . Pt(I)极区加入氢氧化钠是为了增强溶液的导电性
D . 膜x是阴离子交换膜
|
|
| 5. 多选题 | 详细信息 |
|
我国科学家利用N2掺杂多孔碳(NHPC)制成的催化剂实现了电解苯酚(
下列说法正确的是( )
A . NiP/NHPC极为阴极
B . 通电时,H+向FeRu/NHPC极迁移
C . 阴极反应式为
|
|
| 6. 多选题 | 详细信息 |
|
电致变色玻璃以其优异的性能将成为市场的新宠,如图所示五层膜的玻璃电致变色系统其工作原理是在外接电源下,通过在膜材料内部发生氧化还原反应,实现对器件的光透过率进行多级可逆性调节。(已知: WO3和Li4Fe4[Fe(CN)6]3均为无色透明,LiWO3和Fe4[Fe(CN)6]3均为蓝色)
下列有关说法正确的是( )
A . 当A接电源的负极时,发生的电极反应为: WO3+Li++e-=LiWO3
B . 当A接电源正极时,透射率增强,不能有效阳拦阳光
C . 当B接电源正极时,Fe4[Fe(CN)6]3 转化为Li4Fe4[Fe(CN)6]
D . 当B接电源负极时,膜由无色变为蓝色
|
|
| 7. 综合题 | 详细信息 | ||||||||||||||||||||
|
为证明AgCl溶于水存在溶解平衡,取1 mo/LKCl溶液10 mL,向其中加入0.2 mol/LAgNO3溶液1 mL,充分反应后将浊液过滤进行如下实验:
已知:①AgOH不稳定,立即分解为Ag2O (棕褐色或棕黑色),Ag粉为黑色; ②AgCl、Ag2O可溶于浓氨水生成 [Ag(NH3)2]+(银氨溶液),Mg、Ag不溶于浓氨水。
|
|||||||||||||||||||||
| 8. 综合题 | 详细信息 |
|
氨气是重要的化工原料,广泛应用于化工、轻工、制药、合成纤维等领城。
|
|
| 9. 综合题 | 详细信息 |
|
丙烯
 是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,副产物有乙腈 是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,副产物有乙腈  、氢氰酸、丙烯醛 、氢氰酸、丙烯醛  等,以丙烯、氨气和氧气为原料,在催化剂存在下合成丙烯腈 等,以丙烯、氨气和氧气为原料,在催化剂存在下合成丙烯腈  的主要反应如下: 的主要反应如下: Ⅰ. Ⅱ. 回答下列问题:
|
|
| 10. 综合题 | 详细信息 |
|
接触法制硫酸生产中的关键工序是
 的催化氧化( 的催化氧化(   )。回答下列问题: )。回答下列问题:
|
|
- 2016年江西省宜春市万载二中高考化学四模试卷
- 2016-2017学年浙江省温州市十校联合体高二上学期期中化学试
- 人教版化学高二选修4第三章第一节弱电解质的电离同步练习
- 广西钦州市2019-2020学年高二下学期化学期末考试试卷
- 2015-2016学年江西省南昌市高一下学期期中化学试卷
- 上海市华东师大二附中2016-2017学年高二上学期化学期末考试试卷
- 备考2018年高考化学一轮基础复习:专题20 化学反应速率
- 人教高中化学一轮复习:专题16物质结构与性质
- 湖北省荆门市2016-2017学年高二下学期化学期末考试试卷
- 2015-2016学年吉林省吉林五十五中高一下学期期中化学试卷(理科)
- 2016-2017学年山东省临沂市高一上学期期中化学试卷
- 2015-2016学年陕西省汉中中学高一上学期期中化学试卷
- 已知几种离子的结构,带电情况及其化合价如下表所示。通过此表除总结出“带电荷的原子属于离子”外还能得出以下结论: (1)
- 如图所示:甲瓶中盛放的是浓硫酸(吸收水蒸汽)乙瓶中放的是用石蕊溶液染成紫色的干燥小花。若关闭阀门Ⅰ,打开阀门Ⅱ,紫色小花
- 已知次氯酸是比碳酸还弱的酸,反应Cl2+H2OHCl+HClO达到平衡后,要使HClO浓度增大,可加入() A.Na
- 13.在显微镜下观察某植物根尖细胞有丝分裂时,其正确的操作方法是 ( ) A.应该从该植物根尖分生区获取
- 18.补写出下列名篇名句中的空缺部分。(6分) (1)师者, 。
- (本题满分14分) 已知函数,不等式对恒成立,数列满足:, , 数列满足:; (Ⅰ)求的值; (Ⅱ)设数列的前和为,前的
- 依据下列材料,回答问题。 材料一 昆明准静止锋又称云贵准静止锋,位于云贵高原,锋面徘徊于昆明和贵阳之间,易形成连阴雨天气
- 下列关于生态系统的叙述中,错误的是 A.生态系统的结构由生产者、消费者和分解者三种成分组成 B.生态系统中的
- 弦乐队在演奏前,演奏员都要调节自己的乐器—拧紧或放松琴弦,这样做主要是改变乐器发出声音的( ) A.响度
- 一次数学测试,某小组五名同学的成绩如下表所示(有两个数据被遮盖).组员日期 甲 乙 丙 丁 戊 方差 平均成绩 得分 8
- 不能用来鉴别CO和CO2两种气体的方法是A.通入澄清石灰水 B.观察颜色C.通入紫色石蕊试液
- 下列变化中,既有共价键和离子键断裂,又有共价键和离子键形成的是 ( ) A.2Na+2H2O=2NaOH
- 联合国总部设在( ) A、纽约 B、华盛顿 C、布鲁塞尔 D、日内瓦
- 下面有关晶体的叙述中,不正确的是 ( ) A.金刚石空间网状结构中,由共价键形成的碳原子环中,最小环
- 5.某种遗传病受一对等位基因控制,下图为该遗传病的系谱图。下列叙述正确的是()A.若该病为伴X染色体隐性遗传病,Ⅱ1为纯
- 一直升机停在南半球的地磁极上空,该处地磁场叶片的长度为l,螺旋桨转动的频率为f,顺着地磁场的方向看螺旋桨,螺旋桨按顺时针
- 在反应X+2Y====R+2M中,已知R和M的摩尔质量之比为22∶9,当1.6 g X与Y完全反应后,生成4.4 g R
- The teacher asked us __________ so much noise. A.don’t make
- 在容量瓶的使用方法中,下列操作正确的是 A.使用容量瓶前检查是否漏水B.容量瓶用蒸馏水洗净后,再用待配溶液润洗C.配制溶
- 斯塔夫里阿诺斯在《全球通史》中说:“(雅典)最初是实行君主政体,以后让位于由九个执政官主持的寡头政治。这九个执政官是主



 ×100%
×100%







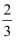 pkPa。则10min内N2的反应速率v(N2)=kPa/min。T时,该反应的平衡常数Kp=(列出含p的计算式即可;分压=总压×物质的量分数)。
pkPa。则10min内N2的反应速率v(N2)=kPa/min。T时,该反应的平衡常数Kp=(列出含p的计算式即可;分压=总压×物质的量分数)。







 。
。
 ,其标准平衡常数:
,其标准平衡常数:  。T℃,压强为
。T℃,压强为  的恒压密闭容器中,通入1mol丙烯、1mol氨气和3mol氧气发生反应Ⅰ、Ⅱ,达到平衡时,容器内有amol
的恒压密闭容器中,通入1mol丙烯、1mol氨气和3mol氧气发生反应Ⅰ、Ⅱ,达到平衡时,容器内有amol  ,b mol
,b mol  ,此时
,此时  的分压
的分压  (分压=总压×物质的量分数,用含a,b的代数式表示,下同);反应Ⅱ的标准平衡常数为。
(分压=总压×物质的量分数,用含a,b的代数式表示,下同);反应Ⅱ的标准平衡常数为。
 可减少氮氧化物的排放,其装置如图所示,电解时Pb电极发生的电极反应式为。
可减少氮氧化物的排放,其装置如图所示,电解时Pb电极发生的电极反应式为。 
 表面反应生成
表面反应生成  的历程:
的历程: 



 反应合成
反应合成 
 、
、  和
和  ,起始时压强为p,进行反应
,起始时压强为p,进行反应  。平衡时,
。平衡时,  (以分压代替浓度计算,分压=总压×物质的量分数)。
(以分压代替浓度计算,分压=总压×物质的量分数)。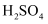 ,其工作原理如图所示,
,其工作原理如图所示, 
 和
和  ,当甲电极消耗
,当甲电极消耗  时,甲、乙两室中
时,甲、乙两室中 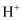 与
与  的总物质的量之比为。(两电极的产物均留在溶液中,忽略水的电离)
的总物质的量之比为。(两电极的产物均留在溶液中,忽略水的电离)


