高考二轮复习知识点:化学反应中能量的转化3
高考二轮复习知识点:化学反应中能量的转化3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 |
|
1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正离子(
A . 1,4-加成产物比1,2-加成产物稳定
B . 与0℃相比,40℃时1,3-丁二烯的转化率增大
C . 从0℃升至40℃,1,2-加成正反应速率增大,1,4-加成正反应速率减小
D . 从0℃升至40℃,1,2-加成正反应速率的增大程度小于其逆反应速率的增大程度
|
|
| 2. 单选题 | 详细信息 |
|
“天问一号”着陆火星,“嫦娥五号”采回月壤。腾飞中国离不开化学,长征系列运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法正确的是( )
A . 煤油是可再生能源
B .
 燃烧过程中热能转化为化学能
C . 火星陨石中的 燃烧过程中热能转化为化学能
C . 火星陨石中的  质量数为20
D . 月壤中的 质量数为20
D . 月壤中的  与地球上的 与地球上的  互为同位素 互为同位素
|
|
| 3. 多选题 | 详细信息 |
|
HCOOH在Pd催化剂表面脱氢的反应机理、反应历程与能量的关系如图所示:
下列说法正确的是( )
A . 在Pd催化剂表面HCOOH脱氢反应的
 H >0
B . 在Pd催化剂表面离解O-H键比C-H键的活化能低
C . 在历程Ⅰ~Ⅴ中,生成Ⅴ的反应速率最慢
D . 用DCOOH或HCOOD代替HCOOH,得到的产物都有HD和CO2 H >0
B . 在Pd催化剂表面离解O-H键比C-H键的活化能低
C . 在历程Ⅰ~Ⅴ中,生成Ⅴ的反应速率最慢
D . 用DCOOH或HCOOD代替HCOOH,得到的产物都有HD和CO2
|
|
| 4. 多选题 | 详细信息 |
|
中国科学院化学研究所报道了化合物1催化CO2氢化机理。其机理中化合物1(催化剂,固态)→化合物2(中间产物,固态)的过程和其相对能量曲线如下图所示。下列说法错误的是( )
A . 化合物1与CO2反应生成化合物2的过程中有两个过渡态TS11-2、TS21-2 , 说明这一过程包含两个基元反应
B . 图中Ⅰ1-2与化合物2互为同分异构体
C . 过程①的活化能高于过程②的活化能
D . 过程①的热化学方程式为:I(s)+CO2(g)=I1-2 (s) △H=2.08 kJ·mol-1
|
|
| 5. 多选题 | 详细信息 |
|
我国已进入新发展阶段,积极推进碳达峰、碳中和,有利于推动低碳技术、低碳经济的快速发展。CO2再利用的常见的两种反应原理如下:
反应①: 反应②: 下列有关说法正确的是( )
A . 植树造林对“碳中和”目标的实现有积极作用
B . 反应①的能量转化形式:化学能
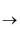 光能
C . 反应②得到的甲醇是重要的化工原料,可用于生产甲酸甲酯
D . 处理等物质的量的CO2时,反应①和反应②中转移的电子数相同 光能
C . 反应②得到的甲醇是重要的化工原料,可用于生产甲酸甲酯
D . 处理等物质的量的CO2时,反应①和反应②中转移的电子数相同
|
|
| 6. 单选题 | 详细信息 |
|
元末陶宗仪《辍耕录》中记载:“杭人削松木为小片,其薄为纸,熔硫磺涂木片顶端分许,名日发烛……,盖以发火及代灯烛用也。”下列有关说法错误的是( )
A . 将松木削薄为纸片状有助于发火和燃烧
B . “发烛”发火和燃烧利用了物质的可燃性
C . “发烛”发火和燃烧伴随不同形式的能量转化
D . 硫磺是“发烛”发火和燃烧反应的催化剂
|
|
| 7. 综合题 | 详细信息 |
|
碳及其化合物间的转化广泛存在于自然界及人类的生产和生活中。已知25℃,
 时: 时: ① ② 回答问题:
|
|
| 8. 综合题 | 详细信息 | ||||||||||||||||||
|
近日IPCC发布了由来自40个国家的91位科学家编写的《全球升温1.5℃特别报告》,报告表明:温室效应引发的环境问题日益严重,CO2的减排和综合利用是解决温室效应及能源问题的有效途径,将CO2转化成有机物可有效实现碳循环。在容积为2L的恒温恒容密闭容器中,充入3molCO2和9molH2 , 一定条件下发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的物质的量随时间变化情况如表所示,并根据数据绘制图像如图(已知相同条件下气体的压强之比等于物质的量之比): CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的物质的量随时间变化情况如表所示,并根据数据绘制图像如图(已知相同条件下气体的压强之比等于物质的量之比):
回答下列问题:
|
|||||||||||||||||||
| 9. 综合题 | 详细信息 |
|
填空。
|
|
| 10. 单选题 | 详细信息 |
|
丙酮是最简单的脂肪酮,人们把它作为模型进行了大量的光化学反应研究。丙酮分子中存在如图1所示4种类型的化学键,即C=O、
 、 、 、 、 , 丙酮在激光强度为 , 丙酮在激光强度为 时,在特定的时间间隔内这4种类型的化学键的键长变化如图2所示。 时,在特定的时间间隔内这4种类型的化学键的键长变化如图2所示。
下列判断错误的是( )
A . I表示C-C键,在该条件下最易断裂
B . 丙酮在该条件下的光解反应是吸热反应
C . 丙酮在该条件下解离的第一步反应可表示为
 D . 丙酮在该条件下的光解反应中只有化学键的断裂
D . 丙酮在该条件下的光解反应中只有化学键的断裂
|
|
高中化学 试卷推荐
- 浙江省诸暨市2021-2022学年高二上学期期末考试化学试题
- 云南省玉溪市2020-2021学年高二上学期期末教学质量检测化学试题
- 江苏省徐州市睢宁县2021-2022学年高一下学期期中考试(线上)化学试题
- 湖北省黄冈市2020-2021学年高二下学期化学期末考试试卷
- 广西百色中学2021-2022学年高二上学期化学第一次月考试卷
- 浙江省舟山市2022届高三下学期第三次模拟化学试题
- 北京市石景山区2020-2021学年高二上学期期末调研化学试题
- 广东省汕头市潮南区2020-2021学年高一上学期化学第二次月考试卷
- 浙江省浙北G2联合体2021-2022学年高一上学期化学期中联考试题
- 北京市朝阳区2022届高三一模考试化学试题
- 黑龙江省肇东市第四中学校2020-2021学年高一上学期化学期中考试试卷
- 新疆昌吉教育共同体2020-2021学年高一下学期化学期中考试试卷
最近更新
- It is said that Nigeria is _______ Great Britain.A. three t
- 财政教育经费投入不足,是长期以来制约我国教育事业发展的一个重要因素。面对这一问题,假如你是人大代表,可以 A.行使立法权
- 解......
- 如图1,在平面直角坐标系中,以坐标原点O为圆心的⊙O的半径为,直线:与坐标轴分别交于A、C两点,点B的坐标为(-4,1)
- “Would you like tea _____ coffee?” “_____, thanks.”A. or, No
- 用下列实验装置进行相应实验,能达到实验目的是①用图1所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒 ②用图2所示
- 已知α、β都是锐角,且sinα=,sinβ=,则α+β=_______________.
- 科学发展观,是对党的三代中央领导集体关于发展的重要思想的继承和发展,既一脉相承又与时俱进。这说明 ( )
- By the time this letter reaches you, I ___ for Paris for fur
- People always feel headache about academic writing.Jennifer
- 我国的语言文字丰富多彩,其中有许多语句蕴含了物理知识。请在下表中填写所列语句涉及到的物理知识。序号 语句 物理知识 示例
- 已知命题方程的两实数根的符号相反;命题,使,若命题“”是假命题,则实数的取值范围是______.
- ......
- 下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是( )① 过滤 ② 蒸发 ③ 溶解
- (07年高考江苏卷・14)有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中
- 现有由氧化铁和铝组成的铝热剂,某实验小组分别进行如下实验:(1)取a g样品,向其中加人足量的NaOH溶液,测得生成气体
- 有人指出,中国政府非常稳定,政策非常持续,没有被竞选左右的思维模式。西方的 问题就是由于竞选导致各个党派互相竞争。这肯定
- 两圆的圆心距,它们的半径分别是一元二次方程的两个根,这两圆的位置关系是A.外离
- 用下图表示的一些物质或概念间的从属关系中,正确的是:
- 15.





 葡萄糖
葡萄糖  完全燃烧生成
完全燃烧生成  和
和  ,放出
,放出  热量。
热量。
 。
。 的热化学方程式为。
的热化学方程式为。
 、
、  键的键焓分别为
键的键焓分别为  、
、  ,
,  。
。
 只有部分转化为
只有部分转化为  ,大部分以水合
,大部分以水合  表示。已知25℃时,
表示。已知25℃时,  的平衡常数
的平衡常数  ,正反应的速率可表示为
,正反应的速率可表示为  ,逆反应的速率可表示为
,逆反应的速率可表示为  ,则
,则  (用含
(用含  的代数式表示)。
的代数式表示)。
 ,其平衡常数
,其平衡常数  。[已知
。[已知  ,
,  ]
]


 +6H2O
+6H2O 晶体与
晶体与 混合搅拌 ④碳酸钙分解
混合搅拌 ④碳酸钙分解 在
在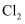 中燃烧 ⑥灼热的碳与
中燃烧 ⑥灼热的碳与 的反应
的反应
 设计成的原电池如图所示。
设计成的原电池如图所示。





