高考二轮复习知识点:物质的分离与提纯5
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||
|
碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,并测定产品中少量碳酸氢钠的含量,过程如下:
步骤I. ①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中; ②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 ③在上述锥形瓶中再加入2滴指示剂N,继续用 ④平行测定三次, 已知:(i)当温度超过35℃时, (ii)相关盐在不同温度下的溶解度表
回答下列问题:
|
|||||||||||||||||||||||||||||||||||||||||
| 2. 综合题 | 详细信息 |
 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以  形式存在,还含有 形式存在,还含有  、 、  、 、  、 、  等物质。以独居石为原料制备 等物质。以独居石为原料制备  的工艺流程如下: 的工艺流程如下: 回答下列问题:
|
|
| 3. 实验探究题 | 详细信息 |
|
胆矾(
 )易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的 )易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的  (杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题: (杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
|
|
| 4. 单选题 | 详细信息 |
|
我国古代《演繁露》记载:“盐已成卤水,暴烈日,即成方印,洁白可爱,初小渐大或数十印累累相连”,其中涉及的分离方法是( )
A . 升华
B . 蒸发
C . 萃取
D . 过滤
|
|
| 5. 综合题 | 详细信息 |
|
铬铁矿的主要成分为亚铬酸亚铁(
 ),还含有 ),还含有  及少量难溶于水和碱溶液的杂质。以铬铁矿为原料制备重铬酸钾( 及少量难溶于水和碱溶液的杂质。以铬铁矿为原料制备重铬酸钾(  )的工艺流程如图所示: )的工艺流程如图所示: 回答下列问题:
|
|
| 6. 单选题 | 详细信息 |
|
由含[Cu(NH3)4]Cl2的蚀刻废液制取[Cu(NH3)4]CO3溶液的流程如图:
下列有关说法错误的是( )
A . 上述制取流程不涉及氧化还原反应
B . “沉铜”在加热条件下进行,发生反应的离子方程式为[Cu(NH3)4]
 +2OH- +2OH-  4NH3↑+CuO↓+H2O
C . “滤液”中大量存在的离子有Na+、 4NH3↑+CuO↓+H2O
C . “滤液”中大量存在的离子有Na+、  、Cl-和OH-
D . “浸铜”时温度过高可能导致铜的浸出率下降 、Cl-和OH-
D . “浸铜”时温度过高可能导致铜的浸出率下降
|
|
| 7. 实验探究题 | 详细信息 |
|
三氯化六氨合钴(III){[Co(NH3)6]Cl3}是制备其它三价钴配合物的重要试剂。实验室以活性炭为催化剂,合成三氯化六氨合钴(III)晶体的流程如图
已知:①Co2+不易被氧化,Co3+具有强氧化性;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。 ②[Co(NH3)6]Cl3·6H2O在水中的溶解度随温度的升高而增大,加入浓盐酸有利于晶体析出。
|
|
| 8. 实验探究题 | 详细信息 |
|
高铁酸钾(K2FeO4)为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中产生O2 , 在碱性溶液中较稳定。
|
|
| 9. 单选题 | 详细信息 |
|
实验室以CaCO3为原料制备CO2并获得无水CaCl2。下列装置能达到相应实验目的的是( )
A . 装置①生成CO2
B . 装置②除去CO2中的HCl
C . 装置③干燥CO2
D . 装置④制得无水CaCl2
|
|
| 10. 单选题 | 详细信息 |
|
烟气脱硫能有效减少SO2的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[(1-x)Al2(SO4)3·xAl2O3]溶液,并用于烟气脱硫。下列说法正确的是( )
A . “酸浸”后,所得滤渣Ⅰ的主要成分为H2SiO3
B . pH约为3.6时,溶液中存在大量的H+、Al3+、CO
 C . 调pH时,若pH偏高,则所得溶液中c(Al3+)将增大
D . 碱式硫酸铝溶液经多次循环使用后,所得溶液中c(SO
C . 调pH时,若pH偏高,则所得溶液中c(Al3+)将增大
D . 碱式硫酸铝溶液经多次循环使用后,所得溶液中c(SO 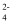 )将增大 )将增大
|
|
- 2016-2017学年福建省宁德市部分一级达标中学高二上学期期中化学试卷
- 广东省深圳市2018-2019学年高考理综-化学一模考试试卷
- 山东省枣庄市薛城区2017-2018学年高一上学期化学期中考试试卷
- 2016-2017学年江苏省盐城市高三上学期期中化学试卷
- 2015-2016学年云南省保山市腾冲八中高一下学期期中化学试卷(理科)
- 四川省攀枝花市2017-2018学年高一上学期化学期末考试试卷
- 高中化学人教版(2019)必修第一册第二章第二节 氯及其化合物
- 高中化学鲁科版(2019)选择性必修1 第1章第1节 化学反应的热效应
- 2016年上海市崇明县高考化学一模试卷
- 2017年高考化学备考复习专题六:非金属及其化合物
- 北京师大附中2017-2018学年高二上学期化学期中考试试卷
- 浙江省海宁市三校2015-2016学年高二下学期化学期中考试试卷
- 认真观察下面一幅漫画,按要求答题。(4分)(1)给这幅漫画拟一个标题,6字以内。(2分) 答:(2)这幅漫画讽
- 某同学做了如下实验:把点燃的一支蜡烛伸进盛有氧气的干燥集气瓶里,燃烧停止后,冷却,可观察到瓶内壁上有附着,由此说明蜡烛燃
- (2015·呼和浩特中考)在下面语段中,先找出有语病的句子,然后提出修改意见。 ①为了端正学生的学习态度,提高教师的业
- 下列因式分解正确的是( ) A. B. C. D.
- The Maldives faces the threat of extinctionfrom rising sea l
- 唐朝时发明的筒车,主要优势体现在( ) A.运用了自然力 B.可调节水的流量
- 做“探索弹力与弹簧伸长量关系”的实验步骤如下: A.以弹簧伸长量为横坐标,以弹力为纵坐标,描出各组数据(x,F)对应的点
- 每天都会有新的盐分进入海水,海水中也有一些盐分进入海床沉积层、新注入的盐分数量与海水里跑掉的盐分数量互相抵消,海水的平均
- 如图所示,质量m=2kg的小物块从倾角θ=37°的光滑斜面上的A点由静止开始下滑,经过B点后进入粗糙水平面,已知AB长度
- 直接促使日本无条件投降的重要事件是( ) ①中国人民发起全面反攻 ②苏联出兵中
- 下列几种溶液久置于空气中,溶质成分不变,但溶质的质量分数减小且溶液质量增加的是( ) A. 浓硫酸
- 下列各组词语中读音或书写正确的一组是 A.拮责jié 心无旁骛 wù B.亵xiè渎
- 如图所示是滑动变阻器的结构示意图,当把滑动变阻器接入电路中并要求当滑片P向B端移动时,电路中的电流变大,则应该把电路的两
- ________ is no possibility ________ Bob can win the first pr
- 一机器可以按各种不同的速度运转,其生产物件有一些会有缺点,每小时生产有缺点物件的多少随机器运转速度而变化,用x表示转速(
- 煤、石油、天然气是重要的化石燃料,下列关于化石燃料的叙述错误的是A.石油是一种化工产品B.将石油分馏可得到多种产品C.将
- 苹果醋具有保健养生、改善疲劳、美容养颜等功能,其中含有的苹果酸化学式为C4H6O5 。下列有关说法正确的是 A.苹果醋是
- 等物质的量的钠、镁、铝与足量稀H2SO4反应生成的氢气的物质的量之比是 A.1:1:1 B.1:2:3
- 读下列材料,回答下列问题 材料一:图15为世界部分区域图。近年来北冰洋海冰融化速度加快,流出北冰洋的洋流增强。同
- 如图,已知AB∥CD,则∠A、∠C、∠P的关系为____________________________。
 的制备
的制备 步骤Ⅱ.产品中
步骤Ⅱ.产品中  含量测定
含量测定 盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸
盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸  ;
; ;
; 平均值为22.45,
平均值为22.45,  平均值为23.51。
平均值为23.51。 开始分解。
开始分解。






 的
的  ,
,  的
的  ,
,  );
);
 ,在高温条件下,
,在高温条件下,  、葡萄糖(
、葡萄糖(  )和
)和  ,同时生成
,同时生成  和
和  ,该反应的化学方程式为
,该反应的化学方程式为
 ,冷却后用
,冷却后用  调
调  为3.5~4,再煮沸
为3.5~4,再煮沸  ,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、、乙醇洗涤、,得到胆矾。其中,控制溶液
,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、、乙醇洗涤、,得到胆矾。其中,控制溶液  ,加入胆矾后总质量为
,加入胆矾后总质量为  ,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为
,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为  。根据实验数据,胆矾分子中结晶水的个数为(写表达式)。
。根据实验数据,胆矾分子中结晶水的个数为(写表达式)。

 和
和  ,该反应的氧化剂和还原剂的物质的量之比为。
,该反应的氧化剂和还原剂的物质的量之比为。
 、
、  、
、  等阴离子。利用“煅烧”产生的气体X调节pH,可防止产品混入较多的杂质,则气体X为(填化学式,下同),滤渣2的主要成分为。
等阴离子。利用“煅烧”产生的气体X调节pH,可防止产品混入较多的杂质,则气体X为(填化学式,下同),滤渣2的主要成分为。
 会转化为
会转化为  ,影响产品的纯度并产生有毒气体污染环境,写出影响产品纯度的相关反应离子方程式。
,影响产品的纯度并产生有毒气体污染环境,写出影响产品纯度的相关反应离子方程式。
 溶液进行处理,将
溶液进行处理,将  转化为
转化为  ,平均每次消耗了vmL。废水中
,平均每次消耗了vmL。废水中  为。(用含a、b、v的式子表示)。
为。(用含a、b、v的式子表示)。 ,使
,使  而沉降,分离出污泥,检测到废水中
而沉降,分离出污泥,检测到废水中  ,室温下
,室温下 
 。
。



 +
+  =Fe(OH)3+
=Fe(OH)3+  +OH-
+OH- +H2O
+H2O




