(人教版)2023-2024学年高中化学必修第一册 1.3氧化还原反应 同步分层训练培优版
(人教版)2023-2024学年高中化学必修第一册 1.3氧化还原反应 同步分层训练培优版
教材科目:化学
试卷分类:高一上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高一上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
有Fe2+、NO3-、Fe3+、NH4+、H2O和H+六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述错误的是 ( )
A . 氧化剂与还原剂的物质的量之比为1:8
B . 还原产物为NH4+
C . 若有1mol NO3-参加还原反应,转移8mole-
D . 该反应中H2O是反应物之一
|
|
| 2. 综合题 | 详细信息 |
|
氧化还原是一类重要的反应。
|
|
| 3. 综合题 | 详细信息 |
|
氧化还原是一类重要的反应。
|
|
| 4. 单选题 | 详细信息 |
|
纯碱在生产、生活中有广泛应用。例如可用足量的纯碱溶液吸收含氯气的尾气,生成三种盐(反应1);工业上也可用纯碱溶液从海水中提取溴,其主要原理如下:
反应2: 反应3: 下列说法正确的是( )
A . 反应2中氧化剂与还原剂的质量之比为1∶5
B . 标准状况下,22.4L溴单质中含有2mol溴原子
C . 反应1中生成的三种盐是NaClO,
 和 和 D . 反应2中的
D . 反应2中的 与反应1中的 与反应1中的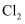 表现出了相似的化学性质 表现出了相似的化学性质
|
|
| 5. 单选题 | 详细信息 |
|
工业上常用NaClO碱性溶液吸收工业废气中的SO2 , 为了提高吸收效率,常用Ni2O3 , 作为催化剂,在反应过程中产生的四价镍和氧原子都具有极强的氧化能力,可加快对SO2的吸收,其中的催化过程如图所示:
下列说法不正确的是( )
A . NaClO碱性溶液吸收SO2的离子方程式是:ClO-+SO2+2OH-=Cl-+SO42-+H2O
B . 过程1的离子方程式是:ClO-+Ni2O3=2NiO2+Cl-
C . 过程2中,氧化剂是ClO- , 还原剂是NiO2
D . 此催化过程的离子反应为:ClO-
 Cl-+O Cl-+O
|
|
| 6. 推断题 | 详细信息 | ||||
某溶液Q中含有如表所示离子中的5种离子,且离子浓度均为0.5mol/L(不考虑水的电离与离子水解)。现向溶液Q中加入足量稀氢溴酸,有单一气体R产生,经分析,反应前后阴离子种类不变。
已知
|
|||||
| 7. 综合题 | 详细信息 |
|
回答下列问题
|
|
| 8. 综合题 | 详细信息 |
铁是人类较早使用的金属之一。化学研究中涉及到铁及其化合物的相关文献种类很多。请回答下列问题:
|
|
| 9. 单选题 | 详细信息 |
汽车都安装有安全气囊,发生剧烈的碰撞时,安全气囊中会发生反应:
|
|
| 10. 单选题 | 详细信息 |
下列有关主要应用不涉及氧化还原反应的是
A .
 和 和 混合液可用于除铁锈
B . 混合液可用于除铁锈
B .  溶液可用于制作铜印刷电路板
C . 溶液可用于制作铜印刷电路板
C .  可用于天然水的杀菌消毒和净化
D . 可用于天然水的杀菌消毒和净化
D .  可用于呼吸面具和潜水艇中的氧气的供给 可用于呼吸面具和潜水艇中的氧气的供给
|
|
高中化学 试卷推荐
- 人教版化学高二选修1第二章第一节合理选择饮食同步练习
- 黑龙江省大庆市三校联考2018-2019学年高二下学期化学期末考试试卷
- 上海市普陀区2016-2017学年高考化学二模考试试卷
- 2015-2016学年广西柳州市铁路一中高一上学期段考化学试卷
- 2015-2016学年山东省临沂市蒙阴一中高二下学期期中化学试卷
- 江苏省盐城市2018-2019学年高一下学期化学期末考试试卷
- 浙江省百校联盟2019-2020学年高三上学期化学10月月考试卷
- 高中化学人教版必修1 第一章第一节 化学实验基本方法
- 2015-2016学年河北省邯郸一中高一下学期期中化学试卷(实验班)
- 重庆市垫江县2017-2018学年高三上学期理综-化学开学考试试卷
- 重庆市区县2018-2019学年高二下学期化学期末考试试卷
- 北京市东城区2017-2018学年高三上学期化学期末考试试卷
最近更新
- 计算:. 1
- 已知函数f(x)=lnx-,其中a∈R. (1) 当a=2时,求函数的图象在点(1,f(1))处的切线方程; (2) 如
- 分解因式:3a3 - 12a = .
- 孟德尔发现了两大遗传定律,他获得成功的原因包括: ①正确选用实验材料;②采用从单因子到多因子的研究方法;③应用统
- 请根据你的积累,将正确项选出( )(2分)A.《智取生辰纲》节选自《水浒》,记晁盖、吴用等人劫取梁中书生辰纲的经过.故
- 阅读下面一段文字,按要求写作。 人类文化遗产不仅有物质的,如我国的泰山、长城、苏州古典园林等已被评为世界历史文化遗产;还
- 液氨在工业生产上有着广泛应用,然而由于忽视安全,液氨泄漏事件时有发生。下列有关说法错误的是() A.液氨常用作制冷剂B
- 阅读下面这首诗,完成后面小题。 古风(其十) 李 白 齐有倜傥生,鲁连①特高妙。 明月出海底,一朝开光曜。 却秦振英声,
- 在△ABC中,,则△ABC为( ) A.锐角三角形 B.直角三角形 C.钝角三角形 D.无法判定
- 咳嗽是一种常见病,肺结核会引发咳嗽,其他病原体引起的肺炎也有咳嗽的症状,花粉过敏也可能会引发咳嗽。下列相关叙述正确的是(
- 如图,两个同心圆中,大圆的半径是小圆半径的2倍,把一粒大米抛到圆形区域中,则大米落在小圆内的概率为( ) A
- 一列简谐横波在某一时刻的波形图如图1 所示,图中P、Q两质点的横坐标分别为 x=1.5m和x=4.5m。.P点的振动图像
- 20. Don’t be too wordy. Just give me a very _____ answer. A.
- 将矩形纸片ABCD按如图所示的方式折叠,得到菱形AECF.如果AB=,那么BC的长为_______.
- 能够分解水中有机物达到净化污水作用的细菌是( ) A.乳酸菌 B.甲烷菌
- 图中的虚线是水平运动物体的原始方向,实线是其偏转方向,正确的图示是
- 下列字形和划线字注音全部正确的一项是( )(2分) A.戳穿寒噤(jìn)不言而喻锲而不舍(qiè) B.隔陌狡黠(
- 填空(4分,每空0.5分) (1)《劝学》第二段,荀子以亲身的体验,强调空想不如学习。他说:“
- 阅读下面的文字,完成1—3题。 陕北说书 延安人民喜闻乐见的陕北说书,其发生、发展的历史,理应同陕北道情①同步,但因无足
- 己知元素的离子aAn+、bB(n+1)+、cCn-、dD(n+1)-均是由同周期主族元素形成的简单离子。下列叙述正确的是
 SiCl4+2CO 当反应消耗6 g 碳时,生成还原产物mol。
SiCl4+2CO 当反应消耗6 g 碳时,生成还原产物mol。
 ;
; 。
。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、
 、
、 、
、 、
、 、
、 、
、 、
、 、
、

 与
与 的反应,则根据实验现象可推算出V的范围为<V<。
的反应,则根据实验现象可推算出V的范围为<V<。 , 在上述过程中
, 在上述过程中 被(填“氧化”或“还原”),
被(填“氧化”或“还原”),

 、
、 、
、 三种离子的氧化性由强到弱的顺序是。
三种离子的氧化性由强到弱的顺序是。 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。
 和浓盐酸制氯气的反应为
和浓盐酸制氯气的反应为
 被还原,那么被氧化的氯化氢的质量为。
被还原,那么被氧化的氯化氢的质量为。


 , 有关该反应说法正确的是
, 有关该反应说法正确的是
 是还原剂
是还原剂 发生还原反应
发生还原反应 既是氧化反应的产物也是还原反应的产物
既是氧化反应的产物也是还原反应的产物


