高考二轮复习知识点:硫酸根离子的检验
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
下列有关实验的操作正确的是( )
A . 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗
B . 检验某溶液是否含有SO
 时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸
C . 为观察Mg条在CO2气体中的燃烧,在一个底部铺有少量玻璃棉的集气瓶中收集满CO2气体,取一小段除去表面氧化膜的Mg条用坩埚钳夹持点燃后迅速投入上述集气瓶底部
D . 用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH值 时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸
C . 为观察Mg条在CO2气体中的燃烧,在一个底部铺有少量玻璃棉的集气瓶中收集满CO2气体,取一小段除去表面氧化膜的Mg条用坩埚钳夹持点燃后迅速投入上述集气瓶底部
D . 用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH值
|
|
| 2. 综合题 | 详细信息 |
|
化学小组实验探究
 与 与 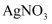 溶液的反应。 溶液的反应。
|
|
| 3. 单选题 | 详细信息 |
|
下列实验方案中,能达到实验目的的是( )
A . A
B . B
C . C
D . D
|
|
| 4. 单选题 | 详细信息 |
|
对溶液中下列离子进行检验,正确的操作是( )
A . NH4+:取样,加入氢氧化钠溶液,即产生使湿润红色石蕊试纸变蓝的气体
B . SO42-:取样,加入足量的盐酸无现象,再滴入氯化钡溶液有白色沉淀产生
C . Fe2+:取样,滴入硫氰化钾溶液无现象,再加入过量的氯水,溶液呈血红色
D . Cl-:取样,滴入硝酸银溶液产生白色沉淀,再加入过量的硫酸沉淀不消失
|
|
| 5. 单选题 | 详细信息 |
|
某溶液含有Ba2+、Fe2+、Cl-、NO3-等离子,向其中加入足量的稀硫酸后,溶液中离子的物质的量几乎不变的是( )
A . Ba2+
B . Fe2+
C . Cl-
D . NO3-
|
|
| 6. 单选题 | 详细信息 | ||||||||||||||||||||
|
下列实验操作、现象与结论对应关系正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 7. 单选题 | 详细信息 |
|
向FeCl3溶液中加入Na2SO3溶液,测定混合后溶液pH随混合前溶液中
 变化的曲线如图所示。 变化的曲线如图所示。 实验发现: ⅰ.a 点溶液澄清透明,向其中滴加 NaOH 溶液后,立即产生灰白色沉淀,滴入 KSCN 溶液显红色; ⅱ.c 点和 d 点溶液中产生红褐色沉淀,无气体逸出;取其上层清液滴加NaOH溶液后无明显现象,滴加 KSCN 溶液显红色。 下列分析合理的是( )
A . 检验a点溶液中反应生成的阴离子所需试剂为:稀硝酸和BaCl2溶液
B . c点和d点出现上述现象的主要原因是Fe3+和
 发生双水解反应
C . b点较a点溶液pH升高的主要原因:2Fe3++ 发生双水解反应
C . b点较a点溶液pH升高的主要原因:2Fe3++  +H2O = 2Fe2++ +H2O = 2Fe2++  +2H+
D . 向d点上层清液中滴加 NaOH溶液无明显现象,证明溶液中无Fe3+ +2H+
D . 向d点上层清液中滴加 NaOH溶液无明显现象,证明溶液中无Fe3+
|
|
| 8. 单选题 | 详细信息 | |||||||||||||||
|
室温下,进行下列实验,根据实验操作和现象所得的结论正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 9. 实验探究题 | 详细信息 | |||||||||||||
|
某研究性学习小组查阅资料收集到如下信息:铁盐能蚀刻银而用来制作液晶显示器的银线路板。他们对蚀刻银的过程进行了探究。
|
||||||||||||||
| 10. 实验探究题 | 详细信息 |
|
胆矾(
 )易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的 )易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的  (杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题: (杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
|
|
- 浙江省湖州市2020-2021学年高二上学期化学期末考试试卷
- 浙江省金华市金华十校2020-2021学年高一上学期化学期末考试试卷
- 辽宁省本溪满族自治县2021-2022学年高一下学期开学考试化学试题
- 冲刺2021高考化学押题训练(一)物质的组成、性质、分类和化学用语
- 江西省萍乡市2021-2022学年高一下学期期中考试化学试题
- 江苏省如皋市2020-2021学年高二下学期化学开学考试试卷
- 广东省东莞市2020-2021学年高二下学期期末统考化学试题
- 广西钦州市2020-2021学年高一下学期期末考试化学(理)试题
- 新疆昌吉教育共同体2020-2021学年高二下学期化学期末考试试卷
- 陕西省咸阳市武功县2021-2022学年高一下学期期中质量调研化学试题
- 湖南省名校联盟2021-2022学年高二上学期期末教学质量检测化学试题
- 安徽省滁州市2020-2021学年高一上学期期末联考化学试题
- 图7为大陆西岸四个地点的地理位置示意图。读图回答下列各题。若不考虑地形因素,四个地点中1月份降雨较多的是A、甲 丙
- 能源的开发和利用是当前科学研究的重要课题。(1)利用二氧化铈(CeO2)在太阳能作用下前实现如下变废为宝的过程: mC
- 不同元素间最本质的区别是A.中子数不同 B.电子数不同 C.质子数不同 D.相对原子质量
- 在一个光滑水平的桌面上做直线运动的小铁球旁:放置一磁铁,铁球在磁铁的吸引下,运动轨迹如图虚线所示,A、B为轨迹上的两点,
- 万民法在财产规定方面的主要思想是( ) A、保护奴隶主利益 B、保护所有公民利益 C、保护私有财产
- 某合金(仅含铜、铁)中铜和铁的物质的量之和为ymol,其中Cu的物质的量分数为a ,将其全部投入100mLbmol·L-
- _____ excited the whole nation most is_____ more than 100 wo
- 由于天气寒冷,吃早饭时妈妈要用热水给小明加热250 g瓶装牛奶,如图2-7所示,要使这瓶牛奶的温度由10℃最终升高到50
- 狮子捕食斑马,其生理意义在于( ) A.获取营养 B.强者欺凌弱者 C.游戏 D.将它驱除出领地
- 4x(2x+1)=3(2x+1);
- 1945年日本投降后,重庆一家报纸以“日本无条件投降”为谜面,要求打一个中国古代历史人物,当时谜底有两个:屈原(原子弹)
- 质点做直线运动的v-t图象如图所示,规定向右为正方向,则该质点在前8 s内平均速度的大小和方向分别为( ) A.0.
- 分类是学习和研究化学物质及其变化的一种常用的基本方法.现有生铁,它与下列哪组属于同一类物质() A.硫酸亚铁、氯化铁 B
- 几位同学讨论课本中的熔点表时,发表了以下几种观点,正确的是 A.熔点表中各物质熔化时都要吸收热量且温度保持不变 B.熔点
- 中国古代社会经济发展的根本特点是自给自足,为谋生而非谋利,为消费而非交换。这一根本特点决定了我国历代王朝推行的经济政策是
- 如图甲所示,物块A、B的质量分别是 mA= 4.0kg 和 mB= 3.0kg,用轻弹簧相连放在光滑的水平地面上,物块B
- 血液中有一种含铜的呈蓝色的蛋白分子,其相对分子质量为151 000。已知其中铜元素的质量分数为0.34%,则平均每个分子
- 下列物质由分子构成的是() A.金 B.氨气 C.氯化镁
- 八年级学生周末乘汽车到游览区游览,游览区距学校180km.一部分学生乘慢车先行,出发1h后,另一部分学生乘快车前往,结果
- 2008年清明节刚过,王先生购买彩票就中了一个500万元的大奖,交税后实得400万。经过一段时间的思考,王先生决定用这笔

 与Cu反应的化学方程式是
与Cu反应的化学方程式是 、
、  或二者混合物。
或二者混合物。 
 ,进而推断B中含有
,进而推断B中含有  的产生有两个途径:
的产生有两个途径: 进入D。
进入D。 溶液,未出现白色沉淀,可判断B中不含
溶液,未出现白色沉淀,可判断B中不含 
 溶液的试管中加入
溶液的试管中加入  的
的 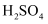 溶液
溶液 被
被  还原为
还原为 
 酸化的
酸化的  溶液中
溶液中
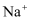

 氧化了银,证据是。通过如下实验验证了推测是合理的:
氧化了银,证据是。通过如下实验验证了推测是合理的:
 ,冷却后用
,冷却后用  调
调  为3.5~4,再煮沸
为3.5~4,再煮沸  ,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、、乙醇洗涤、,得到胆矾。其中,控制溶液
,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、、乙醇洗涤、,得到胆矾。其中,控制溶液  ,加入胆矾后总质量为
,加入胆矾后总质量为  ,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为
,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为  。根据实验数据,胆矾分子中结晶水的个数为(写表达式)。
。根据实验数据,胆矾分子中结晶水的个数为(写表达式)。



