从巩固到提高 高考化学二轮微专题38 晶体结构
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
砷化镉晶胞结构如图。图中“①”和“②”位是“真空”,晶胞参数为apm,建立如图的原子坐标系,①号位的坐标为(
 , ,  , ,  )。已知:砷化镉的摩尔质量为Mg/mol,NA为阿伏加德罗常数的值。下列说法错误的是( ) )。已知:砷化镉的摩尔质量为Mg/mol,NA为阿伏加德罗常数的值。下列说法错误的是( )
A . 砷化镉中Cd与As原子个数比为3:2
B . 两个Cd原子间最短距离为0.5apm
C . ③号位原子坐标参数为(
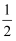 , 1, , 1,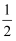 )
D . 该晶胞的密度为 )
D . 该晶胞的密度为 g·cm-3 g·cm-3
|
|
| 2. 综合题 | 详细信息 |
|
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
|
|
| 3. 综合题 | 详细信息 |
|
铜及其化合物在能源、信息等领域应用广泛。回答下列问题:
|
|
| 4. 综合题 | 详细信息 | ||||||||
|
KH2PO4晶体具有优异的非线性光学性能。我国科学工作者制备的超大KH2PO4晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
|
|||||||||
| 5. 综合题 | 详细信息 |
|
超导材料和超导技术是2世纪最伟大的发现之一,有着广阔的应用前景。我国科学家发现了一种新型的超导体材料
 , 由 , 由 和 和 交替堆叠构成。其中A层是由 交替堆叠构成。其中A层是由 无限四方平面层构成,S原子位于八面体上下顶点上(如图a),其俯视图如图b。 无限四方平面层构成,S原子位于八面体上下顶点上(如图a),其俯视图如图b。
|
|
| 6. 综合题 | 详细信息 |
|
碳族元素在生产生活中的应用极其广泛,请回答以下有关碳族元素的问题。
|
|
| 7. 综合题 | 详细信息 |
|
氮族元素包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi),在性质上表现出从典型的非金属元素到典型的金属元素的一个完整的过渡。
|
|
| 8. 综合题 | 详细信息 | ||||||||||||||||
|
我国中科院天津工业技术研究所,首次实现人工通过二氧化碳合成淀粉。请回答下列问题:
|
|||||||||||||||||
| 9. 综合题 | 详细信息 |
|
|
| 10. 综合题 | 详细信息 |
|
钾离子电池以其优异的性能成为替代锂离子电池的一种选择,该电池的负极是由钾嵌入石墨中构成,正极主要含
 、铝箔、醚类有机物等。从某废旧钾离子电池中回收部分材料的流程如下: 、铝箔、醚类有机物等。从某废旧钾离子电池中回收部分材料的流程如下:
已知:I.放电时负极的电极反应式为 II.常温下, 回答下列问题:
|
|
- 四川省德阳市2022届高三三诊理综化学试题
- 浙江省宁波市2021-2022学年高三上学期化学10月月考试卷
- 广东省广州市海珠区2021-2022学年高一上学期期末考试化学试题
- 广西北海市2021-2022学年高三上学期第一次化学模拟考试理综化学试题
- 江西省九江市2021年高考化学二模试卷
- 湖北省腾云联盟2021-2022学年高三上学期化学10月联考试卷
- 江苏省连云港市东海县2021-2022学年高二下学期期中考试化学试题
- 2021高考真题汇编-化学反应中的能量变化
- 上海市虹口区2021年高考化学二模试卷
- 吉林省永吉县第四中学2021-2022学年高一上学期化学9月月考试卷
- 辽宁省大连市2022届高三第一次模拟考试化学试题
- 四川省遂宁市2021-2022学年高三下学期三诊化学试题
- 科学家用含有14C的二氧化碳来追踪光合作用中的碳原子,这种碳原子的转移途径是: A.二氧化碳→叶绿素→ADP;
- 通过如图所示的实验(不考虑水分蒸发)得到相应的五种溶液。下列叙述不正确的是( ) A.t1℃时,溶液①是不饱
- Many kids ________ the net bar, and _____had a bad effect on
- 下列关于热力学第二定律的说法中,正确的是()A.如果没有能量损失,由热机把从单独一个热源吸收的热量全部转化成机械能B.热
- “权力不受制约必然产生腐败,加强法制监督是防止权力滥用的重要措施。”当前,全国人大正在不断通过新的法律制度加大反腐力度。
- 1、 当今世界,发达国家的人口再生产类型类似于A③ B② C① D④
- 18世纪的法国,越来越多的人不再盲从统治者的说教,学会了用自己的头脑思考问题。他们思考的问题与文艺复兴、宗教改革时期相
- 烟草、食用烟草的昆虫、烟草花叶病毒、甲型H1N1病毒中的核酸,含有的碱基种类分别是 A 5 4 5 4
- 下列有关电磁波的说法,正确的是( )A.电磁波不能在真空中传播B.电磁波在空气中的传播速度约为340m/sC.可见
- A、B两个点电荷在真空中所产生电场的电场线(其中方向未标出)的分布如图所示.图中O点为两点电荷连线的中点,MN为两点电
- 已知:2H2(g)+ O2(g)=2H2O(l) ΔH=-571.6 KJ·mol-1
- 阅读下面文章,完成后面小题。 云和梯田 张抗抗 传说中“中国最美的云和梯田”,隐匿于浙西南括苍山脉雾气迷蒙的群峰深处,弯
- 下列物质的用途主要由其化学性质决定的() A.用氮气保存食品 B.用氢
- 2008年奥运会吉祥物“中国福娃”近日在北京公布,北京奥运会吉祥物由五个分别以鱼、熊猫、奥运圣火、藏羚羊、京燕为创意,被
- Almost everyone is ________ bringing down the price of housi
- 如图表示染色体组成为AaCcDd的生物产生的精细胞,试根据细胞内染色体的组合,分析不考虑交叉互换的情况下,下列相关叙述不
- 有关内环境与稳态的叙述,正确的是 A.内环境的稳态就是指温度
- 硒(Se)是个导体材料,也是补硒保健品中的元素。工业上提取硒的方法之一是用H2SO4和NaNO3处理合Se的工业废料,而
- 如图表示某小岛上蜥蜴进化的基本过程.有关叙述中不正确的是() A. 图中X、Y、Z分别表示的是突变和基因重组
- 在一棵树的相同位置上,傍晚和次日早晨各取一片大小相似的叶片,分别用、表示,将两片叶干燥后称重,其关系为 A.

 , 其环状结构如图所示,S原子的杂化轨道类型是。
, 其环状结构如图所示,S原子的杂化轨道类型是。
 分子中共价键的类型是,常温下
分子中共价键的类型是,常温下 是气体而
是气体而 (NA表示阿伏加德罗常数的值)。
(NA表示阿伏加德罗常数的值)。

 表示,与之相反的用-
表示,与之相反的用- )形式存在的原因是。
)形式存在的原因是。 电子总数相同的等电子体的分子式为。
电子总数相同的等电子体的分子式为。

 和K+ , KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+ , KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO


 )具有良好的抗炎活性。下列说法正确的是。
)具有良好的抗炎活性。下列说法正确的是。 和
和 的键角相同
的键角相同 是一种极少数不溶性的钠盐,其阴离子的立体构型为。
是一种极少数不溶性的钠盐,其阴离子的立体构型为。



 是芳香性π配体,P的杂化方式是 ,
是芳香性π配体,P的杂化方式是 , 表示,其中m代表形成大π键的原子数,n代表形成大π键的电子数)
表示,其中m代表形成大π键的原子数,n代表形成大π键的电子数)


 表示,与之相反的用-
表示,与之相反的用- 与CO2互为等电子体,写出
与CO2互为等电子体,写出
 )检验Fe2+ , 生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子参与杂化的原子轨道为。
)检验Fe2+ , 生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子参与杂化的原子轨道为。 属于多卤素阳离子,其空间构型为。
属于多卤素阳离子,其空间构型为。


 ;
; , 当溶液中某离子浓度低于
, 当溶液中某离子浓度低于 时,认为该离子已沉淀完全。
时,认为该离子已沉淀完全。 (填“已”或“未”)沉淀完全。
(填“已”或“未”)沉淀完全。
 溶液的操作名称为。
溶液的操作名称为。
 , 则石墨晶体密度为
, 则石墨晶体密度为 (列式即可)。
(列式即可)。




