高考二轮复习知识点:物质的分离与提纯6
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 | |||||||||||||||
|
磁选后的炼铁高钛炉渣,主要成分有
 、 、  、 、  、MgO、CaO以及少量的 、MgO、CaO以及少量的  ,为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。 ,为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
该工艺下,有关金属离子开始沉淀和沉淀完全的pH见下表:
回答下列问题:
|
||||||||||||||||
| 2. 单选题 | 详细信息 |
|
氧化铍(BeO)在航天航空等领域有着广泛的应用。一种以预处理后的硅铍矿(主要含BeO、Fe2O3、SiO2和FeO等)为原料提取BeO的流程如下图所示:
已知:Be(OH)2具有两性,在强碱性溶液中可转化为BeO 下列说法错误的是( )
A . “酸浸”步骤所得“滤渣①”的主要成分为SiO2
B . “滤液②”经处理后可获得副产品Na2SO4▪10H2O
C . “碱溶”时,主要反应为Be(OH)2+2OH-=BeO
 +2H2O
D . “水解”时,适当增大溶液pH有利于提高BeO的提取率 +2H2O
D . “水解”时,适当增大溶液pH有利于提高BeO的提取率
|
|
| 3. 实验探究题 | 详细信息 | ||||||||||||
|
CuCl2是常见的化学试剂,学习小组开展了与CuCl2相关的系列实验。回答下列问题:
|
|||||||||||||
| 4. 单选题 | 详细信息 |
|
高氯酸钾是一种强氧化剂,易溶于水.以氯化钠为原料制备高氯酸钾的一种流程如图:
下列说法错误的是( )
A . “电解”生成气体的主要成分为H2
B . “高温分解”反应中氧化剂和还原剂的物质的量之比为3∶1
C . 本实验条件下,KClO4在水中的溶解度比NaClO4小
D . 母液经分离、提纯可制得食盐
|
|
| 5. 综合题 | 详细信息 |
|
氧化钴
 可制备反铁磁材料、催化剂、电极材料等.由富钴废液(含 可制备反铁磁材料、催化剂、电极材料等.由富钴废液(含  、 、  、 、  、 、  、 、  )制备氧化钴的一种流程如图: )制备氧化钴的一种流程如图: 已知:Ⅰ.“反应”过程中 Ⅱ.烧渣中含有 回答下列问题:
|
|
| 6. 综合题 | 详细信息 |
|
二氧化钛和三氧化钨(TiO2/WO3)纳米异质结薄膜广泛应用于光催化、光电催化和传感器等领域。从废弃薄膜中回收钛和钨等稀缺金属既有利于资源综合利用又避免污染环境,以下是TiO2/WO3纳米异质结薄膜回收的工艺流程:
已知: Ⅰ.乙胺是无色极易挥发的液体,结构简式为CH3CH2NH2 , 呈碱性,与酸发生反应:CH3CH2NH2+H+=CH3CH2NH Ⅱ.酸性条件下,Na2WO4与乙胺“萃取”发生反应:2CH3CH2NH Ⅲ.TiOSO4易溶于水,属于强电解质;偏钛酸难溶于水,其化学式可表示为H2TiO3或TiO(OH)2 , 室温时,Ksp[TiO(OH)2]=1.0×10-27。 回答下列问题:
|
|
| 7. 综合题 | 详细信息 | ||||||||||
|
氯化亚铜(CuCl)可用作有机合成的催化剂,CuCl微溶于水,不溶于醇和稀酸,可溶于Cl-浓度较大的溶液(CuCl+Cl-
 CuCl CuCl  ),在潮湿空气中易水解、易氧化。工业上用黄铜矿(主要成分是CuFeS2 , 还含有少量的SiO2)制备CuCl的工艺流程如图: ),在潮湿空气中易水解、易氧化。工业上用黄铜矿(主要成分是CuFeS2 , 还含有少量的SiO2)制备CuCl的工艺流程如图: 25℃时,相关物质的Ksp见表。
回答下列问题:
|
|||||||||||
| 8. 实验探究题 | 详细信息 |
|
水合肼(N2H4·H2O)是一种重要的化工原料,工业上用尿素[CO(NH2)2]、NaOH和NaClO溶液反应制备水合肼的实验流程如图:据此某化学兴趣小组设计了下列实验制备N2H4·H2O。
查阅资料:①3NaClO
|
|
| 9. 综合题 | 详细信息 | |||||||||||||||
|
某油脂厂废弃的油脂加氢所用催化剂主要含金属Ni、Al、Fe及他们的氧化物,还有少量其他不溶性物质。采用如图工艺流程回收其中的镍来制备硫酸镍晶体(NiSO4·7H2O):
溶液中金属离子开始沉淀和完全沉淀的pH如表所示,回答下列问题:
|
||||||||||||||||
| 10. 综合题 | 详细信息 | ||||||
|
工业生产中会产生稀土草酸沉淀废水,其主要成分为盐酸和草酸(H2C2O4)的混合溶液及微量的草酸稀土杂质等。工业上处理废水的方法包括“①氧化法”和“②沉淀法”。相关工业流程如图所示:
已知:①Ka1(H2C2O4)=6.0×10-2;Ka2(H2C2O4)=6.25×10-5。 ②25℃时,各物质的溶度积常数如表:
回答下列问题:
|
|||||||
- 备考2020年高考化学二轮专题 07 化学反应中的能量变化
- 河北省唐山市2017-2018学年高考理综-化学二模考试试卷
- 人教版化学高二选修4第二章第四节化学反应进行的方向同步练习
- 浙江省嘉兴市2016-2017学年高一上学期期末考试试卷
- 专题07:镁、铝及其化合物
- 2016年高考理综真题试卷(化学部分)(天津卷)
- 2017_2018学年高中化学人教版选修四 第四章电化学基础4.2化学电源b
- 2017年江西省高考化学模拟试卷
- 2016年山东省菏泽市成武一中高考化学三模试卷
- 备考2018年高考化学一轮基础复习:专题14 原子结构 核外电子排布
- 湖南省永州市2019-2020学年高一下学期化学期末考试试卷
- 陕西省延安市实验中学大学区校际联盟2016-2017学年高二上学期化学期末考试试卷(A卷)
- Professor Maskus says the government shouldmake it easier f
- 为加强银行体系流动性管理,中国人民银行6月7日宣布上调存款准备金率1个百分点。这是我国今年以来第5次上调存款准备金率,上
- (本小题满分14分) 如图5所示,四棱锥的底面是半径为的圆的内接四边形,其中是圆的直径,,,. (1)求线段的长; (2
- 下列有关二氧化碳的用途中,不正确的是A.供给呼吸 B.作化工产品的原料 C.用于灭火 D.作气体肥料
- 2009年12月19日,庆祝澳门回归祖国10周年大会暨特区第三届政府就职典礼,特区政府欢迎晚宴上,强调澳门10年成就前所
- 设-3π<α<-,化简.
- 下列各组离子在指定溶液中能大量共存的是 (
- 下列选用的相关仪器符合实验要求的是
- 设集合,,,则 A. B.
- 陕西出土的大盂铜鼎铭文记载,周康王一次赏赐盂壹仟柒佰零玖个奴隶。据此铭文判断,盂受赏赐时的身份是 A.周康王的嫡长子
- 表示阿伏加德罗常数,下列叙述中正确的是:( ) A.通常状态下,和各1 mol含有的电子数均为 B.标准状况下当氧气
- 阅读下面的选文,回答16~21题。(16分) 背叛 ①在南极探险的途中,森和队伍失散了,伴随他的只有那少得可怜的行囊和一
- “存天理灭人欲,它本来是理学思想中一种卓越的自我修养,属于精神的领域,现在却成为面对广大民众的一种现实的社会伦常,沦落为
- (8分)如图,AB是半圆的直径,点O是圆心,点C是OA的中点,CD⊥OA交半圆于点D,点E是的中点,连接AE、OD,过点
- 有一包粉末,可能由KCl、K2SO4、K2CO3、CuCl2、MgCl2中的一种或几种物质组成。现做如下实验: 实验一:
- 已知用赤铁矿石冶炼铁的化学方程式为Fe2O3+3CO2Fe+3CO2 请计算:(相信你一定能行!) ⑴Fe2O3的相对分
- 二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是( )
- 下列反应属于化合反应的是() A.2HgO2Hg+O2↑ B.H2+CuOCu+H2O C.C2H5OH+3O22
- 比较昆虫、两栖动物、鸟类的生殖发育过程,你认为维恩图中①②③处代表的内容依次是( )A.变态发育 卵生
- 与无脊椎动物相比,脊椎动物的特征是( )A、都是陆生动物 B、都是哺乳动物 C、都是恒温动物 D、体内





 的化学方程式。
的化学方程式。

 水解析出
水解析出  沉淀,该反应的离子方程式是。
沉淀,该反应的离子方程式是。




 +H++
+H++  ⇌
⇌  +H2O,3
+H2O,3  +Co3+⇌3H++
+Co3+⇌3H++  ↓
↓ 、
、  、
、  、
、  、
、 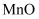 ;滤渣的成分为
;滤渣的成分为  、
、  。
。 ”时溶液的
”时溶液的  ,从
,从  废液中(废液的密度为
废液中(废液的密度为  )经此工艺最终得到
)经此工艺最终得到  ,则
,则 


 (CH3CH2NH3)2WO4
(CH3CH2NH3)2WO4



 2NaCl+NaClO3;②N2H4·H2O易溶于水,熔点-40℃,沸点为118℃,具有强还原性,能与NaClO剧烈反应生成N2;属于二元弱碱,在空气中可吸收CO2而产生烟雾。
2NaCl+NaClO3;②N2H4·H2O易溶于水,熔点-40℃,沸点为118℃,具有强还原性,能与NaClO剧烈反应生成N2;属于二元弱碱,在空气中可吸收CO2而产生烟雾。






