高考二轮复习知识点:探究物质的组成或测量物质的含量3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 推断题 | 详细信息 |
|
某兴趣小组对化合物X开展探究实验。
其中:X是易溶于水的强酸盐,由3种元素组成;A和B均为纯净物;B可使品红水溶液褪色。请回答:
|
|
| 2. 综合题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||
|
碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,并测定产品中少量碳酸氢钠的含量,过程如下:
步骤I. ①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中; ②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 ③在上述锥形瓶中再加入2滴指示剂N,继续用 ④平行测定三次, 已知:(i)当温度超过35℃时, (ii)相关盐在不同温度下的溶解度表
回答下列问题:
|
|||||||||||||||||||||||||||||||||||||||||
| 3. 单选题 | 详细信息 | ||||||||||||||||
 (俗称海波)是常用的一种定影剂。工业使用的海波中常混有少量 (俗称海波)是常用的一种定影剂。工业使用的海波中常混有少量 和 和 杂质,为测定一种海波晶体样品的成分,某同学称取三份质量不同的该样品,分别加入相同浓度的稀硫酸20mL,充分反应后测得有关实验数据如下(标准状况)。 杂质,为测定一种海波晶体样品的成分,某同学称取三份质量不同的该样品,分别加入相同浓度的稀硫酸20mL,充分反应后测得有关实验数据如下(标准状况)。
下列说法错误的是( )
A . 第一份、第二份样品均完全反应,第三份样品过量
B . 样品中
 C . 样品中除了含有
C . 样品中除了含有 、 、 , 还含有 , 还含有 D . 所加硫酸溶液的物质的量浓度为0.5mol/L
D . 所加硫酸溶液的物质的量浓度为0.5mol/L
|
|||||||||||||||||
| 4. 单选题 | 详细信息 |
|
有一固体由Na2CO3、NaCl、CaCl2、CuSO4中的一种或几种物质组成,为检验此混合物的组成,进行如下实验:①将少量固体混合物溶于水搅拌后,得无色透明溶液;②在上述溶液中滴加硝酸钡溶液,有白色沉淀生成;③过滤,在白色沉淀中加入过量稀硝酸,沉淀全部溶解。根据实验现象可判断其组成可能为( )
A . NaCl、CaCl2
B . Na2CO3、CaCl2
C . Na2CO3、NaCl
D . CaCl2、CuSO4
|
|
| 5. 综合题 | 详细信息 |
|
铅在氧化物中的价态有+2价和+4价,含+4价铅的氧化物是一种很强的氧化剂,常温时在酸性条件下可将
 氧化成 氧化成 , 自身还原为+2价。 , 自身还原为+2价。 在加热过程发生分解的失重曲线如下图所示。 在加热过程发生分解的失重曲线如下图所示。
已知: 请计算:
|
|
| 6. 综合题 | 详细信息 |
|
氯化铜、氯化亚铜广泛地用作有机合成催化剂。实验室中以粗铜粉(含杂质Fe)为原料,制备铜的氯化物,流程如图:
|
|
| 7. 单选题 | 详细信息 |
|
测量汽车尾气中氮氧化物(
 、 、 )含量的方法如下: )含量的方法如下:i.在高温、催化剂作用下, ii.再利用 下列说法不正确的是( )
A . 基态
 与 与 具有的能量不同
B . 具有的能量不同
B .  在大气中形成酸雨: 在大气中形成酸雨: C .
C .  与 与 发生反应: 发生反应: D . 测得荧光强度越大,说明汽车尾气中
D . 测得荧光强度越大,说明汽车尾气中 含量越高 含量越高
|
|
| 8. 单选题 | 详细信息 |
|
二氧化锰矿粉中
 含量测定实验流程如图。下列说法不正确的是( ) 含量测定实验流程如图。下列说法不正确的是( )
A .
 将 将 还原为 还原为 B . 滴定终点溶液的颜色从无色变为浅紫色
C .
B . 滴定终点溶液的颜色从无色变为浅紫色
C .  含量为 含量为 D . 若滴定终点时滴定管尖嘴处出现气泡,则测得
D . 若滴定终点时滴定管尖嘴处出现气泡,则测得 含量偏小 含量偏小
|
|
| 9. 综合题 | 详细信息 | |||||||||||||||
|
重铬酸钾在工业中有广泛的应用,某学习小组模拟工业制备重铬酸钾并探究其性质。
|
||||||||||||||||
| 10. 综合题 | 详细信息 |
|
黄铜矿[主要成分为
 , 含少量氯磷灰石 , 含少量氯磷灰石 ]为原料的火法炼铜主要流程如下: ]为原料的火法炼铜主要流程如下:已知:氯磷灰石高温下易被氧化为
|
|
- 高化人教新版必修1第一章第三节 氧化还原反应同步训练
- 2016-2017学年浙江省嘉兴市七校联考高一上学期期中化学试卷
- 2016-2017学年山东省临沂市蒙阴一中高二上学期期中化学试卷
- 广东省潮州市潮安区2019-2020学年高一下学期化学期末考试试卷
- 2017年山西省重点中学协作体高考化学模拟试卷(一)
- 2016-2017学年河南省河南大学荆紫关附中 高二上学期开学化学试卷
- 陕西省渭南市三贤中学2019-2020学年高一下学期化学期中考试试卷
- 第3讲:氧化还原反应
- 2015-2016学年山东省德州市跃华学校高二下学期期中化学试卷
- 安徽省合肥市庐江县2019-2020学年高一下学期化学期末考试试卷
- 2015-2016学年安徽省淮南市示范高中五校高一上学期第一次月考化学试卷
- 2015-2016学年湖北省襄阳市枣阳市育才学校高一下学期期中化学试卷
- 如图,在斜三棱柱ABC—A1B1C1中,AB=BC=2,∠ABC=120°,又顶点A1在底面ABC上的射影落在AC上,侧
- 计算:
- 某县城2009年底商品房均价为2000元/,经过2010年第1季度和第2季度的涨价,商品房均价达3600元/,设每季度平
- 阅读下面一首诗歌,然后回答问题。(6分) 夜泊钱塘(明)茅坤 江行日已暮,何处可维舟?树里孤灯雨,风前一雁秋。 离心迸落
- 下列说法正确的是 A.硫酸、纯碱、小苏打和生石灰分别属于酸、碱、盐和氧化物 B.蔗糖、硫酸钡和水分别属于非电解质、强电解
- 阅读下面的宋诗,然后回答问题。 游月陂 宋??程颢 月陂堤上四徘徊,北有中天百尺台。 万物已随秋气改,一樽聊为晚凉开。
- “穿睡衣睡裤不能出门”。这是2010年上海召开世博会之前,该市政府对居民的要求。这引起了广泛的争议。一方面,穿睡衣确实不
- 右图表示环境因素对绿色植物光合作用速率的影响,据图分析,正确的是( )A.当处于a或b点时,叶肉细胞的细胞质基质、
- 国务院《关于深化体制机制改革加快实施创新驱动发展战略的若干意见》,强调发挥市场竞争激励创新的根本作用,营造公平、开放、透
- 中国人民银行2008年9月15日发布的50个大、中、小城市城镇储户问卷调查显示,在当前物价和利率水平下,认为“更多储蓄”
- 某单位有技工18人,技术员12人,工程师6人,现从这些人中抽取一个容量为n的样本.如果采用系统抽样和分层抽样的方法抽取,
- 如图所示,水平的传送带上放一物体,物体下表面及传送带上表面均粗糙,导电性能良好的弹簧的右端与物体及滑动变阻器滑片相连,弹
- 世界第一经济强国,最大的资源消耗国和废物排放国是 A.日本 B.中国
- 明朝前期管辖东北女真族的机构是 A.黑水都督府 B.伊犁将军 C.奴儿干都
- We are all sorryto hear that the number of the Asian tigers
- 下列关于氢键的说法中,正确的是A.氢键比分子间作用力强,所以它属于化学键B.因为液态水中存在氢键,所以水比硫化氢稳定C.
- The children a P Eclass on the playground when it suddenl
- 依次填入下面横线处的语句,衔接最恰当的一组是 最初揭露“公务机要费弊案”的国民党籍立委邱教,4日上午表示:
- 在横线处填上恰当的关联词,使上下文连贯起来。 在教育教学过程中,学生____①____处于被动、从属地位、____②__
- 小孩用10N的水平拉力拉桌子,桌子未被拉动,桌子受到的摩擦力的大小为

 的制备
的制备 步骤Ⅱ.产品中
步骤Ⅱ.产品中  含量测定
含量测定 盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸
盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸  ;
; ;
; 平均值为22.45,
平均值为22.45,  平均值为23.51。
平均值为23.51。 开始分解。
开始分解。






 。
。 表示A点的化学组成,则
表示A点的化学组成,则 。
。
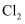 。求剩余固体中氧元素的质量。(写出计算过程)
。求剩余固体中氧元素的质量。(写出计算过程)


 CuCl42-(aq)(绿色)+4H2O(l)设计简单实验,证明溶液中有上述转化关系。
CuCl42-(aq)(绿色)+4H2O(l)设计简单实验,证明溶液中有上述转化关系。


 , 还含有
, 还含有 等杂质)制备重铬酸钾(
等杂质)制备重铬酸钾( )固体的工艺流程如下:
)固体的工艺流程如下:
 遇水强烈水解。
遇水强烈水解。 橙色
橙色 绿色
绿色 元素的化合价是。
元素的化合价是。 等可溶性盐,滤渣1为红褐色固体,写出步骤②
等可溶性盐,滤渣1为红褐色固体,写出步骤② 配成
配成 溶液,取出
溶液,取出 于锥形瓶中,加入足量稀
于锥形瓶中,加入足量稀 和碘化钾溶液(
和碘化钾溶液( , 然后加入
, 然后加入 水和淀粉指示剂,用
水和淀粉指示剂,用 标准溶液滴定(
标准溶液滴定( ),至滴定终点消耗标准液
),至滴定终点消耗标准液 , 则所得产品中重铬酸钾的纯度:。(滴定过程中其他杂质不参与反应)
, 则所得产品中重铬酸钾的纯度:。(滴定过程中其他杂质不参与反应)



 后溶液颜色与实验II试管中颜色几乎相同
后溶液颜色与实验II试管中颜色几乎相同 ;
; 。某研究小组以黄铜矿为原料进行如下实验。
。某研究小组以黄铜矿为原料进行如下实验。
 矿样与足量
矿样与足量 混合,以氨气为载气,在1250℃左右高温炉中加热,将产生的
混合,以氨气为载气,在1250℃左右高温炉中加热,将产生的 气体用含淀粉的溶液吸收,同时用
气体用含淀粉的溶液吸收,同时用 的
的 标准溶液缓慢滴定(还原产物为碘离子)。装置如图所示(Sn的+4价化合物比+2价稳定)。
标准溶液缓慢滴定(还原产物为碘离子)。装置如图所示(Sn的+4价化合物比+2价稳定)。
 的作用是。
的作用是。
 的流程如下(已知
的流程如下(已知 难溶于水):
难溶于水):
 还原(硫元素被氧化为
还原(硫元素被氧化为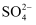 ),则对应反应的离子方程式为。
),则对应反应的离子方程式为。


