高考二轮复习知识点:性质实验方案的设计3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 | |||||||||||||||
|
下列相关实验方案正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 2. 单选题 | 详细信息 | |||||||||||||||
|
利用下列选项中提供的仪器(夹持仪器、部分试剂省略),能完成对应实验的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 3. 多选题 | 详细信息 | ||||||||||||||||||||
|
下列方案设计、现象和结论都正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 4. 单选题 | 详细信息 |
|
向碘水、淀粉的混合液中加入AgNO3溶液,蓝色褪去。为探究褪色原因,实验过程如图。下列分析错误的是( )
A . 过程①后溶液pH明显变小
B . 过程③中加入NaCl溶液的目的是除去Ag+
C . 过程④中氧化I-的物质不只有O2
D . 综合上述实验,过程①中蓝色褪去的原因是Ag+氧化了I2
|
|
| 5. 单选题 | 详细信息 | |||||||||||||||
|
下列实验现象与实验操作不相匹配的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 6. 单选题 | 详细信息 | |||||||||||||||
|
下列实验操作一定能达到实验目的的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 7. 单选题 | 详细信息 | |||||||||||||||
|
下列实验方案能达到相应实验目的的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 8. 单选题 | 详细信息 |
|
实验I和实验II中,均有气体产生。
下列分析错误的是( )
A . NaHSO3溶液中:c(SO
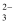 )>c(H2SO3)
B . I中有CO2生成
C . II中产生白色沉淀
D . I和II中溶液的pH均增大 )>c(H2SO3)
B . I中有CO2生成
C . II中产生白色沉淀
D . I和II中溶液的pH均增大
|
|
| 9. 实验探究题 | 详细信息 |
|
在处理NO废气的过程中,催化剂[Co(NH3)6]2+会逐渐失活变为[Co(NH3)6]3+。某小组为解决这一问题,实验研究
 和 和  之间的相互转化。 之间的相互转化。 资料:i.Ksp[Co(OH)2]=5.9×10-15 , Ksp[Co(OH)3]=1.6×10-44 ii.Co2++6NH3 Co3++6NH3 iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH
|
|
| 10. 实验探究题 | 详细信息 | ||||||||||||||||
|
某化学实验小组探究
 与 与  溶液的反应。 溶液的反应。
|
|||||||||||||||||
- 人教版化学高二选修6第四单元实验4-3含氯消毒液性质、作用的探究同步练习
- 浙江省衢州市2019-2020学年高一下学期化学期末考试试卷
- 2015-2016学年四川省眉山中学高二下学期期中化学试卷
- 2017_2018学年高中化学人教版选修四 第四章电化学基础4.3.1电解池
- 2015-2016学年河北省邯郸市曲周一中高二下学期期末化学试卷
- 山东省烟台市2017-2018学年高一下学期化学期末考试试卷
- 吉林省长春市普通高中2019-2020学年高三上学期化学期末考试试卷
- 2016-2017学年天津市红桥区高一下学期期中化学试卷
- 2018年高考化学真题试卷(海南卷)
- 高中化学人教版(2019)选择性必修1第三章第一节电离平衡
- 吉林省吉林市2020年高考理综-化学三模试卷
- 2015-2016学年广东省广州市番禹区仲元中学高一下学期期末化学试卷(文科)
- 甲看见路边的树向北运动, 乙看到甲静止不动, 如果以地面为参照物, 则乙是向 运动.
- 俄罗斯文豪屠格列夫曾遇见一个乞丐,他很想有所施舍,但他翻遍所有的口袋却没找到一分钱。见乞丐高高地举着脏兮兮的手,他上前一
- 下列关于我国地理环境的叙述,错误的是()A.我国大部分地区位于北温带B.我国是一个海陆兼备的国家C.中国领土最北端在黑龙
- (2012·齐齐哈尔) 洋务运动和明治维新都发生在19世纪60年代,比较它们的相同点是( ) A.都使本国迅速强大
- .在菱形ABCD中,∠BAD=,E为对角线AC上的一点(不与A,C重合),将射线EB绕点E顺时针旋转角之后,所得射线与直
- 某产品的总成本y(万元)与产量x(台)之间的函数关系是y=3 000+20x-0.1x2(0<x<240,x∈N),若每
- 在屈肘动作中起牵动作用的结构是 A.关节 B.皮肤 C.神经
- 阅读下面的文字,完成14―17题辋川尚静朱鸿辋川是一个长长的峡谷,王维曾经在这里居住。辋川确实很静,一条河流,两岸青山,
- .把CO2通入下列饱和溶液中,最终会有沉淀的是A.CaCl2 B.Na2CO3C.Ca(OH)2D.NaHCO3
- 生活在一个池塘内的藻类、水蚤、鱼虾及淤泥中的细菌和真菌,在生态学上叫做( ) A.种群 B.生物群落 C.
- 如图所示,光滑曲线导轨足够长,固定在绝缘斜面上,匀强磁场B垂直斜面向上.一导体棒从某处以初速度v0沿导轨面向上滑动,最后
- 如图(16)所示是某种物质熔化时温度随时间变化的图象,根据该图象可判断出这种物质一定是 (填“晶体
- 下图所示是第二次世界大战期间美国的战争宣传海报,主题是“全力以赴,摧毁日本”,它最早可能出现于( ) A.1941年
- 读图,回答问题。(6分)(1)马六甲海峡地处_____________地区(亚洲分区)。图中B表示__________洋
- 将一个长方体内部挖去一个圆柱(如图所示),它的主视图是
- 已知:药品名称 熔点/℃ 沸点(℃) 密度g/cm3 溶解性 正丁醇 -89.5 117.7 0.8098 微溶于水、溶
- 请回答下列有关生命科学实验的问题。 (1)颤藻和水绵细胞的比较观察实验,下图中甲生物是 ,用碘液试剂对其细胞进
- 如图所示,重为100N的物体B,在足够深的水中匀速下沉,通过滑轮组拉着重600N的物体A沿水平方向匀速运动,在4s内物体
- 下列各组词语中,没有错别字的一组是 A.精湛 金鸾殿 顺藤摸瓜 竹篮打水一场空 B.聚拢 滑稽戏 愤笔疾书
- 设函数,则 A. 为的极大值点 B.为的极小值点 C. 为的极大值点 D. 为的极小值点
 的
的 溶液
溶液 溶于100mL水中并充分搅拌
溶于100mL水中并充分搅拌 有还原性
有还原性 溶液中滴加少量
溶液中滴加少量 溶液,观察紫色是否变浅
溶液,观察紫色是否变浅 、
、 溶液的pH,通过pH的大小判断
溶液的pH,通过pH的大小判断 溶液,观察是否有气体逸出
溶液,观察是否有气体逸出

 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105


 CoCl2
CoCl2  Co(OH)2
Co(OH)2
 于试管中,滴入几滴血红色溶液,溶液的紫色褪去,据此推断血红色溶液中含有Fe2+。此结论(填“正确”、“不正确”),理由是。
于试管中,滴入几滴血红色溶液,溶液的紫色褪去,据此推断血红色溶液中含有Fe2+。此结论(填“正确”、“不正确”),理由是。
 )或c(
)或c(  )有关
)有关 的关系如图所示。(已知吸光度越大,溶液颜色越深)。
的关系如图所示。(已知吸光度越大,溶液颜色越深)。



