高考二轮复习知识点:化学电源新型电池3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 填空题 | 详细信息 |
|
某液氨﹣液氧燃料电池示意图如上,该燃料电池的工作效率为50%,现用作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液中NaOH的浓度为0.3mol•L﹣1 , 则该过程中需要氨气的质量为g(假设溶液电解后体积不变).
|
|
| 2. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||||||||||
|
煤是一种重要的化工原料,人们将利用煤制取的水煤气、焦炭、甲醚等广泛用于工农业生产中.
|
|||||||||||||||||||||||||||||||||||||
| 3. 单选题 | 详细信息 |
|
金属(M)﹣空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n , 已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )
A . 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B . 比较Mg,Al,Zn三种金属﹣空气电池,Al﹣空气电池的理论比能量最高
C . M﹣空气电池放电过程的正极反应式:4M++nO2+2nH2O+4ne﹣=4M(OH)n
D . 在Mg﹣空气电池中,为防止负极区沉积Mg(OH)2 , 宜采用中性电解质及阳离子交换膜
|
|
| 4. 单选题 | 详细信息 |
|
锌﹣空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH﹣+2H2O═2Zn(OH)42﹣ . 下列说法正确的是( )
A . 充电时,电解质溶液中K+向阳极移动
B . 充电时,电解质溶液中c(OH﹣)逐渐减小
C . 放电时,负极反应为:Zn+4OH﹣﹣2e﹣═Zn(OH)42﹣
D . 放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
|
|
| 5. 单选题 | 详细信息 |
|
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42﹣可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( )
A . 通电后中间隔室的SO42﹣离子向正极迁移,正极区溶液pH增大
B . 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C . 负极反应为2H2O﹣4e﹣=O2+4H+ , 负极区溶液pH降低
D . 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
|
|
| 6. 综合题 | 详细信息 | ||||||||||||||||||||||||||||||||
|
“低碳循环”已引起各国家的高度重视,而如何降低大气中CO2的含量和有效地开发利用CO2正成为化学家研究的主要课题.
|
|||||||||||||||||||||||||||||||||
| 7. 实验探究题 | 详细信息 | |||||||||||||||||||||
|
工业上产生的氮氧化物可用天然气来处理.
|
||||||||||||||||||||||
| 8. 综合题 | 详细信息 |
|
肼(N2H4)是一种高能燃料,在工业生产中用途广泛.
|
|
| 9. 综合题 | 详细信息 | |||||||||||||||||||||
|
碳及其化合物应用广泛.
I.工业上利用CO和水在沸石分子筛表面反应制氢气,CO(g)+H2O(g)⇌CO2(g)+H2(g)
|
||||||||||||||||||||||
| 10. 多选题 | 详细信息 |
|
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2 , 可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )
A . 电池放电时Na+从a极区移向b极区
B . 电极a采用MnO2 , 放电时它被还原
C . 该电池负极的电极反应式为:BH4﹣+8OH﹣﹣8e﹣═BO2﹣+6H2O
D . 放电时,a极区的电极反应生成碱,碱性增强
|
|
- 人教版化学高二选修3第一章第二节原子结构与元素的性质同步练习
- 黑龙江省齐齐哈尔市2017-2018学年高考理综-化学一模考试试卷
- 2015-2016学年江苏省盐城市建湖二中高一下学期期中化学试卷
- 备考2019年高考化学二轮专题 04 离子反应
- 新疆昌吉市教育共同体四校2017-2018学年高二下学期化学期末考试试卷
- 2016-2017学年江苏省扬中、六合、句容、省溧、中华、江浦、华罗庚七校联考高三上学期期中化学试卷
- 2016-2017学年福建省福州市八县一中联考高二上学期期中化学试卷
- 2016-2017学年江西省吉安三中高二上学期期中化学试卷
- 2018年高考化学真题试卷(江苏卷)
- 吉林省蛟河市朝鲜族中学校2019-2020学年高二上学期化学期中考试试卷
- 浙江省“七彩阳光”新高考研究联盟2017-2018学年高一上学期化学期中考试试卷
- 陕西省榆林市2020年高考理综-化学3月线上模拟试卷
- 有性生殖的生物产生后代需进行受精作用,植物体细胞杂交要进行原生质体的融合, 单克隆抗体的制备需进行动物细胞融合,可见细胞
- 细胞内无机盐的作用不包括()A. 调节生命活动 B. 维持酸碱平衡 C. 组成某些化合物 D. 提供营养
- 魏晋南北朝时期至唐代,佛教盛行所造成的后果有 ①麻痹了人民,一定程度上避免了社会矛盾的激化②佛教建筑——石窟艺术得到发展
- 如图是某几何体的三视图,则该几何体是()A.长方体 B.正方体 C.圆柱
- 造成东西方经济差距日益拉大,并最终使东方从属于西方的基本原因有() ①科学技术水平进步 ②资产阶级革命成③无产阶级革命受
- 一定温度下,在恒容密闭容器中进行可逆反应2NO2(g) ⇌2NO(g) + O2(g),下列可以作为反应达到化学平衡状态
- 某个命题与自然数n有关,若n=k(k∈N*)时该命题成立,那么可推得n=k+1时该命题也成立,现已知当n=5时该命题不成
- 正常情况下,将成熟的花粉粒离体培养成单倍体植株幼苗时,细胞内不可能出现的是( ) A.染色单体形成 B.染
- 读下图,完成1-3题。1.图中天体M可能是()
- (10分)在12m高的塔上,以一定的初速度竖直上抛一物体,经2s到达地面,则:(1)物体抛出时的速度为多大?(2)物体落
- Please give us a ______ explanation ____ why you have done s
- 有4盏电灯,如图所示连接在电路中,L1,L2都标有“220V,100W”的字样,L3,L4都标有“220V,40W”的字
- 如图,在ΔABC中,AB=30,BC=24,CA=27, AE=EF=FB,EG∥FD∥BC,FM∥EN∥AC,则图中
- 《马关条约》签订后,列强对华经济侵略进入一个新阶段。这主要体现在()。 A.列强强迫清政府承担巨额赔款
- 用天平和量筒测定金属块的密度将托盘天平放在水平桌面上,游码放在天平标尺的零刻线处,调节天平横梁的平衡。在调节天平横梁平衡
- 2015年恰逢新疆维吾尔族自治区成立60周年。60年来,新疆发生了翻天覆地的变化。1955年新疆生产总值仅为12亿元,2
- 某同学在学校感到自卑,影响了生活和学习。老师开导他,如果只看到自己的缺陷和不足,就会产生消极情绪,我们要善于挖掘自身优势
- 下列叙述正确的是( ) A.1个甘氨酸分子中存在9对共用电子 B.PCl3和了BCl3分子中所有原子的最外层都达到
- 阅读表达 阅读短文,按要求完成短文后的各项任务。 Around the world, people have d
- 下图1是测量神经纤维膜内外电位的装置,图2是测得的膜电位变化。下列有关叙述错误的是:A.图1中A能测出静息电位的大小,相




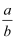 的值(填具体值或取值范围).
的值(填具体值或取值范围).
 O2(g)=CO2(g)△H1=﹣141kJ•mol﹣1
O2(g)=CO2(g)△H1=﹣141kJ•mol﹣1 O2(g)=CO2(g)+2H2O(g)△H3=﹣726kJ•mol﹣1
O2(g)=CO2(g)+2H2O(g)△H3=﹣726kJ•mol﹣1




