高考二轮复习知识点:氧化性、还原性强弱的比较2
高考二轮复习知识点:氧化性、还原性强弱的比较2
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 | ||||||||||||||||||||
|
由下列实验及现象不能推出相应结论的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 2. 综合题 | 详细信息 |
|
水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
|
|
| 3. 多选题 | 详细信息 |
|
钒元素在酸性溶液中有多种存在形式,其中VO2+为蓝色,VO
 为淡黄色,VO 为淡黄色,VO  具有较强的氧化性。Fe2+、SO 具有较强的氧化性。Fe2+、SO 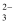 等能把VO 等能把VO  还原为VO2+。向VOSO4溶液中滴加酸性KMnO4溶液,溶液颜色由蓝色变为淡黄色。下列说法正确的是( ) 还原为VO2+。向VOSO4溶液中滴加酸性KMnO4溶液,溶液颜色由蓝色变为淡黄色。下列说法正确的是( )
A . 在酸性溶液中氧化性:MnO
 >VO2+>Fe3+
B . 亚硫酸钠溶液与酸性(VO2)2SO4溶液发生反应:2VO >VO2+>Fe3+
B . 亚硫酸钠溶液与酸性(VO2)2SO4溶液发生反应:2VO  +2H++SO +2H++SO 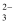 =2VO2++SO =2VO2++SO  +H2O
C . 向VOSO4溶液中滴加酸性KMnO4溶液反应化学方程式为:10VOSO4+2H2O+2KMnO4=5(VO2)2SO4+2MnSO4+2H2SO4+K2SO4
D . 向含1mol VO +H2O
C . 向VOSO4溶液中滴加酸性KMnO4溶液反应化学方程式为:10VOSO4+2H2O+2KMnO4=5(VO2)2SO4+2MnSO4+2H2SO4+K2SO4
D . 向含1mol VO  的酸性溶液中滴加含1.5 mol Fe2+的溶液完全反应,转移电子为1.5mol 的酸性溶液中滴加含1.5 mol Fe2+的溶液完全反应,转移电子为1.5mol
|
|
| 4. 综合题 | 详细信息 |
|
|
| 5. 单选题 | 详细信息 |
|
向CuSO4溶液中加入H2O2溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊(Cu2O),继续加入H2O2溶液,红色浑浊又变为蓝色溶液,这个反应可以反复多次。下列关于上述过程的说法错误的是( )
A . Cu2+将H2O2还原为O2
B . H2O2既表现氧化性又表现还原性
C . Cu2+是H2O2分解反应的催化剂
D . 发生了反应Cu2O+H2O2+4H+═2Cu2++3H2O
|
|
| 6. 综合题 | 详细信息 |
|
钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
|
|
| 7. 单选题 | 详细信息 |
|
硝酸厂的尾气中含有大量的氮氧化物(NOx),将尾气与H2混合,通入Ce(SO4)2与Ce2(SO4)3的混合溶液中实现无害化处理,其转化过程如图所示。下列说法正确的是( )
A . 该转化过程的实质为NOx被H2还原
B . 过程I发生反应的离子方程式:H2+Ce4+=2H++Ce3+
C . 处理过程中,混合溶液中Ce3+和Ce4+总数减少
D . x=1时,过程II中氧化剂与还原剂的物质的量之比为2:1
|
|
| 8. 单选题 | 详细信息 |
|
对于铝和烧碱溶液的反应,下列说法错误的是( )
A . 铝是还原剂
B .
 是氧化剂
C . 是氧化剂
C .  与 与  是氧化剂
D . 氢气是还原产物 是氧化剂
D . 氢气是还原产物
|
|
| 9. 单选题 | 详细信息 |
|
I-具有还原性,含碘食盐中的碘元素以KIO3的形式存在,I-、I2、IO
 在一定条件下可以发生如图转化关系,下列说法错误的是( ) 在一定条件下可以发生如图转化关系,下列说法错误的是( )
A . 由图可知氧化性的强弱顺序为Cl2 > IO
 > I2
B . 用淀粉碘化钾试纸和白醋可检验食盐是否加碘
C . 生产等量的碘,反应①和反应②转移电子数目之比为2∶5
D . 反应③的离子方程式:3Cl2+ I-+3H2O →6Cl- + IO > I2
B . 用淀粉碘化钾试纸和白醋可检验食盐是否加碘
C . 生产等量的碘,反应①和反应②转移电子数目之比为2∶5
D . 反应③的离子方程式:3Cl2+ I-+3H2O →6Cl- + IO  +6H+ +6H+
|
|
| 10. 单选题 | 详细信息 |
|
为防止废弃的硒单质(Se)造成环境污染,通常用浓硫酸将其转化成SeO2 , 再用KI溶液处理后回收Se。发生反应:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;②SeO2+4KI+4HNO3=4KNO3+Se+2I2+2H2O,下列说法正确的是( )
A . ①中SO2是氧化产物,SeO2是还原产物
B . ②中HNO3是氧化剂,KI是还原剂
C . 由①②可知浓硫酸能将KI氧化生成I2
D . 由①②可知还原性由强到弱的顺序:Se>KI>SO2
|
|
高中化学 试卷推荐
- 辽宁省锦州市2018-2019学年高二下学期化学期末考试试卷
- 四川省资阳市2016-2017学年高二上学期化学期末考试试卷
- 云南省保山市2017-2018学年高考理综-化学一模考试试卷
- 2015-2016学年安徽省黄山市高一上学期期末化学试卷
- 2016-2017学年河南省洛阳市高三上学期期中化学试卷
- 浙江省绍兴蕺山外国语学校2019-2020学年高一下学期化学期中考试试卷
- 江苏省苏州市第十中学2017-2018学年高一上学期化学期末考试试卷
- 北京市西城区2017-2018学年高一下学期化学期末考试试卷
- 高中化学人教版(2019)选择性必修1 第四章第二节 电解池
- 2016年北京市高考化学模拟试卷(3月份)
- 江苏省徐州市2016-2017学年高二上学期化学期末考试试卷
- 2016年江西省宜春市万载二中高考化学一模试卷
最近更新
- 下列各句中,加点的词语运用错误的一项是 A.2010年以来世界各地的活火山相继喷发,先是冰岛火山狂喷,后是印尼、日本等地
- 已知A为澄清溶液,焰色反应透过蓝色钴玻璃为紫色,C难溶于水(1)试推断(写化学式):A B
- 下列有关“叶绿体色素的提取和分离”的实验叙述正确的是 A.加入碳酸钙防止滤液挥发
- 某校高三一班有学生54人,二班有学生42人,现在要用分层抽样的方法从两个班抽出16人参加军训表演,则一班和二班分别被抽取
- 下图为植物组织培养的基本过程,则制作人工种子,及生产治疗烫伤、割伤的药物——紫草素,应分别选用编号:A.④② B
- 清代统治者能够正确处理各民族之间的关系,这主要表现在
- Mary wanted to travel around the world all by herself, but h
- 下列词语中加点字的读音完全正确的一项是( ) A、炽热 (zhì) 阴霾 (mái) 琐屑 (xiāo)
- 2010年是我国的“扩大开放年”,也是我国中西部地区承接东南部沿海地区产业转移的机遇期。结合下表,回答16-17题: 目
- 围绕以下《外交大事记》的一块展板,四位同学展开讨论,其中观点正确的是( )外交大事记 1981年底,中国明确表示肯
- 文学类文本阅读西拉沐伦河漂流张抗抗西拉沐伦河来自兴安岭南端的湟源河谷,为商代先民的摇篮。据说湟源的沙丘若垄似链,形成盆地
- 当前,气候变化已成为国际社会国别合作与博弈的焦点。发达国家以应对气候变化的重大挑战为契机,加大技术创新投入,以便在未来的
- 下列7种化学符号: 18O;14C;23Na;14N;32S; 16O; 1H2 (1)表示核素的符号共_
- 下列图形中,既是轴对称图形又是中心对称图形的是() A. B.
- (3分)在利用重锤下落验证机械能守恒定律的实验中正确的是 A.应该用天平称出重锤的质量B.应该选用点迹清晰,第一
- 设函数,将的图像向右平移个单位长度后,所得的图像与原图像重合,则的最小值等于 A. B.
- 决定元素种类的是( ) A.电子数 B.质子数 C.中子数 D.最外层电子数
- 下列有关分离提纯的说法正确的是A.用浓溴水除去苯中混有的苯酚B.用重结晶的方法提纯苯甲酸C.用分液的方法分离乙酸和乙酸乙
- 在下列物理现象或者物理过程中,机械能守恒的是( ) A.匀速下落的降落伞
- 某校对学生课外活动内容进行调查,结果整理成下表: 性别 课外活动内容 合计 体育 文娱 男生 21 23 44 女生 6


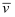 (a)=kPa·min−1。467 ℃时PH2和PCO随时间变化关系的曲线分别是、。489 ℃时PH2和PCO随时间变化关系的曲线分别是、。
(a)=kPa·min−1。467 ℃时PH2和PCO随时间变化关系的曲线分别是、。489 ℃时PH2和PCO随时间变化关系的曲线分别是、。 +VO2++=Cl-+VO
+VO2++=Cl-+VO  +
+ 、Cl-、VO2+还原性由大到小的顺序是。
、Cl-、VO2+还原性由大到小的顺序是。
 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 。
溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 。 




