【备考2024年】从巩固到提高 高考化学二轮微专题10 元素周期律
【备考2024年】从巩固到提高 高考化学二轮微专题10 元素周期律
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
A,B,C,D,E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
|
|
| 2. 综合题 | 详细信息 |
|
已知①~⑩号元素在周期表中的位置如图。试回答下列问题:
|
|
| 3. 综合题 | 详细信息 |
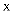 、 、  、 、  、 、  、 、  五种元素的原子序数依次递增。已知:① 五种元素的原子序数依次递增。已知:①  位于周期表中第四周期 位于周期表中第四周期  族,其余的均为短周期主族元素:② 族,其余的均为短周期主族元素:②  的氧化物是光导纤维的主要成分;③ 的氧化物是光导纤维的主要成分;③  原子核外 原子核外  层电子数为奇数;④ 层电子数为奇数;④ 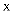 是形成化合物种类最多的元素;⑤ 是形成化合物种类最多的元素;⑤  原子 原子 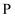 轨道的电子数为4。请回答下列问题: 轨道的电子数为4。请回答下列问题:
|
|
| 4. 综合题 | 详细信息 |
|
A、B、C、D、E、F、G是原子序数依次增大的短周期主族元素,A的原子核内无中子,B、F在元素周期表中的相对位置如图,B与氧元素能形成两种无色气体,D是地壳中含量最多的元素,E是地壳中含量最多的金属元素。
|
|
| 5. 综合题 | 详细信息 |
|
已知A、B、C、D、E、F为前4周期的6种元素,原子序数依次增大,其中A位于周期表中s区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn , B和E同主族,D原子的最外层电子数是其内层电子数的3倍;F元素位于元素周期表的第4行、第11列。试回答下列问题:
|
|
| 6. 推断题 | 详细信息 |
|
有八种短周期主族元素
 ,其中 ,其中  随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。 随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。  的最高价氧化物对应水化物溶液(浓度均为 的最高价氧化物对应水化物溶液(浓度均为  )的 )的  与原子序数的关系如图2所示。 与原子序数的关系如图2所示。 根据上述信息回答下列问题:
|
|
| 7. 综合题 | 详细信息 |
|
化学工业为疫情防控提供了强有力的物质支撑。氯及其化合物既是重要化工原料,又是广泛使用的高效灭菌消毒剂。回答下列问题:
|
|
| 8. 综合题 | 详细信息 |
|
有8种短周期主族元素x、y、z、d、e、f、g、h,其中x、y、d、f随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示,z、e、g、h的最高价氧化物对应水化物溶液(浓度均为0.01mol/L)的pH与原子序数的关系如图2所示。
根据判断出的元素回答下列问题:
|
|
| 9. 综合题 | 详细信息 |
|
一种新型漂白剂(结构如图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,Z原子的核外电子排布为1s1 , W、Y、Z的最外层电子数之和等于X的最外层电子数,X基态原子核外有两个单电子,W、X对应的简单离子核外电子排布相同。
回答下列问题:
|
|
| 10. 综合题 | 详细信息 | ||||||||||||||
|
如图是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
试回答下列问题。
|
|||||||||||||||
高中化学 试卷推荐
- 湖南省五市十校2020-2021学年下学期高一期末联考化学试题
- 辽宁省名校联盟2021-2022学年高一3月联合考试化学试题
- 广东省汕头市2021-2022学年高三上学期期末教学质量监测化学试题
- 新疆乌鲁木齐地区2021年高考化学一模试卷
- 广东省汕尾市2020-2021学年高二上学期化学期末考试试卷
- 河南名校联盟2021-2022学年高二上学期期末考试化学试题
- 湖南省衡阳市2021-2022学年高一下学期期中考试化学试题
- 备考2021年高考化学二轮专题 第8讲 电化学原理及应用
- 河北省沧州市2021年高考化学三模试卷
- 北京一零一中学2020-2021学年高一上学期化学期中考试试卷
- 安徽省黄山市2021年高考化学二模试卷
- 江苏省扬州市2020-2021学年高三下学期化学开学考试试卷
最近更新
- 李华准备到外企求职,必须具备一定的英语水平。请发e-mail告知他学英语的方法。 提示:1. 养成良好的学习英语习惯(如
- (2019·天津)阅读《母亲的刺绣时光》一文,回答问题。 母亲的刺绣时光 宫 佳 ①母亲是一个心灵手巧的人,一针一线,
- 下图表示森林生态系统中碳循环的部分过程,其中甲、乙、丙、丁构成生态系统的生物群落,箭头表示物质循环的方向。下列有关叙述错
- 如图2所示的四个实例中,目的是为了减小摩擦的是
- 下列关于西双版纳的说法,正确的有:() A.景区到昆明及邻国的交通方式以铁路为主 B.近年来其旅游业发展呈直线上升趋势
- 如图所示,在真空中把一绝缘导体向带负电的小球P缓缓靠近(不相碰),下列说法中正确的是 A.B端的感应电荷越来越多B
- 硒(Se)是人体中的微量元素,有防癌抗癌作用。饮用含适量硒的矿泉水有益于人体健康。有一种硒的氧化物,化学式为SeO3,其
- 阅读下列各段文言文,完成文后相应的题目 刘义隆将王玄谟寇滑台,诏假慧龙楚兵将军,与安颉等同讨之。相持五十余日,诸将以贼盛
- 实验室制取Fe(OH)3胶体的方法是:向盛有沸水的小烧杯中滴加FeCl3饱和溶液1ml~2ml,待溶液呈红褐色后停止加热
- 如果,则下列不等式中,不成立的是( ) A. B. C. D.
- 函数f(x)=cos4x,x∈R是 A.最小正周期为π的偶函数 B.最小正周期为π的
- 提取下面一段话的主要信息,在方框内写出四个关键词。(4分)新浪科技讯:近日,美国科学家宣布,他们在撒哈拉沙漠中发掘到一个
- “朕欲革去中书省,升六部,仿古六卿之制,俾之各司所事。……如此,权不专于一司,事不留于壅蔽,卿等以为如何?”材料中的“朕
- 下列四图中,表示北半球近地面风向的是(以下单位为百帕)
- His determination and devotion to science _____ the great di
- 某有机样品3.1g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g,经过滤得到10g沉淀。该有机样品可
- 23.仿照下面的示例,自选话题,另写两句话,要求内容贴切,句式与示例相同。(5分) 一朵鲜花点缀不出绚丽的春天,万紫千红
- 图示区域时常发生季节性洪水灾害,其特征为“一日一峰”,白天流量很大,夜晚洪峰消退。读图回答问题。(1)分析该区域季节性洪
- .莫里循是澳大利亚人,曾任《泰晤士报》驻华首席记者,中华民国总统政治顾问。他居住北京达20余年(1887-1920年),
- 船在流水中,在甲地和乙地间来回行驶一次的平均速度和船在静水中的速度是否相等,为什么?


 晶胞中(结构如图所示)所包含的
晶胞中(结构如图所示)所包含的 
 的空轨道接受
的空轨道接受  的氮原子提供的形成配位键。
的氮原子提供的形成配位键。
 是(写名称),
是(写名称),  分子中
分子中  键的数目为
键的数目为  。
。



 的简单离子半径大小为<<(用离子符号表示);
的简单离子半径大小为<<(用离子符号表示);  的最高价氧化物对应的水化物酸性较强的是(用化学式表示)。
的最高价氧化物对应的水化物酸性较强的是(用化学式表示)。
 组成的剧毒化合物
组成的剧毒化合物  不慎泄露时,通常用过氧化氢溶液处理,以减少污染,反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,该反应的化学方程式为。
不慎泄露时,通常用过氧化氢溶液处理,以减少污染,反应生成一种酸式盐和一种气体,二者溶于水均呈碱性,该反应的化学方程式为。


 ]氧化为葡萄糖酸[
]氧化为葡萄糖酸[  ],进而制取葡萄糖酸锌,装置如图所示。
],进而制取葡萄糖酸锌,装置如图所示。







