理综化学7+4二轮专题复习卷 专题二 离子反应
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 | ||||||||||||
|
硫酸锌(
 )是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用.硫酸锌可由菱锌矿制备.菱锌矿的主要成分为 )是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用.硫酸锌可由菱锌矿制备.菱锌矿的主要成分为 , 杂质为 , 杂质为 以及 以及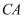 、 、 、 、 、 、 等的化合物.其制备流程如下: 等的化合物.其制备流程如下:
本题中所涉及离子的氯氧化物溶度积常数如下表:
回答下列问题:
|
|||||||||||||
| 2. 单选题 | 详细信息 |
|
铍是航天、航空、电子和核工业等领域不可替代的材料,有“超级金属”之称。以绿柱石[
 ]为原料制备金属铍的工艺如下: ]为原料制备金属铍的工艺如下:
已知:750℃烧结时,
A . 提高烧结后的水浸效率可以将烧结固体粉碎处理
B . 对过滤1后的滤液中加入过量的NaOH溶液有利于Be元素的沉淀
C . “沉氟”反应的离子方程式为
 D . 工业上电解
D . 工业上电解 熔融混合物制备金属铍,在阳极析出金属铍 熔融混合物制备金属铍,在阳极析出金属铍
|
|
| 3. 单选题 | 详细信息 |
|
海带中含有丰富的碘元素,某化学兴趣小组设计的海带提碘实验流程如下图,下列说法中正确的是( )
A . 上述流程中各步操作用到的仪器包括:
 B . “氧化”时,试剂可选用O2、H2O2或Br2
C . 上述流程包括三个氧化还原反应和三种分离操作
D . “反萃取”时,反应的离子方程式为I2+2OH-=I-+IO
B . “氧化”时,试剂可选用O2、H2O2或Br2
C . 上述流程包括三个氧化还原反应和三种分离操作
D . “反萃取”时,反应的离子方程式为I2+2OH-=I-+IO +H2O +H2O
|
|
| 4. 单选题 | 详细信息 |
|
钒元素用途广泛,如图是一种钒的化合物催化某反应的反应机理。下列叙述错误的是( )
A .
 是该反应的催化剂
B . 过程①②④中反应的原子利用率为100%
C . 该催化循环中V的成键数目发生变化
D . 该反应的离子方程式为:H2O2+Cl-+ H+= HOCl+ H2O 是该反应的催化剂
B . 过程①②④中反应的原子利用率为100%
C . 该催化循环中V的成键数目发生变化
D . 该反应的离子方程式为:H2O2+Cl-+ H+= HOCl+ H2O
|
|
| 5. 单选题 | 详细信息 |
|
下列各组离子在给定溶液中能大量共存的是( )
A . 在
 氨水中: 氨水中: B . 在
B . 在 氯化钠溶液中: 氯化钠溶液中: C . 在
C . 在 醋酸溶液中: 醋酸溶液中: D . 在
D . 在 硝酸银溶液中: 硝酸银溶液中:
|
|
| 6. 单选题 | 详细信息 |
|
下列判断正确的是( )
A . 加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不溶解,可确定原溶液中有Cl-存在
B . 加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可确定原溶液中有CO32-存在
C . 加入稀盐酸酸化的BaCl2溶液,生成白色沉淀,可确定原溶液中有SO42-存在
D . 通入Cl2后,溶液由无色变为深黄色,加入淀粉溶液后,溶液变蓝,可确定原溶液中有I-存在
|
|
| 7. 单选题 | 详细信息 |
|
宏观辨识与微观探析是化学学科核心素养之一、下列关于含N化合物的物质性质实验对应的反应方程式书写错误的是( )
A . 将过量氨气通入氯化铝溶液中:
 B . 用浓氨水检验氯气管道是否泄漏:
B . 用浓氨水检验氯气管道是否泄漏: C . 温度升高气体颜色加深:
C . 温度升高气体颜色加深:  D .
D .  溶液显碱性: 溶液显碱性:
|
|
| 8. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||||||||||
|
碘化钾常用作合成有机化合物的原料。某实验小组设计实验探究KI的还原性。
|
|||||||||||||||||||||||||||||||||||||
| 9. 综合题 | 详细信息 | |||||||||||||||
|
某炉渣主要成分有
 、 、 、 、 、MgO、CaO以及少量的 、MgO、CaO以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
已知:“焙烧”中,
回答下列问题:
|
||||||||||||||||
| 10. 综合题 | 详细信息 | ||||||||||||||
|
随着人们对晒的性质深入认识及产品硒的纯度提高,硒的应用范围越来越广。某科学小组以含硒物料(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)为原料提取硒,设计的流程如图:
回答下列问题:
|
|||||||||||||||
- 山东省潍坊市2020年高考化学一模试卷
- 2016年江西省宜春市樟树市高考化学四模试卷
- 浙江省宁波市2020年高考化学二模试卷
- 内蒙古包头市包钢四中2015-2016学年高一上学期化学期末考试试卷
- 江苏省南京市2020年高考化学三模试卷
- 人教高中化学一轮复习:专题15实验设计与评价
- 高中化学人教版(新课标)必修1 第二章第一节 物质的分类
- 广东省梅州市梅州中学2019-2020学年高二下学期化学4月月考试卷
- 吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期化学期末考试试卷
- 黑龙江省佳木斯一中2019-2020学年高一上学期化学期末考试试卷
- 高中化学人教版(新课标)必修1 第四章第三节 硫和氮的氧化物
- 河南省驻马店市2019-2020学年高一下学期化学期末考试试卷
- 阅读下面一则材料,根据要求作文。(60分)诗人马丽华在藏北旅行,她借宿在苍姆决家。仓姆决家生活很苦。在这样的环境中借宿,
- 如图8-4-9所示,在光滑水平面上两平板车的质量分别为M1=2 kg和M2=3 kg,在M1的光滑表面上放有质量m=1
- 在2010年11月12日—17日广州举办的亚运会上,中国代表团势如破竹,共获得199枚金牌,以史上最高的金牌数为中国军团
- 尽管微博简短和情绪化的表达方式容易成为谣言滋生的温床,给公众与社会和谐带来不少困扰,但如果能加强管理,完善法制,塑造良好
- 史书载:“汉初萧(何)曹(参)为相,镇以无为,从民之欲而不扰乱。”它反映汉初的统治思想是( ) A.儒家思想 B.法家思
- (甘肃省天水一中2009届高三最后一次模拟考试) My senior year of high school was
- 已知函数(a>0) (1)若0对任意的xR成立,求实数a的值, (2)在(1)的条件下,证明:
- 将2名教师,4名学生分成2个小组,分别安排到甲、乙两地参加社会实践活动,每个小组由1名教师和2名学生组成,不同的安排方案
- 下列生活用品所含的主要材料,属于有机合成材料的是 A.纯羊毛衫 B.塑料盆 C.不锈钢餐
- 下列各句中没有语病的一句是() A.河北省公安厅就三鹿牌婴幼儿配方奶粉重大安全事故有关调查侦办进展情况进行了通报,称已有
- 质量相等的A、B两物体,从等高处同时开始运动,A做自由落体运动,B做初速度为v0的平抛运动,不计空气阻力,则 (
- 中国隋唐科举制、雅典梭伦的财产等级制、罗马的万民法,其相似的作用是( ) A.拓宽了官吏选拔途径
- (2011年湖南怀化,13题)下列有关实验现象的描述中不正确的是A.木炭在氧气中燃烧发出白光B.细铁丝在氧气中剧烈燃烧,
- 这是一幅世界名画,画中人的微笑是世界上最迷人的微笑。它的作者是:A、拉斐尔 B、达·芬奇
- -- “What will you do during the summer holiday?”-- “I don’t
- (10分)质量相等的小球A、B分别固定在轻杆的中点及端点,当棒在光滑的水平面上绕O点匀速转动时,如图。求棒的OA段及AB
- (7分)反应A(g)+B(g) C(g) +D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列
- 已知定义在R上的函数是奇函数,当时,, 则当时,的表达式为_____________.
- 下列应用与盐类的水解无关的是A.纯碱溶液可去除油污 B.NaCl可用作防腐剂和调味剂C.TiCl4溶于
- 2002年6月6日,《海峡都市报》报道:“104国道设计使用年限为15年以上,但是才使用了5年就大修,现已伤痕累累”、有












 B.
B. C.
C.
 的滤液①中分批加入适量
的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有
溶液充分反应后过滤,滤渣②中有 , 该步反应的离子方程式为。
, 该步反应的离子方程式为。
 反应可以释放
反应可以释放 并循环利用,同时得到的副产物是、。
并循环利用,同时得到的副产物是、。

 与绿柱石作用生成易溶于水的
与绿柱石作用生成易溶于水的 , “滤渣1”中含有铁、铝、硅的氧化物,
, “滤渣1”中含有铁、铝、硅的氧化物, 可与过量
可与过量 结合成
结合成 。下列说法正确的是( )
。下列说法正确的是( )

 的KI溶液,需要称取KI的质量为g。
的KI溶液,需要称取KI的质量为g。


 溶液
溶液
 mL
mL


 ”为可逆反应。
”为可逆反应。 KI溶液,
KI溶液, 溶液,淀粉溶液,
溶液,淀粉溶液, 溶液,KSCN溶液。实验如下:
溶液,KSCN溶液。实验如下:





 )的pH
)的pH 。
。
 进入溶液,则
进入溶液,则 沉淀,该反应的离子方程式是。
沉淀,该反应的离子方程式是。


 , HSeO
, HSeO H++SeO
H++SeO 。已知0.01mol·L-1H2SeO4溶液的pH为x,则K(HSeO
。已知0.01mol·L-1H2SeO4溶液的pH为x,则K(HSeO


