高考二轮复习知识点:盐类水解的应用2
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 | |||||||||
|
以废旧锌锰电池中的黑锰粉(MnO2、MnO(OH)、NH4Cl、少量ZnCl2及炭黑、氧化铁等)为原料制备MnCl2 , 实现锰的再利用。其工作流程如下:
|
||||||||||
| 2. 综合题 | 详细信息 | |||||||||||||||
|
已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)中制备草酸镍晶体的流程如图所示:
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
②Ksp(CaF2)=1.46×10-10; ③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。 请回答下列问题:
|
||||||||||||||||
| 3. 综合题 | 详细信息 |
|
NaBH4是一种常见的还原剂。一种以H2、Na、硼酸三甲酯[B(OCH3)3]为原料,生产NaBH4的工艺流程如下:
|
|
| 4. 综合题 | 详细信息 |
|
研究含硒工业废水的处理工艺,对控制水体中硒超标具有重要意义。
|
|
| 5. 综合题 | 详细信息 |
|
一种固定烟气中CO2的工艺流程如下:
|
|
| 6. 综合题 | 详细信息 |
|
用磷铁渣(含Fe、FeP、Fe2P及少量杂质)制备FePO4·2H2O(磷酸铁)的工艺流程如下:
|
|
| 7. 多选题 | 详细信息 |
|
草酸(H2C2O4)是一种二元弱酸。室温时,下列指定溶液中微粒物质的量浓度关系正确的是( )
A . 0.1 mol·L−1 NaHC2O4溶液:c(Na+)>c(C2O
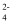 )>c(HC2O )>c(HC2O  )
B . 0.1 mol·L-1 Na2C2O4溶液:c(OH-) = c(H+) + 2c(H2C2O4) + c(HC2O )
B . 0.1 mol·L-1 Na2C2O4溶液:c(OH-) = c(H+) + 2c(H2C2O4) + c(HC2O  )
C . 0.1 mol·L−1 H2C2O4溶液:0.2 mol·L−1 + c(OH-) = c(H+) + 2c(H2C2O4) + c(HC2O )
C . 0.1 mol·L−1 H2C2O4溶液:0.2 mol·L−1 + c(OH-) = c(H+) + 2c(H2C2O4) + c(HC2O  )
D . 向Na2C2O4溶液中滴加H2C2O4溶液至中性:c(Na+) = 2c(C2O )
D . 向Na2C2O4溶液中滴加H2C2O4溶液至中性:c(Na+) = 2c(C2O 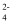 ) )
|
|
| 8. 多选题 | 详细信息 |
|
25℃时,0.10 L某二元弱酸H2A用1.00 mol·L-1NaOH溶液调节其pH,溶液中H2A、HA-及A2-的物质的量浓度变化如图所示:
下列说法错误的是( )
A . H2A的Ka1=1×10-4
B . 溶液在X点和Z点时水的电离程度相同
C . 在Y点时,c(Na+)>3c(A2-)
D . 0.1 mol·L-1NaHA溶液中:c(Na+)>c(HA-)>c(H2A)>c(A2-)
|
|
| 9. 综合题 | 详细信息 |
|
草酸亚铁晶体(FeC2O4·2H2O)是一种重要的化工原料,广泛应用于涂料、染料、玻璃器皿等的着色剂,也可用于新型电池材料,感光材料的生成。实验室制备草酸亚铁晶体的一种流程如下:
|
|
| 10. 多选题 | 详细信息 | |||||||||||||||
|
根据下列实验操作和现象所得到的结论正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
- 2016-2017学年福建省莆田二十五中高一下学期期中化学试卷
- 2016-2017学年河南省洛阳市春都路中学高二上学期开学化学试卷
- 人教版化学高二选修6第三单元实验3-1几种无机离子的检验同步练习
- 2015-2016学年海南省海口二中高二上学期期末化学试卷(理科)
- 江苏省宿迁市2017-2018学年高二下学期化学期末考试试卷
- 新疆维吾尔自治区伊宁市生产建设兵团四师一中2018-2019学年高一上学期化学期中考试试卷
- 2017年高考化学真题试卷(天津卷)(正式版)
- 2016年江西省宜春市靖安县高考化学二模试卷
- 山西省运城市2017-2018学年高三上学期化学期中考试试卷
- 安徽省芜湖市2019-2020学年高二上学期化学期末考试试卷(文)
- 2016年广东省深圳市高考化学二模试卷
- 2015年云南省昆明市高考化学模拟试卷(5月份)
- (4分)有同学说,冬天穿棉袄觉得暖和是因为棉袄能产生热量。请你设计两个小实验来证明他的说法是错误的,并对冬天穿棉袄觉得暖
- 从以下诗句中选择三句,分别填入下面语段的横线上。(填字母序号即可)(4分)A.山寺桃花始盛开B.千叶桃花胜百花C.红杏枝
- 牙齿对动物的生存具有重要意义,生活在南极的海豹在冰下游泳时,隔一段时间就会用牙齿咬破坚冰,浮出水面呼吸空气,海豹牙齿的损
- The other parents tried to pull the heartbroken father off
- 种群研究的核心问题是( ) A.种群的特征 B.种群的密度
- 下列变化属于化学变化的是 A.石蜡熔化 B.酒精挥发 C.食物腐烂 D.胆矾研碎
- 工业酒精中含甲醇(CH4O),甲醇燃烧时生成二氧化碳和水,在这个反应中,参加反应的甲醇、氧气与生成的二氧化碳和水的化学计
- 具有100个碱基对的一个DNA分子片段,内含60个腺嘌呤,如果连续复制2次,则需要游离的鸟嘌呤脱氧核苷酸( )个 A
- 国有大中型企业要按照现代企业制度的方向,进行规范的公司制改革,大力推进股份制,完善公司法人治理结构。对国有大中型企业进行
- 子曰:“由,诲汝知之乎?知之为知之,不知为不知,是知也。”这一说法要求我们 A.深入实践,促进认识发展B.主观必须符合客
- 一些食物的近似pH值如下:葡萄3.5~4.5,苹果2.9~3.3,牛奶6.3~6.6,鸡蛋清7.6~8.0 。下列说法错
- 下列物质能够反应,且没有明显现象的是A. Na2CO3溶液加入澄清石灰水中B. Fe2O3加入NaOH溶液中 C.
- 骆驼和骆驼刺等沙漠动、植物表现出对_______的适应。海豹的皮下脂肪是对______的适应,而旗形树的树冠是对____
- Ⅰ型糖尿病的病因是胰岛B细胞受损,胰岛素分泌不足,下列选项中符合Ⅰ型糖尿病患者实际情况的是()A. 葡萄糖的氧化分解作用
- 我国未来将建立月球基地,并在绕月轨道上建造空间站.如图所示,关闭动力的航天飞机在月球引力作用下向月球靠近,并将与空间站在
- 补出下列名句名篇中的空缺: 1、故国神游,多情应笑我,早生华发。 ,
- 下列各组词语中,没有错别字的一组是 ( ) A
- 我国著名110米栏运动员刘翔在运动会上,对枪声的反应灵敏,动作灵巧、快速、协调,主要原因是通过训练使( ) A.运动
- .在图中,根据给出的入射光线AO画出反射光线OB,并标出反射角及其度数.【解析】根据光的反射定律,反射角等于入射角,所以
- 植物种子内质量相等的下列物质,在被充分氧化时释放能量最多的是() A.淀粉 B.油脂 C.蛋白质 D.核酸









 图-1
图-1 图-2
图-2




