高考二轮复习知识点:原电池工作原理及应用1
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
一种高性能的碱性硼化钒(VB2)—空气电池如下图所示,其中在VB2电极发生反应:
 该电池工作时,下列说法错误的是( ) 该电池工作时,下列说法错误的是( )
A . 负载通过0.04 mol电子时,有0.224 L(标准状况)O2参与反应
B . 正极区溶液的pH降低、负极区溶液的pH升高
C . 电池总反应为
 D . 电流由复合碳电极经负载、VB2电极、KOH溶液回到复合碳电极
D . 电流由复合碳电极经负载、VB2电极、KOH溶液回到复合碳电极
|
|
| 2. 单选题 | 详细信息 |
|
微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是( )
A . 负极反应为
 B . 隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C . 当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D . 电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
B . 隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C . 当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D . 电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
|
|
| 3. 多选题 | 详细信息 |
|
我国科研团队设计了一种表面锂掺杂的锡纳米粒子催化剂
 , 可提高电催化制甲酸盐的产率,同时释放电能,实验原理如图所示。下列说法正确的是( ) , 可提高电催化制甲酸盐的产率,同时释放电能,实验原理如图所示。下列说法正确的是( )
A . 充电时,Zn电极周围pH降低
B . 放电时,每生成
 , 转移 , 转移 个电子
C . 使用催化剂Sn或者 个电子
C . 使用催化剂Sn或者 均能有效减少副产物CO的生成
D . 使用 均能有效减少副产物CO的生成
D . 使用 催化剂,中间产物更不稳定 催化剂,中间产物更不稳定
|
|
| 4. 多选题 | 详细信息 |
|
无膜氯液流电池是一种先进的低成本高储能电池,可广泛应用于再生能源储能和智能电网的备用电源等,电池工作原理如图所示:
下列说法错误的是( )
A . 放电时,M极为正极
B . 放电时,右侧储液器中NaCl的浓度增大
C . 充电时,N极的电极反应式为:Na3Ti2(PO4)3-2e-=NaTi2(PO4)3+2Na+
D . 充电时,电路中每转移1mole- , N电极理论上质量减小23g
|
|
| 5. 综合题 | 详细信息 | |||||||||||||||||||||||||||||||||
|
锂离子电池是新能源汽车的核心部件,综合利用好含锂资源对新能源汽车可持续发展至关重要。科学家用含锂废渣(主要金属元素的含量:
 、 、 、 、 、 、 )制备 )制备 , 并制备锂离子电池的正极材料 , 并制备锂离子电池的正极材料 。部分工艺流程如下: 。部分工艺流程如下:
资料:①滤液1、滤液2中部分离子浓度(
②EDTA能和某些二价金属离子形成稳定的水溶性络合物 ③某些物质的溶解度(S)
|
||||||||||||||||||||||||||||||||||
| 6. 综合题 | 详细信息 |
|
丙烯是重要的有机化工原料,丙烷脱氢是工业生产丙烯的重要途径。回答下列相关问题:
|
|
| 7. 综合题 | 详细信息 |
|
我国提出争取在2030年前实现“碳达峰”,2060年前实现“碳中和”,这对于改善环境,实现绿色发展至关重要。“碳中和”是指将人类经济社会活动所必需的碳排放,通过植树造林和其他人工技术或工程加以捕集利用或封存,从而使排放到大气中的二氧化碳净增量为零。下列各项措施能够有效促进“碳中和”。回答下列问题:
|
|
| 8. 综合题 | 详细信息 | |||||||||||||||
|
以电镀厂含锌废液(主要成分为
 ,还含有少量的 ,还含有少量的  )为原料制备 )为原料制备  的工艺流程如下: 的工艺流程如下: 溶液中金属离子开始沉淀和完全沉淀的
回答下列问题:
|
||||||||||||||||
| 9. 综合题 | 详细信息 |
|
从铜转炉烟灰(主要成分ZnO还有Pb、Cu、Cd、As、Cl、F等元素)中回收锌、铜、铅等元素进行资源综合利用,具有重要意义。以铜转炉烟灰制备重要化工原料活性氧化锌的工艺流程如图所示。
已知:活性炭净化主要是除去有机杂质。 请回答以下问题:
|
|
| 10. 综合题 | 详细信息 |
|
乙醇用途广泛且需求量大,寻求制备乙醇的新方法是研究的热点。
|
|
- 四川省雅安市2017-2018学年高二上学期化学期末考试试卷
- 浙江省名校协作体联盟2019-2020学年高二上学期化学第一次月考试卷
- 吉林省白山市2020年高考理综-化学二模试卷
- 湖北省荆州市2019-2020学年高一下学期化学期末考试试卷
- 2016-2017学年辽宁省大连渤海高中高二上学期期中化学试卷(理科)
- 新人教版必修二高中化学第三章有机化合物3.2.1乙烯
- 2016-2017学年云南省昭通市高三上学期期末化学试卷
- 陕西省宝鸡市2017-2018学年高考理综-化学三模考试试卷
- 专题05:物质的量、物质的量浓度
- 第26讲:高分子化合物及人体内的营养物质
- 四川省雅安市2017-2018学年高一上学期化学期末考试试卷
- 备考2019年高考化学二轮专题 11 非金属及其化合物
- 红军长征胜利结束的标志是( ) A.遵义会议的召开 B.红军三大主力甘肃会宁会师 C.
- 高纯MnCO3是广泛用于电子行业的强磁性材料。MnCO3为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,温度高于100
- 求不等式|x+1|≥|x|的解集.
- 选出标点使用无误的一句( ) A.我不知道他究竟用什么办法使她心服的? B.这件事你跟他说了吗?老李。 C. 他是今天去
- 费孝通说:“我们社会中最重要的亲属关系就是这种丢石头形成的圆心波的性质,以自己为中心,像石子一般投入水中,一圈圈推出去,
- 椰枣是西亚哪个国家的特产( ) A、阿富汗 B、土耳其 C、伊朗
- 锌铜原电池产生电流时,阳离子 ( )A.移
- Sheila. stop_______ bad things aboutothers. A. tosay
- 某同学在图书馆查阅资料时,发现了中国古代某地居民的一份职业结构表,据此推断这种职业结构最可能出现在何时何地
- 如图所示,在水平桌面上的盛水容器中漂浮一个质量分布均匀的正方体木块,若将木块露出水面的部分截去并取走,那么:A、木块余下
- 下列关于氧气的说法不正确的是 A.O2可以支持燃烧 B.O2可用排水法收集 C.O2可用于医
- 下列关于印度说法错误的是( ) A.是南亚面积最大的国家 B.以热带季风气候为主 C.1999年印度棉花产量居世界
- 将离心率为的双曲线的实半轴长a和虚半轴长b 同时增加m 个单位长度,得到离心率为的双曲线,则( ) A.对任意的a,
- 2011年10月31日,据联合国人口基金会的估算,当天世界人口已经达到( )。A、65亿 B、6
- 大量事实表明,在蛋白质合成旺盛的细胞中常有较大的核仁。这可支持哪种说法 A.细胞中的蛋白质主要是由核仁合成的 B.核仁
- It would be interesting to discover how many young people go
- 东西部地区经济合作所取得的实效,不正确的是( ) A.目前东、西部对口帮扶成效显著 B.西部招商引资在西部大开发的
- We have launched another nun-made satellite.______ is annou
- My littlesister was born _____ a sunny morning _______ June,
- 平面内有k条直线,其中任何两条直线不平行,任何三条不共点,设k条直线的交点个数为f(k),则f(k+1)与f(k)的关系





 )
)







 溶液,控制温度在95℃充分反应后,分离出固体
溶液,控制温度在95℃充分反应后,分离出固体 稀溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极进行电解。电解后,向得到的
稀溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极进行电解。电解后,向得到的 溶液共热、过滤、洗涤、干燥得高纯
溶液共热、过滤、洗涤、干燥得高纯 , 则放电时正极反应式为。
, 则放电时正极反应式为。
 2C3H6(g)+2H2O(g) △H1=-238kJ•mol-1
2C3H6(g)+2H2O(g) △H1=-238kJ•mol-1
 =。
=。

 CH3OCOOCH3(g)+H2O(g) ΔH
CH3OCOOCH3(g)+H2O(g) ΔH

 (草酸根)正极反应过程中,O2是催化剂,催化过程可表示为:
(草酸根)正极反应过程中,O2是催化剂,催化过程可表示为:


 如下表所示:
如下表所示:



 溶液 B.
溶液 B.  C.稀硫酸 D.
C.稀硫酸 D. 
 和
和  ,科研团队进一步研发了可逆
,科研团队进一步研发了可逆  电池,电池工作时复合膜(由a、b膜复合而成)层间的
电池,电池工作时复合膜(由a、b膜复合而成)层间的  解离成
解离成 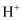 和
和  。
。 
 时,电池复合膜中
时,电池复合膜中  时,
时, 

 )=6.0×10-3mol·L-1 , 现将8.0×10-3mol·L-1FeCl3溶液与浸出液等体积混合生成砷酸铁沉淀。若该温度时Ksp(FeAsO4)=2.0×10-22 , 则反应后溶液中c(AsO
)=6.0×10-3mol·L-1 , 现将8.0×10-3mol·L-1FeCl3溶液与浸出液等体积混合生成砷酸铁沉淀。若该温度时Ksp(FeAsO4)=2.0×10-22 , 则反应后溶液中c(AsO
 ×100%如图所示。
×100%如图所示。

 +
+ →
→




