高考二轮复习知识点:常用仪器及其使用3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
下列图示表示灼烧操作的是( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 2. 单选题 | 详细信息 |
|
关于下列仪器使用的说法错误的是( )
A . ①、④不可加热
B . ②、④不可用作反应容器
C . ③、⑤可用于物质分离
D . ②、④、⑤使用前需检漏
|
|
| 3. 实验探究题 | 详细信息 |
 磁性材料在很多领域具有应用前景,其制备过程如下(各步均在 磁性材料在很多领域具有应用前景,其制备过程如下(各步均在  氛围中进行): 氛围中进行): ①称取 ②向三颈烧瓶中加入 ③持续磁力搅拌,将 ④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在 ⑤管式炉内焙烧2h,得产品3.24g。 部分装置如图: 回答下列问题:
|
|
| 4. 单选题 | 详细信息 | ||||||||||||
|
进行下列实验操作时,选用仪器正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||
| 5. 实验探究题 | 详细信息 |
|
三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·3H2O,Mr=491 g/mol),是制备某些负载型活性铁催化剂的主要原料。实验室中,可通过摩尔盐晶体[(NH4)2Fe(SO4)2·6H2O,Mr=392 g/mol]制备,实验步骤如下:称取5.00 g摩尔盐晶体,加入含5滴1.0 mol/L H2SO4溶液的蒸馏水溶解。再滴加饱和H2C2O4溶液,加热煮沸,生成FeC2O4·2H2O胶状沉淀后继续煮沸3分钟,过滤。在上述沉淀中加入饱和K2C2O4溶液,水浴加热至40℃滴加H2O2溶液,一段时间后,煮沸除去过量的H2O2溶液。再加入4mL饱和H2C2O4溶液,调节溶液的pH为3,一系列操作后,得到三草酸合铁酸钾晶体的质量为5.95g。回答下列问题:
|
|
| 6. 实验探究题 | 详细信息 | |||||||||||||||||||||
|
苯硫酚
 是一种局部麻醉剂。某小组拟制备苯硫酚并探究其性质,已知相关物质的部分信息如下表所示: 是一种局部麻醉剂。某小组拟制备苯硫酚并探究其性质,已知相关物质的部分信息如下表所示:
操作步骤: ①向三口烧瓶中加入 ②再向三口烧瓶中慢慢加入 ③撤去水浴B,微热三口烧瓶,并保持一定的回流。反应平稳后,再加热 ④将反应后的混合液进行水蒸气蒸馏,分出苯硫酚,如图2。 ⑤加入氯化钙,经操作X得粗品 回答下列问题:
|
||||||||||||||||||||||
| 7. 单选题 | 详细信息 | ||||||||||||||||||||
|
下列实验所选择的仪器和试剂准确完整的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 8. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||||
|
某课题小组利用硫渣与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:四氯化锡(SnCl4)常温下为无色液体、易水解。
硫渣的化学组成
氯气与硫渣反应相关产物的熔沸点
|
|||||||||||||||||||||||||||||||
| 9. 单选题 | 详细信息 |
|
下列操作正确的是( )
A . 用酒精灯直接加热锥形瓶内液体
B . 用纸槽向玻璃试管中加铁粉
C . 用托盘天平称取
 时,右盘上放2个 时,右盘上放2个  砝码并用镊子拨动游码至 砝码并用镊子拨动游码至  处
D . 苯酚不慎沾到皮肤上后,立即用抹布擦拭掉,然后再用水冲洗 处
D . 苯酚不慎沾到皮肤上后,立即用抹布擦拭掉,然后再用水冲洗
|
|
| 10. 单选题 | 详细信息 | ||||||||||||||||||||
|
为完成下列各组实验,所选玻璃仪器和试剂均准确、完整的是(不考虑存放试剂的容器和连接装置)( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
- 河南省焦作市2020-2021学年高一上学期化学期中考试试卷
- 2022年新高考广东化学高考真题
- 青海省海东市2021年高考化学二模试卷
- 河北省承德市2021年高考化学二模试卷
- 江苏省淮安市高中校协作体2021-2022学年高二下学期期中考试化学试题
- 四川省成都市蓉城名校联盟2021-2022学年高一下学期入学考试化学试题
- 四川省雅安市2020-2021学年高一下学期期末检测化学试题
- 浙江省山河联盟学校2020-2021学年高一下学期化学4月月考试卷
- 福建省八地市(福州、厦门、泉州、莆田、南平、宁德、三明、龙岩)2022届高三毕业班4月诊断性联考化学试题
- 重庆市2021-2022学年缙云教育联盟高三第〇次诊断性检测化学试题
- 吉林省白山市2020-2021学年高二上学期化学期末考试试卷
- 河北省石家庄市2021-2022学年高三上学期毕业班教学质量检测(一)化学试题
- 关于闭合电路的性质,以下说法正确的是A.电源短路时,输出电流无限大 B.电源断路时,路端电压无限大
- Today, roller skating is easy and fun. But a long time ago,
- —Jenny, which seasonis your favorite? —For me, summer is ___
- 若b<0<a,则下列各式不成立的是: A、a-b>0 B、-a+b<0
- 依次填出下面一段文字横线处的语句,衔接最恰当的一组是 狗是忠义、勇敢而又聪明的动物。 , 。 , 。 , ,使狗
- 阅读《拿来主义》选段,完成小题。 他占有,挑选。看见鱼翅,并不就抛在路上以显得“平民化”,只要有养料,也和朋友们像萝
- The workers can complete the new bridge in_________ . A.two
- Tom's mother needed ________ at once, ________ made him worr
- 你班将开展综合性学习“古诗苑漫步”活动,请你积极参与。1.请你在前黑板上书写一条主题语:
- 读河流人工裁弯取直工程图。此工程重点治理的河段是( )A.川江 B.荆江 C.沱沱河
- 下列与生态系统有关的叙述中,正确的是() A. 寄生生物的存在会影响被寄生生物的生存,从而降低生物多样性 B. 食物链
- 下列图案是轴对称图形的有( )。A.(1)(2)B.(1)(3)C.(1)(4)D.(2)(3) (1)
- 如图是杭州萧山少儿公园局部景点示意图。“蹦蹦床”A在“小舞台”C的正北方向,在“正大门”B的北偏东30°方向;“小舞台”
- 已知棱台的上下底面面积分别为,高为,则该棱台的体积为___________。
- 如图(1),在三角形中,,若,则;若类比该命题,如图(2),三棱锥中,面,若点在三角形所在平面内的射影为,则有什么结论?
- 美国1787年《联邦宪法》确立了一套“地狱和体制的双向平衡机制”,是孟德斯鸠“以权力制约权力”学说第一次在政府体制的设计
- 0ur chairman hasn’t come yet.If he on time,we would have
- X物质是一种重要的阻燃剂,工业上用三氧化二锑(Sb2O3)为原料按下列反应Sb2O3+2H2O2=X+2H2O可制取X物
- 阅读下面的文字,完成下面题目:语文诗话1语文的实质是什么?有人认为语文的实质是工具性。我认为,这种观点是片面的,它忽视了
- 南京长江二桥,二桥全程长21.97km,为了保证交通安全合畅通,规定车辆通过二桥速度最大为100km/h,最小为60km

 ,配成
,配成  溶液,转移至恒压滴液漏斗中。
溶液,转移至恒压滴液漏斗中。 溶液。
溶液。 溶液以
溶液以  的速度全部滴入三颈烧瓶中,100℃下回流3h。
的速度全部滴入三颈烧瓶中,100℃下回流3h。 干燥。
干燥。
 有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置,选出一种可行的方法,化学方程式为,对应的装置为(填标号)。
有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置,选出一种可行的方法,化学方程式为,对应的装置为(填标号)。  、
、  、
、  、
、  、饱和
、饱和  、饱和
、饱和 

 ,离子方程式为。
,离子方程式为。
 水解
水解



 溶液的化学反应方程式。
溶液的化学反应方程式。
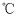




 冰和
冰和  浓硫酸。
浓硫酸。 苯磺酰氯,尽快地分次加入
苯磺酰氯,尽快地分次加入  锌粉,继续反应
锌粉,继续反应  ,温度保持在
,温度保持在  左右,如图1。
左右,如图1。 。
。 。再进行蒸馏,收集馏分,得纯品
。再进行蒸馏,收集馏分,得纯品  。
。 。
。
 溶液中,振荡,溶液褪色,说明苯硫酚具有(填“氧化”或“还原”)性。
溶液中,振荡,溶液褪色,说明苯硫酚具有(填“氧化”或“还原”)性。
 、Ca2+、Mg2+杂质
、Ca2+、Mg2+杂质
 +I2=2I-+
+I2=2I-+ 
 溶液、硝酸银溶液
溶液、硝酸银溶液 的焰色试验
的焰色试验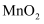 、浓盐酸、
、浓盐酸、  溶液
溶液


