高考二轮复习知识点:元素周期表中原子结构与元素性质的递变规律2
高考二轮复习知识点:元素周期表中原子结构与元素性质的递变规律2
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。回答下列问题:
|
|
| 2. 综合题 | 详细信息 |
|
磷是人体所必需的重要矿物质元素,磷的化合物在生产和生活中应用广泛。
反应:P4+ NaOH+H2O→ NaH2PO2 +PH3(未配平)制得的次磷酸钠(NaH2PO2)可作食品防腐剂,也可用于化学镀镍。 请回答下列问题:
|
|
| 3. 综合题 | 详细信息 |
|
过碳酸钠(2Na2CO3·3H2O2)晶体性质具有Na2CO3和H2O2
的双重性,被广泛用于氧气发生、漂白杀菌、污水处理、金属表面处理以及高分子聚合控制等。
|
|
| 4. 推断题 | 详细信息 |
|
X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素。X和R属同族元素;Z和U位于第VIIA族;X和Z可形成化合物XZ4;Q基态原子的s轨道和p轨道的电子总数相等;T的一种单质在空气中能够自燃。
请回答下列问题:
|
|
| 5. 单选题 | 详细信息 | |||||||||||||||
|
短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法正确的是( )
A . 元素电负性:Z<W
B . 简单离子半径:W<Y
C . 元素第一电离能:Z<W
D . 简单氢化物的沸点:X<Z
|
||||||||||||||||
| 6. 综合题 | 详细信息 |
|
周期表前四周期的元素
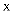 、 、  、 、  、 、  ,原子序数依次增大,X原子基态时 ,原子序数依次增大,X原子基态时  层中 层中 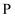 轨道电子数与s轨道电子数相同; 轨道电子数与s轨道电子数相同;  原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料; 原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料;  位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题: 位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
|
|
| 7. 单选题 | 详细信息 | ||||||||||
|
现有4种短周期主族元素X、Y、Z和Q,原子序数依次增大,其中Z、Q在同一周期。相关信息如下表:
下列说法正确的是( )
A . 常温时,X单质能与水发生剧烈反应
B . Y与Q元素组成的YQ4分子,空间构型为正四面体
C . Y、Z、Q最高价氧化物对应水化物的酸性依次减弱
D . 第五周期且与Q同主族元素的单质在常温常压下呈液态
|
|||||||||||
| 8. 单选题 | 详细信息 |
|
我国嫦娥五号探测器带回1.731 kg的月球土壤,经分析发现其构成与地球土壤类似,土壤中含有的短周期元素W、X、Y、Z,原子序数依次増大,最外层电子数之和为 15。X、Y、Z为同周期相邻元素,且均不与W同族,下列结论正确的是( )
A . 原子半径大小顺序为W>X>Y>Z
B . 化合物XW中的化学健为离子键
C . Y单质的导电性能弱于Z单质的
D . Z的氧化物的水化物的酸性强于碳酸
|
|
| 9. 综合题 | 详细信息 |
|
氧、硫、硒、碲等氧族元素在化合物中常表现出多种氧化态,含氧族元素的化合物在研究和生产中有许多重要用途。请回答以下问题:
|
|
| 10. 单选题 | 详细信息 |
|
一种麻醉剂的分子结构式如图所示。其中,
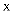 的原子核只有1个质子;元素 的原子核只有1个质子;元素  、 、  、 、  原子序数依次增大,且均位于 原子序数依次增大,且均位于 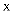 的下一周期;元素 的下一周期;元素  的原子比 的原子比  原子多8个电子。下列说法不正确的是( ) 原子多8个电子。下列说法不正确的是( )
A .
 是一种强酸
B . 非金属性: 是一种强酸
B . 非金属性:  C . 原子半径:
C . 原子半径:  D .
D .  中, 中,  的化合价为+2价 的化合价为+2价
|
|
高中化学 试卷推荐
- 2015-2016学年吉林省吉林市毓文中学高二下学期期中化学试卷
- 广西百色市2017-2018学年高一下学期化学期末考试试卷
- 2016年上海市黄浦区高考化学一模试卷
- 黑龙江省鸡西市虎林高级中学2016-2017学年高二上学期化学期末考试试卷
- 山东省济宁市2019-2020学年高一下学期化学期末考试试卷
- 广东省揭阳市2017-2018学年高二下学期化学期末考试试卷
- 江苏省扬州市2018-2019学年高二下学期化学期末考试试卷
- 江苏省无锡市普通高中2017-2018学年高二上学期化学期末考试试卷
- 专题27:苯、芳香烃
- 2016-2017学年湖北省四地七校高二下学期期中化学试卷
- 山东省德州市2017-2018学年高一下学期化学期末考试试卷
- 备考2018年高考化学一轮基础复习:专题24 水的电离和溶液的酸碱性
最近更新
- 学校决定在校园里某些地方写上富有教育性的诗句,用来劝学和励志,请你推荐一条,并说明推荐理由。(注意:①必须是比较有名的诗
- 下列各组省(区)中,人口密度最小的是 ( ) A.湖南、江西
- 如太阳直射20°N,那么
- 下列直接影响动物种群密度变化的是( ) A.出生率、死亡率和迁入、迁出 B.年龄组成和出生率、死亡
- 右图为某一遗传病系谱图,该病不可能的遗传方式是 ( ) (A)常染色体
- 设为曲线上一点,曲线在点处的切线的斜率的范围是,则点纵坐标的取值范围是_____ ___.
- 在函数y=中,自变量x的取值范围是 .
- p{font-size:10.5pt;line-height:150%;margin:0;padding:0;}td{f
- 下列物品或装饰品,不易受酸雨腐蚀的是:( ) A. 大理石华表 B. 铝合金窗框 C.
- 地崩山摧壮士死, 。(李白《蜀道难》)
- 长江、黄河共同流经的省级行政区是( ) A.青海、四川 B.青海、宁夏 C.云南、
- 已知抛物线y=x2+2x+k+1与x轴有两个不同的交点,则一次函数y=kx﹣k与反比例函数y=在同一坐标系内的大致图象是
- 根据拼音写出汉字或根据汉字写拼音。共4分 润如油gāo________ 一代天jiāo________
- 下列实验操作中正确的是
- ,志在千里。(曹操《龟虽寿》)
- 目前普遍认为,质子和中子都是由被称为u夸克和d夸克的两类夸克组成的.u夸克带电荷量为e,d夸克带电荷量为-e,e为元电荷
- (11分)由于生态环境的破坏,地表土裸露,大片土地沙漠化,加上春季干旱少雨,所以近年来我国北方地区3、4月份扬尘天气明显
- 函数中,自变量x的取值范围是 .
- 请根据常见金属性质回答问题: (1)将以下常见金属的活动顺序补充完整。金属活动性由强逐渐减弱 (2)黄金首饰不易锈蚀的
- The doctor came upand asked me ______the day before. A.wha

 )水对人体危害极大,可用过碳酸钠改性赤泥进行处理,反应如下:
)水对人体危害极大,可用过碳酸钠改性赤泥进行处理,反应如下:  +H2O2→MnCO3¯+ +OH-+H2O
+H2O2→MnCO3¯+ +OH-+H2O  溶液对应的pH(25℃)
溶液对应的pH(25℃) 基态核外电子排布式为,用铁氰化钾溶液检验
基态核外电子排布式为,用铁氰化钾溶液检验  的离子方程式为。
的离子方程式为。
 ,反应的化学方程式:。
,反应的化学方程式:。 






