近三年高考化学真题分类汇编:化学反应速率和化学平衡3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用作有机合成中的碘化剂。回答下列问题:
|
|
| 2. 单选题 | 详细信息 |
|
室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v1=k1c2(M),反应②的速率可表示为v2=k2c2(M) (k1、k2为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是( )
A . 0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1
B . 反应开始后,体系中Y和Z的浓度之比保持不变
C . 如果反应能进行到底,反应结束时62.5%的M转化为Z
D . 反应①的活化能比反应②的活化能大
|
|
| 3. 单选题 | 详细信息 |
|
常温下,用
 的盐酸分别滴定20.00mL浓度均为 的盐酸分别滴定20.00mL浓度均为  三种一元弱酸的钠盐 三种一元弱酸的钠盐  溶液,滴定曲线如图所示。下列判断错误的是( ) 溶液,滴定曲线如图所示。下列判断错误的是( )
A . 该
 溶液中: 溶液中:  B . 三种一元弱酸的电离常数:
B . 三种一元弱酸的电离常数:  C . 当
C . 当  时,三种溶液中: 时,三种溶液中:  D . 分别滴加20.00mL盐酸后,再将三种溶液混合:
D . 分别滴加20.00mL盐酸后,再将三种溶液混合: 
|
|
| 4. 多选题 | 详细信息 |
|
已知:
  ,向一恒温恒容的密闭容器中充入 ,向一恒温恒容的密闭容器中充入  和 和  发生反应, 发生反应,  时达到平衡状态I,在 时达到平衡状态I,在  时改变某一条件, 时改变某一条件,  时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是( ) 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是( )
A . 容器内压强不变,表明反应达到平衡
B .
 时改变的条件:向容器中加入C
C . 平衡时A的体积分数 时改变的条件:向容器中加入C
C . 平衡时A的体积分数  : :  D . 平衡常数K:
D . 平衡常数K: 
|
|
| 5. 单选题 | 详细信息 |
|
铁的配合物离子(用
 表示)催化某反应的一种反应机理和相对能量的变化情况如图所示: 表示)催化某反应的一种反应机理和相对能量的变化情况如图所示: 下列说法错误的是( )
A . 该过程的总反应为
 B .
B . 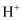 浓度过大或者过小,均导致反应速率降低
C . 该催化循环中 浓度过大或者过小,均导致反应速率降低
C . 该催化循环中  元素的化合价发生了变化
D . 该过程的总反应速率由Ⅱ→Ⅲ步骤决定 元素的化合价发生了变化
D . 该过程的总反应速率由Ⅱ→Ⅲ步骤决定
|
|
| 6. 综合题 | 详细信息 | ||||||||
|
氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法I:氨热分解法制氢气 相关化学键的键能数据
一定温度下,利用催化剂将
|
|||||||||
| 7. 单选题 | 详细信息 |
 为阿伏加德罗常数的值。下列叙述正确的是( ) 为阿伏加德罗常数的值。下列叙述正确的是( )
A .
 重水( 重水(  )中含有的质子数为 )中含有的质子数为  B .
B .  的 的  与 与  完全反应时转移的电子数为 完全反应时转移的电子数为  C .
C .  环状 环状  ( (  键数为 键数为  D .
D .  的 的  溶液中 溶液中  离子数为 离子数为 
|
|
| 8. 单选题 | 详细信息 |
|
已知相同温度下,
 。某温度下,饱和溶液中 。某温度下,饱和溶液中  、 、  、与 、与  的关系如图所示。 的关系如图所示。 下列说法正确的是( )
A . 曲线①代表
 的沉淀溶解曲线
B . 该温度下 的沉淀溶解曲线
B . 该温度下  的 的  值为 值为  C . 加适量
C . 加适量  固体可使溶液由a点变到b点
D . 固体可使溶液由a点变到b点
D .  时两溶液中 时两溶液中 
|
|
| 9. 综合题 | 详细信息 |
|
二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
|
|
| 10. 单选题 | 详细信息 | |||||||||||||||
|
化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
- 山东省潍坊市2020-2021学年高一上学期化学期末考试试卷
- 陕西省宝鸡市2021年高考化学5月模拟试卷
- 浙江省名校新高考研究联盟(Z20联盟)2020-2021学年高三上学期化学第二次月考试卷
- 广东省汕头市潮阳区2020-2021学年高二上学期化学期末考试试卷
- 备考2021年高考化学二轮专题 第2讲 非金属元素及其化合物
- 山东省济南市2021年高考化学三模试卷
- 北京市房山区2020-2021学年高二上学期期末考试化学试题
- 广东省惠州市2022届高三第一次模拟考试化学试题
- 四川省成都市蓉城名校联盟2020-2021学年高二下学期期末联考化学试题
- 上海市徐汇区2021年高考化学二模试卷
- 河南省南阳市六校2021-2022学年高二上学期第一次联合测试化学试题
- 江苏省苏州市吴中区2020-2021学年高二上学期化学期中考试试卷
- “朴雪”乳酸亚铁口服液可以有效地治疗人类缺铁性贫血症,这是因为其中的Fe2+进入人体后能() A.调节血液的
- 某合金与铁的物理性质的比较如下表所示: 熔点/ ℃ 密度/g·cm-3 硬度(金刚石为10) 导电性(银为100) 某
- 下列四组生物中,都属真核生物的一组是 ( ) A.噬
- 某企业2008年的生产总值为1000万元,生产成本为600万元。假定该企业2009年生产成本保持不变,经济效益提高了20
- 在第一个“金色十年”,金砖国家经济总量占全球经济比重从12%上升到23%,贸易总额比重从11%上
- (本小题满分12分) 如图所示,在直三棱柱ABC—A1B1C1中,∠ABC=90°,BC=CC1,M、N分别为B
- 下列各句中,加黑的成语使用不正确的一组是( ) A、虽然让人难以相信,但他还是凭一张假证件堂而皇之地走进了展览厅的大门。
- 下列有关植物激素的叙述,正确的是()A.图1中生长素(IAA)和赤霉素(GA)同时存在对茎切段细胞分裂有促进作用 B.图
- 如图所示,小木块放在倾角为 α 的斜面上,受到一个水平力 F(F ≠ 0)的作用处于静止.则小木块受到斜面的支持力和摩擦
- 新疆瓜果特别甜,原因是 A.云量多,光照弱,有利于作物的光合作用 B.降水少,瓜果水分含量少,糖分高 C.昼夜温差大,营
- 登高 杜甫 风急天高猿啸, 渚清沙白鸟飞回。无边落木萧萧下,不尽长江滚滚来。 万里悲秋常作客,百年多病独登台。艰难苦恨繁
- 关于电动势下列说法正确的是 [ ] A.电源电动势等于电源正负极之间的电势差 B.用电压表直接测量电源两极得
- (15分)【历史——历史上重大改革回眸】阅读材料,回答问题。 材料一 下表体现了宗教改革的宣传形式与内容.材料二
- 资源损失的灾情相对于财产的损失而言具有的特点是( ) A滞后性和隐蔽性 B长远性和超前性 C广泛性和
- 设、分别是曲线和上的动点,则、的最小距离是
- 下列实验操作中,正确的是
- 下列叙述不正确的是 ( ) A. CH4与C4H10互为同系物 B. C5H12
- 有关卫生防疫部门经常使用的消毒剂主要有二氧化氯(ClO2)、“84”消毒液(有效成分为NaClO)等,据此回答下问题:
- 70%的囊性纤维病患者是由于编码CFTR蛋白的基因缺失了3个碱基,导致了CFTR蛋白的结构异常,该实例可以说明 A.基因
- 同志在全国民族工作会议上指出,民族地区存在的困难和问题,归根结底要靠发展来解决,我们必须从全局和战略的高度,充分认识加快
 2NOCl(g)+I2(g) KP1
2NOCl(g)+I2(g) KP1
 和lgKP2
和lgKP2 








 分解为
分解为  和
和  。回答下列问题:
。回答下列问题:

 ;
;
 ,在下列哪些温度下反应能自发进行?_______(填标号)
,在下列哪些温度下反应能自发进行?_______(填标号)
 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。 
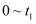 时间内的反应速率
时间内的反应速率 
 (用含
(用含  。(已知:分压=总压×该组分物质的量分数,对于反应
。(已知:分压=总压×该组分物质的量分数,对于反应  ,
,  ,其中
,其中  ,
,  、
、  、
、  、
、  为各组分的平衡分压)。
为各组分的平衡分压)。
 的移动方向为(填“从左往右”或“从右往左”);
的移动方向为(填“从左往右”或“从右往左”);




 ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是(填标号),判断的理由是。
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是(填标号),判断的理由是。 B.
B.  C.
C.  D.
D. 
 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为  ,在
,在  ℃下的
℃下的  、在
、在  下的
下的  如图所示。
如图所示。 
 ;
; 时,
时,  的平衡转化率
的平衡转化率  ,反应条件可能为或。
,反应条件可能为或。
 降温
降温 溶液中,加入乙醇并振荡
溶液中,加入乙醇并振荡 固体放回原试剂瓶
固体放回原试剂瓶


