高中化学人教版(2019)必修第一册寒假专项训练 化学键
高中化学人教版(2019)必修第一册寒假专项训练 化学键
教材科目:化学
试卷分类:高一上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高一上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
元素周期表在学习研究中有很重要的作用,如图是元素周期表的一部分。
回答下列问题:
|
|
| 2. 综合题 | 详细信息 | ||||||||||||
|
W、X、Y、Z为同一周期的四种主族元素,原子序数依次增大。基态Y原子的价电子排布为
 ,X的电离能数据如下表所示。 ,X的电离能数据如下表所示。
|
|||||||||||||
| 3. 综合题 | 详细信息 |
|
A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为
 , B是同周期第一电离能最小的元素,基态C原子的最外层有三个未成对电子,基态E原子的价电子排布式为3d64s2。 , B是同周期第一电离能最小的元素,基态C原子的最外层有三个未成对电子,基态E原子的价电子排布式为3d64s2。
回答下列问题:
|
|
| 4. 综合题 | 详细信息 |
|
将高温水蒸气通到硫氰化钾的表面,会发生如下反应:4KSCN+9H2O(g)→K2CO3+K2S+3CO2+3H2S+4NH3。
完成下列填空:
|
|
| 5. 综合题 | 详细信息 | ||||||||||
|
按要求完成下列问题
|
|||||||||||
| 6. 单选题 | 详细信息 |
|
中国科学家成功合成全氮阴离子
 , ,  是全氮类物质 是全氮类物质  的重要中间体。全氮类物质具有高密度、超高能量及爆轰产物无污染等优点。下列说法中错误的是( ) 的重要中间体。全氮类物质具有高密度、超高能量及爆轰产物无污染等优点。下列说法中错误的是( )
A . 每个
 中含有36个质子
B . 中含有36个质子
B .   属于离子化合物
C . 属于离子化合物
C .   结构中含有离子键和共价键
D . 全氮类物质属于绿色能源 结构中含有离子键和共价键
D . 全氮类物质属于绿色能源
|
|
| 7. 单选题 | 详细信息 |
|
过氧化氢(
 )被称为绿色氧化剂,其分子结构如图所示。两个氢原子位于不重合的两个平面上,两个氧原子位于两平面的交线上。下列有关说法错误的是( ) )被称为绿色氧化剂,其分子结构如图所示。两个氢原子位于不重合的两个平面上,两个氧原子位于两平面的交线上。下列有关说法错误的是( )
A .
 既有氧化性又有还原性
B . 过氧化氢分子中含有H—H键、O—O键
C . 过氧化氢分子的电子式为 既有氧化性又有还原性
B . 过氧化氢分子中含有H—H键、O—O键
C . 过氧化氢分子的电子式为 |
|
| 8. 单选题 | 详细信息 |
|
下列物质性质的变化与化学键强弱无关的是( )
A . HF、HCl、HBr、HI的热稳定性依次减弱
B . NaF、NaCl、NaBr、NaI的熔点依次降低
C . Li、Na、K、Rb 的熔点逐渐降低
D . F2、Cl2、Br2、I2的熔、沸点逐渐升高
|
|
| 9. 单选题 | 详细信息 |
|
少量
 与 与 反应生成 反应生成 和 和 。下列说法正确的是( ) 。下列说法正确的是( )
A .
 的电子式为 的电子式为 的空间构型为直线形
C . 的空间构型为直线形
C .  中O元素的化合价为-1
D . 中O元素的化合价为-1
D .  仅含离子键 仅含离子键
|
|
| 10. 单选题 | 详细信息 |
|
下列变化既破坏了共价键又破坏了离子键的是( )
A . 氯化氢溶于水
B . 水挥发为水蒸气
C . 碳酸氢钠受热分解
D . 氯化镁熔融
|
|
高中化学 试卷推荐
- 高中化学人教版(2019)必修第一册 第四章测试卷
- 高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第二节 影响化学反应速率的因素 影响化学反应速率的因素
- 吉林省白城市第十四中学2019-2020学年高一上学期化学期末考试试卷
- 2016-2017学年四川省成都市龙泉二中高三上学期期中化学试卷
- 北京市海淀区2020年高考化学一模试卷
- 吉林省长春市榆树市2019-2020学年高一上学期化学期末考试试卷
- 2016-2017学年湖北省襄阳市枣阳七中高三上学期开学化学试卷
- 专题20:化学键
- 2015-2016学年江西省赣州市于都三中高二下学期期中化学试卷
- 福建省莆田市2017-2018学年高考理综-化学二模考试试卷
- 北京市石景山区2017-2018学年高考理综-化学一模考试试卷(3月)
- 2016-2017学年湖北省重点高中联考高一下学期期中化学试卷
最近更新
- The young man had made so much noise that he not have
- 劣质商品的生产者和销售者的行为,从经济学上看 ①违背了市场交易原则 ②违反了职业道德
- 我国的沿海、沿江港口、铁路枢纽、高速公路沿线地区,发展了较多工业,主要是因为这些地区( ) A.靠近原料产地,节省
- 下列岩石属沉积岩是A. 玄武岩 B.砂岩、页岩 C. 大理岩 D.花岗岩
- 某研究人员成功找到了一种适宜口服治疗糖尿病的小分子(Boc5)。现用一些各项条件都适宜的糖尿病小鼠(空腹)进行一项验证性
- 圆褐固氮菌双链DNA中的某片段如图所示,若基因B发生突变,导致该基因编码的蛋白质肽链中一个氨基酸变成了另一个氨基酸,据图
- 秦汉时期,通过陆上丝绸之路和海上丝绸之路,中华文明都可以传播的地区是 A.巴尔干半岛 B.印度半岛
- 世界卫生组织将某氧化物RO2列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛应用。实验测得该氧化物中R
- 9、在生物性状遗传中,能稳定遗传的个体是 A.具有等位基因的个体 B.具有隐性性状的个体C.具有显性性状的个体
- 阅读下面这首宋词,回答问题。(8分)点绛唇•送李琴泉吴大有江上旗亭,送君还是逢君处。酒阑呼渡,云压沙鸥暮。漠漠萧萧,香冻
- 分子式为C3H6Cl2的链状有机物的同分异构体共有(不包括立体异构) A.6种 B.5种
- 下列关于清朝文字狱的解释,正确的是() A.为压制反清思想而迫害知识分子的冤案 B.专门关押知识分子的监狱 C.推行文化
- The stone under her feet rolled; and as she was into
- 下图表示人体不同组织处血管示意图(A、B、C分别表示不同类型的血管),请据图分析回答: (11分)(1)图中血管A、B、
- 如图所示实验装置,斜面长2m,秒表每格1s。小车在拉力F作用下,从底端匀速到达顶端,秒表变化如图(指针转动未超过一周)。
- R、M、T、G、J为原子序数依次递增的同一周期主族元素,下列说法一定正确的是(m、n均为正整数)
- 关于美国经济的描述,错误的是 A.是世界上经济最发达的国家 B.农业实现了机械化和生产专业化 C.是世界上出口小汽车、石
- _________ money , they had to give up the research. A. Lac
- 判断下列命题中正确的为( ) A.若,则 B.若,则 C.若,则 D.若,,则
- “新世纪到来之际。我们已经创造了2000多万个新的就业岗位。出现了30多年来最快速的经济增长,失业率为30年来的最低水平

 与
与  互称为。
互称为。




 中硫显正价而氯显负价
中硫显正价而氯显负价 溶液中,有淡黄色沉淀生成
溶液中,有淡黄色沉淀生成 标准溶液滴定
标准溶液滴定  生成
生成  ,该反应的离子方程式为。
,该反应的离子方程式为。





 /
/ 

 溶液中,溶液变浑浊
溶液中,溶液变浑浊 的酸性比
的酸性比  强
强 ,该水化物中的
,该水化物中的  结构有两种断键方式:断
结构有两种断键方式:断  键在水中电离出
键在水中电离出  ;断
;断  键在水中电离出
键在水中电离出 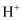 。
。 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩




