高考二轮复习知识点:离子共存1
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用.
|
|
| 2. 多选题 | 详细信息 |
|
对有关NaClO和NaCl混合溶液的叙述正确的是( )
A . 该溶液中,H+、NH
 、SO 、SO  、Br﹣可以大量共存
B . 该溶液中,K+、OH﹣、S2﹣、NO3﹣不能大量共存
C . 向该溶液中滴入少量FeSO4溶液,离子方程式为:2Fe2++ClO﹣+2H+→Cl﹣+2Fe3++H2O
D . 向该溶液中加入浓盐酸,每产生1molCl2 , 转移电子约为6.02×1023个 、Br﹣可以大量共存
B . 该溶液中,K+、OH﹣、S2﹣、NO3﹣不能大量共存
C . 向该溶液中滴入少量FeSO4溶液,离子方程式为:2Fe2++ClO﹣+2H+→Cl﹣+2Fe3++H2O
D . 向该溶液中加入浓盐酸,每产生1molCl2 , 转移电子约为6.02×1023个
|
|
| 3. 多选题 | 详细信息 |
|
若在加入铝粉能产生氢气的无色溶液中,分别加入下列各组离子,可能共存的是( )
A . NH4+、NO3﹣、Al3+、Cl﹣
B . Na+、AlO2﹣、K+、NO3﹣
C . MnO4﹣、K+、SO42﹣、Na+
D . AlO2﹣、K+、NO3﹣、OH﹣
|
|
| 4. 多选题 | 详细信息 |
|
在由水电离产生的H+浓度为1×10﹣13mol•L﹣1的溶液中,一定能大量共存的离子组是( )
A . K+、Cl﹣、NO3﹣、S2﹣
B . K+、Fe2+、I﹣、SO42﹣
C . Na+、Cl﹣、NO3﹣、SO42﹣
D . K+、Ba2+、Cl﹣、NO3﹣
|
|
| 5. 多选题 | 详细信息 |
|
在强酸性溶液中,能大量共存的离子组是( )
A . K+、Cu2+、OH﹣、SO42﹣
B . K+、Na+、Cl﹣、NO3﹣
C . Zn2+、NH4+、NO3+、Cl﹣
D . K+、Na+、CO32﹣、SO42﹣
|
|
| 6. 多选题 | 详细信息 |
|
向含有
 、 、  、 、  、 、  的溶液中加入过量的 的溶液中加入过量的  ,微热并搅拌,然后加入过量的稀盐酸,充分反应后溶液中离子的数目减少的是 ,微热并搅拌,然后加入过量的稀盐酸,充分反应后溶液中离子的数目减少的是
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 7. 多选题 | 详细信息 |
|
下列各组离子在水溶液中能大量共存的是()
A . CO32-、Na+、H+
B . Cu2+、Cl-、OH-
C . Mg2+、Ca2+、NO3-
D . H+、Al3+、SO42-
|
|
| 8. 多选题 | 详细信息 |
|
在某澄清透明的溶液中,能大量共存的离子组是( )
A . Ba2+、Na+、Cl-、HCO3-
B . Fe3+、NH4+、NO3-、SCN-
C . H+、Fe2+、NO3-、SO42-
D . NH4+、Al3+、SO42-、Cl-
|
|
| 9. 综合题 | 详细信息 | ||||||||||||||||||
|
工业上可以用天青石生产碳酸锶后的含锶废渣制备高纯六水氯化锶(SrCl2•6H2O),含锶废渣主要成分为SrCO3 , 且含钡、铁、钙等元素。六水氯化锶是一种无色长针状晶体,易溶于水,微溶于无水乙醇和丙酮,下面为实验室模拟SrCl2•6H2O的制作流程:
已知:①SrSO4微溶于水; ②SrCl2•6H2O在61.5℃以上即会失去4个结晶水生成SrCl2•2H2O。
|
|||||||||||||||||||
| 10. 单选题 | 详细信息 | |||||||||||||||
|
对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
- 上海市浦东新区2018-2019学年高考化学一模考试试卷
- 北京市房山区2017-2018学年高考理综-化学二模考试试卷
- 2015-2016学年辽宁省葫芦岛市六校协作体联考高二下学期期中化学试卷
- 江西省赣州市四校协作2017-2018学年高三上学期化学期中考试试卷
- 2015-2016学年四川省攀枝花十二中高二下学期期中化学试卷
- 2015-2016学年甘肃省陇南市西和二中高二下学期期中化学试卷
- 江西省赣州市2019-2020学年高一下学期化学期末考试试卷
- 2015-2016学年陕西省延安市黄陵中学高一下学期期中化学试卷
- 人教版化学高二选修5第三章第一节醇 酚同步练习
- 2017年湖北省武汉市武昌区高考化学模拟试卷
- 2016-2017学年江西省吉安三中高一上学期期中化学试卷
- 浙江省绍兴市诸暨市2018-2019学年高三上学期化学期末考试试卷
- 如图所示,下列说法中不正确的是( )
- 下列关于二战概况的表述不正确的是 A.直接涉及欧、亚、非、美四大洲 B.直接涉及大西洋、太平洋、印度洋、北冰洋四大洋 C
- 费正清在《美国与中国》中说:“l977年后的中国转变了方针。为了现代化,国家重视专甚于红,重新建立了为国选拔人才的传统制
- (07浙江部分重点中学联考)对线粒体分布、数量的下列叙述中,哪一项是不确切的A.动物细胞比绿色植物细胞的线粒体数量多B.
- 短周期主族元素A、B、C、D、E、的原子序数依次增大,A和B形成5个原子核的分子,A和C形成3个原子核的分子,且两种分子
- 中华民族是一个饱经灾难的民族,灾难使中华民族更加坚强、团结。四川汶川8.0级特大地震将全中国十三亿民众凝聚了起来,将全世
- (1)2015 年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4- 和有机阳离
- 下列实验方案中,不能达到实验目的的是() 选项 实验目的 实验方案 A 检验CH3CH2Br在NaOH溶液中是否发生水解
- 读下图回答:若下图为上图中A城郊三种农事活动收益(元)距城镇(市场)的距离变化示意图。则下列说法正确的是:A.X、Y、Z
- 2002年当地时间5月5日晚,法国总统大选第二轮投票统计结果揭晓,时任总统希拉克以绝对优势挫败极右势力代表勒庞,赢得本
- 下列框图题中,已知A、E、F、H是单质,其中只有A是一种常见的金属单质,其它都是气体,且H是呈黄绿色;B是最常见液体,C
- 如果用3H标记的胸苷和3H标记的尿苷,分别处理活的洋葱根尖,一段时间后检测大分子放射性,最可能的结果是() A.前者部分
- 在含有较多NH4+、Ba2+、NO3ˉ、Clˉ的溶液中还能大量共存的离子是 A.Ag+ B.M
- 我国台湾出口导向型经济发展的有利因素有( ) ①劳动力丰富 ②吸收外国资本 ③岛内市场广阔
- 下列作品属于同一类型的有()①《苹果车》 ②《母亲》 ③《巴黎圣母院》 ④《红与黑》 ⑤《项链》A.①②③④ B.①③④
- 下列图示实验操作中,正确的是 ( )
- 小明想了解不溶于水的化工原料石英粉的密度,已知水的密度为ρ水,他利用天平(含砝码),一个玻璃杯、足量的水,就能完成测量石
- 下列有关染色体的说法,正确的是 A.染色体只存在于生殖细胞中 B.染色体存在于细胞核中 C.染色体容易被酸碱染料染色 D
- 将函数的图象向左平移个单位长度后,所得到的图象关于轴对称,则的最小值是( ) A. B.
- Li Lei's parents______doctors.A. are all B. are bothC. all



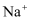 、
、  、
、  、
、 

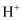 、
、  、
、  、
、 

 、
、 




