内蒙古呼伦贝尔市 2022届高三一模理科综合化学试题
内蒙古呼伦贝尔市 2022届高三一模理科综合化学试题
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
化学与社会、生活、生产密切相关,下列有关说法错误的是。( )
A . 2022年北京冬奥会开幕式上绚丽多彩的焰火,主要利用了“焰色反应”的知识
B . 航天员所穿航天服的主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料
C . “闽鹭”是我国制造的第四艘LNG船。船底镶嵌锌块,锌作正极,以防船体被腐蚀
D . 低碳生活需要节能减排,使用太阳能代替化石燃料,可减少温室气体的排放
|
|
| 2. 单选题 | 详细信息 |
|
有机物R被《科学》评为2021年度十大科学突破,原因是科学家发现其可治疗创伤后应激障碍。有机物R的结构简式如图所示。下列有关R的说法正确的是( )
A . 分子式为C11H13NO2
B . 与苯互为同系物
C . 能发生取代反应和加成反应
D . 苯环上的一氯代物有2种
|
|
| 3. 单选题 | 详细信息 |
|
设
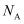 为阿伏加德罗常数的值,下列说法正确的是( ) 为阿伏加德罗常数的值,下列说法正确的是( )
A . 将
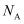 个 个  分子溶于1L水中得到 分子溶于1L水中得到  的氨水
B . 的氨水
B .  ,当0.5mol HCHO完全反应,转移的电子数为 ,当0.5mol HCHO完全反应,转移的电子数为  C . 在含
C . 在含  总数为 总数为 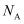 的 的  溶液中, 溶液中,  总数为 总数为  D . 常温下,
D . 常温下,  含有 含有 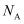 个 个  共价键 共价键
|
|
| 4. 单选题 | 详细信息 |
|
X、Y、Z、M、R为原子序数依次增大的短周期元素,Z、M、X、Y、R的族序数依次增大,X、Y的核电荷数之比为3∶4,Y、Z的原子序数之和与X、M的原子序数之和相等。下列说法正确的是( )
A . 简单离子半径:R>Y>Z>M
B . Y分别与X、Z、M、R形成的化合物中,Y的化合价相同
C . 由X、R组成的物质是常用的有机溶剂,易挥发,易燃烧
D . R分别与Z、M形成的化合物均为离子化合物
|
|
| 5. 单选题 | 详细信息 |
|
实验室从海带中提取碘的过程如下:
下列说法正确的是( )
A . 步骤①⑤分别用装置丙、甲完成
B . 装置乙使用时先放出下层水溶液,再从上口倒出有机层
C . 海带中含有的硫酸盐在步骤③中实现与碘的分离
D . 过程⑦酸化时发生反应的离子方程式:5I-+
 +6H+=3I2+3H2O +6H+=3I2+3H2O
|
|
| 6. 单选题 | 详细信息 | ||||||||||
|
室温下,通过下列实验探究亚硫酸盐的性质。已知:
 、 、  。 。
下列说法正确的是( )
A . 实验1得到的溶液中有
 B . 实验2得到的溶液中有
B . 实验2得到的溶液中有  C . 实验3得到的溶液中有
C . 实验3得到的溶液中有  D . 由实验4中可知:
D . 由实验4中可知: 
|
|||||||||||
| 7. 单选题 | 详细信息 |
|
氨气含氢量高,是一种安全、易储运的优良小分子储氢载体。利用电解原理,可将氨气转化为高纯氢气,其装置如图所示:
已知:起始时两极电解质溶液质量相等,法拉第常数
A . a为电源正极,阳极上的电极反应式为
 B . 反应一段时间后,右室KOH溶液中溶质的物质的量减小
C . 当电源输出8Ah电量时,产生的氢气在标准状况下的体积约为3.34L
D . 忽略气体溶解产生的质量变化,当电路中有0.1mol电子通过时,两室电解质溶液的质量差为1.8g
B . 反应一段时间后,右室KOH溶液中溶质的物质的量减小
C . 当电源输出8Ah电量时,产生的氢气在标准状况下的体积约为3.34L
D . 忽略气体溶解产生的质量变化,当电路中有0.1mol电子通过时,两室电解质溶液的质量差为1.8g
|
|
| 8. 实验探究题 | 详细信息 |
|
高铁酸钾
 为紫色固体,易溶于水,在KOH浓溶液中的溶解度较低,难溶于无水乙醇等有机溶剂,具有强氧化性,在酸性或中性溶液中不稳定,能产生 为紫色固体,易溶于水,在KOH浓溶液中的溶解度较低,难溶于无水乙醇等有机溶剂,具有强氧化性,在酸性或中性溶液中不稳定,能产生  ,在碱性溶液中较稳定且碱性越强越稳定。采用如图(夹持装置略)所示装置制备 ,在碱性溶液中较稳定且碱性越强越稳定。采用如图(夹持装置略)所示装置制备  并提纯。 并提纯。
|
|
| 9. 综合题 | 详细信息 |
|
锆矿石(主要成分为
 ,还含有 ,还含有  及钠、铝、铜的氧化物等杂质),一种以锆矿石为原料制备工业纯 及钠、铝、铜的氧化物等杂质),一种以锆矿石为原料制备工业纯  的工艺流程如图所示: 的工艺流程如图所示: 已知: 回答下列问题:
|
|
| 10. 综合题 | 详细信息 |
|
接触法制硫酸生产中的关键工序是
 的催化氧化( 的催化氧化(   )。回答下列问题: )。回答下列问题:
|
|
高中化学 试卷推荐
- 辽宁省沈阳市实验中学2021-2022学年高一上学期化学10月月考试卷
- 广东省乐昌第二高中2020-2021学年高二上学期化学期中考试试卷
- 浙江省宁波市2020-2021学年高一上学期化学期末考试试卷
- 福建省福州市2021-2022学年高一下学期期中质量抽测化学试题
- 浙江省宁波市2021年高考化学模拟试卷
- 浙江省宁波市慈溪市2020-2021学年高一下学期期末考试化学试题
- 黑龙江省大庆市2021年高考化学一模试卷
- 福建省龙岩市2022届高中毕业班第三次教学质量检测化学试题
- 重庆市九校联盟2021-2022学年高二上学期12月联考化学试题
- 天津市南开区2020-2021学年高三上学期化学期中考试试卷
- 河南省洛阳市2021年高考化学3月试卷
- 四川省绵阳市2022届高三第三次诊断性考试理综化学试题
最近更新
- 将下列各组物质按酸、碱、盐分类依次排列,正确的是( ) A.硫酸、纯碱、小苏打 B.磷酸、熟石
- 1、D(本项内容属于工业范畴) 2、C(“其演奏性能十分完美”有误;本项偷换概念,说法绝对化,不是“十分完美”,原文为“
- 化简:
- 骨髓移植能够治疗白血病,因为健康人的骨髓中有大量的造血干细胞,可不断产生新的血细胞(如图),这一过程称为细胞的(
- Mywife _______ some Korean(韩语)words when she watched the Ko
- 2009年9月8日,因无证醉酒驾车造成重大人员伤亡的孙伟铭,被四川省高级人民法院终审判处无期徒刑,剥夺政治权利终身。从此
- An old man lived alone in a town.He wanted to dig up his pot
- 设函数 (1)求的单调增区间及对称中心; (2)在中分别是角的对边,为锐角,若,,的周长为,求边长
- In Denmark, parents are allowed to set up a new school i
- 世贸组织要求,一旦货物已经进入某个市场,就必须获得不低于相同的当地制造商品所获得的优惠待遇。这体现了世贸组织的( )
- People with bigger brains tend to score higher on standardiz
- 设NA代表阿伏加德罗常数的数值,下列说法中正确的是 ( ) ①常温常压下,17 g重甲基(-14CD3
- 将过量的铁粉放入含AgNO3和Zn(NO3)2的混合溶液中,搅拌,使其充分反应后,过滤,滤液上留下的金属是 ( )
- When you are advised to “get an education” if you want to ra
- 如图所示.为了使道路交通更加通畅,宿迁市几条主干道架设了高架道路,高架道路的路面铺设“海绵”沥青,部分路段两侧设有高3
- 图是“我国九大商品粮生产基地分布图”,读图回答下列问题:(1)商品粮基地①与④相比,其不利的气候条 件是
- 反专制、追求个性解放在14-16世纪成为了西欧文学与中国文学鲜明的时代特征。下列作品能体现这一时代特征的作品是( )①
- 我们现在看来,孔子的话:“丘也闻有国有家者,不患寡而患不均,不患贫而患不安。”中不合理之处主要在于 A.违背了“社会公平
- 细胞内没有同源染色体的是( ) A.体细胞 B.精原细胞 C.初级精母细胞 D.次级精母细胞
- 已知货物的质量为m,在某段时间内起重机将货物以a的加速度加速升高h米,则在这段时间内叙述正确的是,重力加速度为g。



 溶液中通入11.2mL(标准状况)
溶液中通入11.2mL(标准状况) 
 溶液中通入22.4mL(标准状况)
溶液中通入22.4mL(标准状况)  溶液,溶液出现浑浊(20滴溶液体积约为1mL)
溶液,溶液出现浑浊(20滴溶液体积约为1mL)
 为阿伏加德罗常数与元电荷的乘积。下列说法正确的是。( )
为阿伏加德罗常数与元电荷的乘积。下列说法正确的是。( )
 ,理论上在装置D中生成
,理论上在装置D中生成  不能过量,原因是。
不能过量,原因是。
 充分反应后过滤,将滤液转移到250mL容量瓶定容。取25.00mL定容后的溶液于锥形瓶中,加入稀硫酸调至
充分反应后过滤,将滤液转移到250mL容量瓶定容。取25.00mL定容后的溶液于锥形瓶中,加入稀硫酸调至  ,滴加几滴二苯胺磺酸钠作指示剂,用
,滴加几滴二苯胺磺酸钠作指示剂,用  标准硫酸亚铁铵溶液滴定,终点时溶液由紫色变为绿色,消耗标准硫酸亚铁铵溶液14.40mL。已知测定过程中发生反应:
标准硫酸亚铁铵溶液滴定,终点时溶液由紫色变为绿色,消耗标准硫酸亚铁铵溶液14.40mL。已知测定过程中发生反应: 



 易溶于水,390℃会升华;
易溶于水,390℃会升华;  难溶于水,受热易分解。
难溶于水,受热易分解。
 ,写出生成该离子的离子方程式:。
,写出生成该离子的离子方程式:。
 表面反应生成
表面反应生成  的历程:
的历程: 




 、
、  和
和  ,起始时压强为p,进行反应
,起始时压强为p,进行反应  。平衡时,
。平衡时,  (以分压代替浓度计算,分压=总压×物质的量分数)。
(以分压代替浓度计算,分压=总压×物质的量分数)。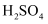 ,其工作原理如图所示,
,其工作原理如图所示, 
 和
和  ,当甲电极消耗
,当甲电极消耗  时,甲、乙两室中
时,甲、乙两室中 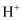 与
与  的总物质的量之比为。(两电极的产物均留在溶液中,忽略水的电离)
的总物质的量之比为。(两电极的产物均留在溶液中,忽略水的电离)


