高考二轮复习知识点:化学平衡的调控
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
在某温度下,将H2和I2各1mol的气态混合物充入1L的密闭容器中,发生反应:H2(g)+I2(g)⇌2HI(g)△H<0;5min后达到平衡状态,测得c(H2)=0.9mol•L﹣1 , 则下列结论中,不能成立的是( )
A . 平衡时H2、I2的转化率相等
B . 从反应开始至平衡的过程中,v(HI)=0.04mol•L﹣1•min﹣1
C . 其他条件不变再向容器中充入少量H2 , I2的转化率提高
D . 若将容器温度提高,其平衡常数K一定增大
|
|
| 2. 综合题 | 详细信息 |
|
甲醇是一种重要的有机化工原料,需求量巨大.目前我国独创的联醇工艺的核心是采用一氧化碳加氢中压合成法.主要反应如下:CO(g)+2H2(g)═CH3OH(g);△H=﹣111.0kJ/mol
另有副反应:2CO+2H2O═CO2+CH4 等;中压法操作:压力为10﹣15MPa,温度控制在513K﹣543K,所用催化剂是CuO﹣ZnO﹣Al2O3 . 合成甲醇的流程如图所示,
请回答:
|
|
| 3. 单选题 | 详细信息 |
|
电化学在化学实验、工业生产和生活中都有重要应用.下列说法正确的是( )
A . 实验室利用锌片和稀硫酸制H2时,在稀硫酸中滴加MgSO4溶液可以加快反应速率
B . 将反应2FeCl3+Cu═2FeCl2+CuCl2设计为原电池,正极反应为Cu﹣2e﹣═Cu2+
C . 利用电解法除去酸性废水中的CN﹣离子,CN﹣在阳极被还原为N2和CO2
D . 利用电解法精炼铜,原粗铜中的杂质有以离子形式被除去,也有以单质形式被除去
|
|
| 4. 综合题 | 详细信息 | |||||||||||||||||||||||||||||||
|
“绿水青山就是金山银山”,因此研究NOx、SO2等大气污染物的妥善处理具有重要意义。
|
||||||||||||||||||||||||||||||||
| 5. 单选题 | 详细信息 |
|
可逆反应xH2S(g)
 xH2(g)+Sx(g)(x>1)达到平衡后,下列说法错误的是( ) xH2(g)+Sx(g)(x>1)达到平衡后,下列说法错误的是( )
A . 若恒容充入H2 , 则新平衡后H2S分解率下降
B . 若增大压强,气体颜色变深,则Sx为有色气体
C . 若恒容升温后,气体密度不变,说明达到了新平衡
D . 若改变某一条件后,压强不能作为判断新平衡的标志,则Sx状态发生改变
|
|
| 6. 综合题 | 详细信息 |
|
探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ. Ⅱ. Ⅲ. 回答下列问题:
|
|
| 7. 综合题 | 详细信息 |
|
实验室以天青石精矿(主要含SrSO4 , 还含有少量SiO2、CaSO4、BaSO4)为原料制取SrSO4 , 其实验流程如下:
|
|
| 8. 多选题 | 详细信息 |
|
金属M的盐
 ,溶液中存在平衡: ,溶液中存在平衡:  。分别在 。分别在  恒温条件下,向 恒温条件下,向  的 的  ,溶液中加入等量 ,溶液中加入等量  固体,持续搅拌下用 固体,持续搅拌下用  传感器连续测量溶液的 传感器连续测量溶液的  ,得到实验图像,下列说法错误的是( ) ,得到实验图像,下列说法错误的是( )
A .
 B .
B .  时平衡常数的数量级是 时平衡常数的数量级是  C . 溶液中存在
C . 溶液中存在  D .
D .  温度下,加入 温度下,加入  ,固体再次达到平衡后, ,固体再次达到平衡后,  减小 减小
|
|
| 9. 单选题 | 详细信息 |
|
实验测得10 mL 0.50 mol·L-1NH4Cl溶液、10 mL 0.50mol·L-1CH3COONa溶液的pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时CH3COOH和NH3·H2O的电离常数均为1.8×10-5.下列说法错误的是( )
A . 图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B . 将NH4Cl溶液加水稀释至浓度
 mol·L-1 , 溶液pH变化值小于lgx
C . 随温度升高,Kw增大,CH3COONa溶液中c(OH- )减小,c(H+)增大,pH减小
D . 25 ℃时稀释相同倍数的NH4Cl溶液与CH3COONa溶液中:c(Na+ )-c(CH3COO- )=c(Cl-)-c(NH mol·L-1 , 溶液pH变化值小于lgx
C . 随温度升高,Kw增大,CH3COONa溶液中c(OH- )减小,c(H+)增大,pH减小
D . 25 ℃时稀释相同倍数的NH4Cl溶液与CH3COONa溶液中:c(Na+ )-c(CH3COO- )=c(Cl-)-c(NH  ) )
|
|
| 10. 单选题 | 详细信息 |
|
在298.15 K、100 kPa条件下,N2(g) +3H2 (g)=2NH3(g) ΔH=-92.4 kJ·mol-1 , N2 (g) 、H2(g)和NH3(g)的比热容分别为29.1、28.9和35.6J·K-1·mol-1。一定压强下,1 mol反应中,反应物[N2(g) +3H2(g)]、生成物[2NH3(g)]的能量随温度T的变化示意图合理的是( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
- 北京市大兴区2021-2022学年高二上学期期中考试化学试题
- 福建省福州市八县(市)协作校2021-2022学年高二上学期期中联考化学试题
- 福建省三明市教研联盟校2021-2022学年高二上学期期中联考化学试题
- 江苏省常熟市2021-2022学年高二上学期期中考试化学试题
- 江苏省淮安市高中校协作体2021-2022学年高二上学期期中考试化学(选修)试题
- 江苏省宿迁市沭阳县2021-2022学年高二上学期期中调研测试化学试题
- 江苏省徐州市2021-2022学年高二上学期期中考试化学试题
- 辽宁省六校2021-2022学年高二上学期期中考试化学试题
- 山西省怀仁市2021-2022学年高二上学期期中化学试题
- 山西省太原市2021-2022学年高二上学期期中考试化学试题
- 福建省福州市福清市高中联合体2021-2022学年高一上学期期中考试化学试题
- 江苏省常熟市2021-2022学年高一上学期期中化学试题
- 若 .
- 已知某几何体的三视图如图,其中正(主)视图中半圆的半径为1,则该几何体的体积为() A.24﹣ B.24﹣
- 阅读下文最后一根皮带①走进成都军区某红军团4连的荣誉室,一张黑白照片格外醒目,照片里仅有一条被截去一段的老式牛皮皮带,皮
- 若,则的值为 ( ) A. B.
- 有广告宣称,普通股民通过专门培训,就能轻松掌握并实现零风险前提下的利润最大化。该广告不可信,因为() ①股票是高收益与高
- 图中纵坐标表示数值大小,横坐标表示纬度,据此完成下列问题。 (1)该图表达的是( ) A.年太阳辐射量的纬度分布
- 计算: (1)(ab2)2·(-a3b)3÷(-5ab);
- 可能存在的第119号元素,有人称“类钫”,据周期表结构及元素性质变化趋势,有关“类钫”的预测说法正确的是: A.“类
- 据报道,最近中科院的有关专家在世界上首次发现了镨元素的一种新的同位素,它的中子数为A.330 B.
- 右图中S表示太阳,说法正确的是( )A.此图包含三级天体系统B.图中b一定是地球C.图中b是卫星 D.图中a有可
- 梭伦说:“我给予了一般人民以恰好足够的权力,亦不使他们失掉尊严,也不给他们太多。”文中的“他们”是指 A.贵族
- Rescuers had to _____ the search because of worsening weathe
- -What’s the best way of losing weight? - A.Wh
- 如图所示,空气中有一折射率为Ã的玻璃柱体,其横截面是圆心角为90°、半径为R的扇形OAB.一束平行光平行于横截面,以45
- 2001年7月13日,莫斯科(东3区)当地时间下午5时20分,宣布北京获得2008年夏季奥运会主办权。请问家住北京的李先
- 已知下列热化学方程式: C(s)+O2(g)====CO2(g);ΔH=-393.5 kJ·mol-1H2(g)+O2(
- 已知某混合金属粉末,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合物金属粉末中铁、
- 下图四支蜡烛都将熄灭,其中一支熄灭的原因与另外三支不同的是( )
- 已知圆柱与圆锥的底面积相等,高也相等,它们的体积分别为V1和V2,则V1:V2=( ) A. 1:3
- 下列各句中加点的成语使用恰当的一句是( ) A.正因为科学是一把“双刃剑”,所以,先进的医疗技术既有可能解除病人的

 O(NO气体)
O(NO气体) 
 =(计算结果用分数表示)
=(计算结果用分数表示)







 。
。




 (aq)
(aq)  SrCO3(s)+SO
SrCO3(s)+SO 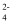 (aq)达到平衡,则反应的平衡常数为[Ksp(SrSO4)=3.2×10−7 , Ksp(SrCO3)=5.6×10−10]。
(aq)达到平衡,则反应的平衡常数为[Ksp(SrSO4)=3.2×10−7 , Ksp(SrCO3)=5.6×10−10]。






