山西省吕梁市柳林县2021-2022学年高二上学期期中考试化学试题
山西省吕梁市柳林县2021-2022学年高二上学期期中考试化学试题
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
一种“即食即热型快餐”适合外出旅行时使用.其内层是用铝箔包裹的、并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是( )
A . 浓硫酸与水
B . 生石灰与水
C . 熟石灰与水
D . 氯化钠与水
|
|
| 2. 单选题 | 详细信息 |
|
根据vt图分析外界条件改变对可逆反应A(g)+3B(g)
可见在t1、t3、t5、t7时反应都达到平衡,如果t2、t4、t6、t8时都只改变了一个反应条件,则下列对t2、t4、t6、t8时改变条件的判断正确的是( )
A . 使用了催化剂、增大压强、减小反应物浓度、降低温度
B . 升高温度、减小压强、减小反应物浓度、使用了催化剂
C . 增大反应物浓度、使用了催化剂、减小压强、升高温度
D . 升高温度、减小压强、增大反应物浓度、使用了催化剂
|
|
| 3. 单选题 | 详细信息 |
|
在密闭容器中发生下列反应aA(g)+bB(g)
 cC(g)+dD(s),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.6倍,下列叙述正确的是( ) cC(g)+dD(s),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.6倍,下列叙述正确的是( )
A . A的转化率变大
B . B的体积分数变大
C . 平衡向正反应方向移动
D . a+b>c
|
|
| 4. 单选题 | 详细信息 |
|
为减少温室气体的排放,科学家研究出以
 为催化剂,光热化学循环分解 为催化剂,光热化学循环分解  的反应,该反应机理及各分子化学键完全断裂时的能量变化如下图所示。 的反应,该反应机理及各分子化学键完全断裂时的能量变化如下图所示。 下列说法正确的是( )
A . 该反应中,光能和热能转化为化学能
B . 该过程中没有电子的转移
C . 使用
 作催化剂可以降低反应的焓变,从而提高化学反应速率
D . 分解 作催化剂可以降低反应的焓变,从而提高化学反应速率
D . 分解  反应的热化学方程式: 反应的热化学方程式: 
|
|
| 5. 单选题 | 详细信息 |
|
用H2O2和H2SO4的混合溶液可溶出废旧印刷电路板上的铜。已知:
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH1=+64.39 kJ·mol-1 ②2H2O2(l)=2H2O(l)+O2(g) ΔH2=-196.46 kJ·mol-1 ③H2(g)+ 在H2SO4溶液中,1 mol Cu(s)与H2O2(l)反应生成Cu2+(aq)和H2O(l)的反应热ΔH等于( )
A . -319.68 kJ·mol-1
B . -417.91 kJ·mol-1
C . -448.46 kJ·mol-1
D . +546.69 kJ·mol-1
|
|
| 6. 综合题 | 详细信息 |
|
二甲醚(DME)被誉为“21世纪的清洁燃料”,由合成气制备二甲醚的主要原理如下:
①CO(g)+2H2(g) ②2CH3OH(g) ③CO(g)+H2O(g) 回答下列问题:
|
|
| 7. 综合题 | 详细信息 |
|
N2O和CO是常见的环境污染气体。
|
|
| 8. 单选题 | 详细信息 |
|
在一定条件下,N2和O2反应生成NO的能量变化如图所示,总反应的焓变ΔH>0,下列说法正确的是( )
A . ΔH1<ΔH2
B . ΔH1<0ΔH3>0
C . |ΔH1+ΔH2|>|ΔH3|
D . ΔH=ΔH1+ΔH2+2ΔH3
|
|
| 9. 单选题 | 详细信息 |
|
下列有关热化学方程式书写与对应表述均正确的是( )
A . 稀硫酸与
 NaOH溶液反应: NaOH溶液反应: B . 在101kPa下
B . 在101kPa下 的燃烧热 的燃烧热 , 则水分解的热化学方程式为 , 则水分解的热化学方程式为 C . 已知
C . 已知 的燃烧热 的燃烧热 , 则有 , 则有 D . 已知9.6g硫粉与11.2g铁粉混合加热生成17.6g FeS时放出19.12kJ热量,则
D . 已知9.6g硫粉与11.2g铁粉混合加热生成17.6g FeS时放出19.12kJ热量,则
|
|
| 10. 单选题 | 详细信息 |
|
接触法制硫酸生产中的关键工序是SO2的催化氧化:2SO2(g)+O2(g)
 2SO3(g) △H=-196kJ·mol-1。钒催化剂参与反应的能量变化如图所示。下列说法正确的是( ) 2SO3(g) △H=-196kJ·mol-1。钒催化剂参与反应的能量变化如图所示。下列说法正确的是( )
A . 钒催化剂改变了SO2催化氧化的反应热
B . 上述条件下加入2molSO2和1molO2发生反应,释放的能量等于196kJ
C . 1molV2O4(s)的能量比2mol VOSO4(s)的能量多399kJ
D . 2V2O5(s)+2SO2(g)=2VOSO4(s)+V2O4(s) △H=-351kJ·mol-1
|
|
高中化学 试卷推荐
- 2015年湖南省长沙市高考化学模拟试卷(4月份)
- 第9讲:碳族元素 无机非金属材料
- 广西靖西市第二中学2019-2020学年高二下学期化学开学考试卷
- 内蒙古包头市2020年高考化学一模试卷
- 北京市西城区2015-2016学年高一上学期化学期末考试试卷
- 安徽省合肥市2019-2020学年高二下学期化学开学考试卷
- 辽宁省阜新市第二高级中学2019-2020学年高一下学期化学期末考试试卷
- 天津市红桥区2020年高考化学二模试卷
- 天津市和平区2017-2018学年高三上学期化学期末考试试卷
- 广东省惠州市2018-2019学年高一上学期化学期末考试试卷
- 高中化学人教版(2019)必修第一册 第二章第三节 物质的量
- 四川省凉山彝族自治州2019-2020学年高一下学期化学期末考试试卷
最近更新
- 在做电解水实验时,常在水中加入氢氧化钠来增强溶液的导电性,但氢氧化钠本身不会发生化学反应,质量也不会发生改变.现将含有8
- 高温下,某反应达到平衡,平衡常数 恒容时,温度升高,H2浓度减小。下列说法
- 北京晚报2010年3月8日消息:全国政协委员、中国电影文学学会会长王兴东特别关注选举权和选举法,建议尽量使用差额选举。差
- 阅读下面的文字,根据要求作文。 (1)87岁的中国画家吴冠中先生,2006年在香港中文大学接受荣誉文学博士称号时说:“如
- ( )57. Please don't forget _______to me, will you?
- 分别用以下三组物质比较锌和铜的金属活动性:①Zn、Cu、稀硫酸;②Zn、Cu、 MgSO4 溶液;③Zn、CuSO4溶
- 如图所示,使用中属于费力杠杆的工具是
- 如图所示,已知α=125°,γ=52°,则β=______.
- (08黄埔区4月模拟)N5是破坏力极强的炸药之一,是比黄金还贵重的物质。下列说法正确的是()A.N5和N2互为同位素
- 下列物质的用途主要利用其化学性质的是() A.氦气用于填充探空气球 B.天然气用作燃料 C.活性炭用于净化水质 D.
- 下列关系式中正确的是( ) A. B. C. D.
- 在Rt△ABC中,∠C=90°,DE是AB的垂直平分线,且∠BAD∶∠BAC=1∶4,求∠B的度数.
- 关于五代辽宋夏金元时期历史特点的表述,正确的是( )①国家从分裂割据、若干民族政权并立逐渐走向统一 ②商品经济发
- 下列各组词语中,没有错别字的一组是( ) A.处心极虑 老奸巨猾 鬼鬼祟祟 出类拔瘁w@w!w$.k#s%5
- 在现实的社会经济生活中,我们会经常碰到这样的情景:购买商品时候,当消费者向商家索要发票时,消费者就要多付钱;如果不需要
- 下列现象是由于地球自转产生的是( )A.四季的变化 B.昼夜更替C.太阳升落时间的早晚D.正午时刻物体影
- In ancient Japan, if you saved someone’s life, they would ma
- 古希腊智者学派思想家伊壁鸠鲁认为,国家起源于人民相互之间的契约;法国政治思想家卢梭认 为,基于全体人民的“共同意志”
- 若|a|=2,|b|=4,且(a+b)⊥a,则a与b的夹角为 .
- 春秋时期,我国在生产工具方面的变革主要是 A.出现青铜工具 B.出现铁农具 C.开始兴修水利


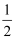 O2(g)=H2O(1) ΔH3=-285.84 kJ·mol-1
O2(g)=H2O(1) ΔH3=-285.84 kJ·mol-1 CH3OH(g) ΔH1=-90.7kJ·mol-1 K1
CH3OH(g) ΔH1=-90.7kJ·mol-1 K1 =2通入1L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)
=2通入1L的反应器中,一定条件下发生反应:4H2(g)+2CO(g) 
 约为时最有利于二甲醚的合成。
约为时最有利于二甲醚的合成。 
 CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:
CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:







