河北省张家口市2020-2021学年高二上学期化学期中考试试卷
河北省张家口市2020-2021学年高二上学期化学期中考试试卷
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
某物质的水溶液能导电,且该物质属于非电解质,则溶于水时化学键被破坏的是( )
A . 乙醇
B . 干冰
C . 蔗糖
D . 硫酸钠
|
|
| 2. 单选题 | 详细信息 |
|
下列物质在水溶液中的电离方程式书写正确的是( )
A . H2CO3
 2H++CO 2H++CO 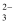 B . Ba(OH)2
B . Ba(OH)2  Ba2++2OH-
C . NaHCO3=Na++H++CO Ba2++2OH-
C . NaHCO3=Na++H++CO 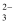 D . AlCl3=Al3++3Cl-
D . AlCl3=Al3++3Cl-
|
|
| 3. 单选题 | 详细信息 |
|
下列反应在任何温度下均能自发进行的是( )
A . 2N2(g)+O2(g)=2N2O(g)△H>0
B . 3SiCl4(g)+2H2(g)+Si(s)
 4SiHCl3(g)△H<0
C . COCl2(g) 4SiHCl3(g)△H<0
C . COCl2(g)  CO(g)+Cl2(g)△H>0
D . 2H2O2(l)=2H2O(l)+O2(g)△H<0 CO(g)+Cl2(g)△H>0
D . 2H2O2(l)=2H2O(l)+O2(g)△H<0
|
|
| 4. 单选题 | 详细信息 |
|
下列事实能用勒夏特列原理解释的是( )
A . 黄绿色的氯水光照后颜色变浅
B . 将铜粉和锌粉混合后放入稀硫酸中,产生气体的速率比不加铜粉快
C . H2、I2(g)、HI混合气体加压后颜色变深
D . 工业制硫酸中,SO2氧化成SO3 , 往往需要使用催化剂
|
|
| 5. 单选题 | 详细信息 |
|
反应SiCl4(g)+2H2(g)
 Si(s)+4HCl(g)△H>0,可用于纯硅的制备。下列有关该反应的说法正确的是( ) Si(s)+4HCl(g)△H>0,可用于纯硅的制备。下列有关该反应的说法正确的是( )
A . 反应物的总能量高于生成物的总能量
B . 该反应的平衡常数K=
 C . 其他条件不变,加入合适催化剂可加快反应速率,同时提高Si的产量
D . 升温或加压均可增大SiCl4的转化率
C . 其他条件不变,加入合适催化剂可加快反应速率,同时提高Si的产量
D . 升温或加压均可增大SiCl4的转化率
|
|
| 6. 单选题 | 详细信息 |
|
在25℃时,用蒸馏水稀释1mol·L-1草酸至0.01mol·L-1 , 随溶液的稀释,下列各项中始终保持增大趋势的是( )
A .
 B .
B .  C .
C .  D . c(H+)
D . c(H+)
|
|
| 7. 单选题 | 详细信息 |
|
丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。
已知:①C4H10(g)+ ②H2(g)+ 丁烷(C4H10)脱氢制丁烯(C4H8)的热化学方程式为C4H10(g) 下列叙述正确的是( )
A . △H3=-123kJ·mol-1
B . 其他条件不变时,反应平衡后升高温度,能提高该反应中丁烯产率
C . 恒温恒容条件下,反应平衡后再充入C4H10(g),混合气体中丁烯的百分含量增大
D . 其他条件不变时,反应平衡后增大压强,能提高该反应中丁烯产率
|
|
| 8. 单选题 | 详细信息 |
|
一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
A . 该反应的化学方程式为3B+4C=6A+2D
B . 从反应开始到1 s时,v(A)=v(C)
C . 反应进行到6 s时,B的平均反应速率为0.05 mol·L-1·s-1
D . 反应进行到6 s时,各物质的反应速率相等
|
|
| 9. 单选题 | 详细信息 |
|
对于反应2SO2(g)+O2(g)
 2SO3(g)△H<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图像不相符的是( ) 2SO3(g)△H<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图像不相符的是( ) (t1时刻v正=v逆;t1时改变条件,t2时重新建立平衡)
A . 加入催化剂
 B . 增加SO3浓度
B . 增加SO3浓度  C . 升高温度
C . 升高温度  D . 增大压强
D . 增大压强 
|
|
| 10. 单选题 | 详细信息 | ||||||||||||
|
COS(结构式为O=C=S)是煤气中主要的含硫杂质之一,煤气燃烧后含硫杂质会转化成SO2从而引起大气污染。利用H2还原法脱除煤气中COS可能使工业气体总含硫量降至环保要求,相关反应为H2(g)+COS(g)=H2S(g)+CO(g)。已知断裂1mol化学键所需的能量如表所示。则该反应的△H为( )
A . +8kJ·mol-1
B . -8kJ·mol-1
C . +347kJ·mol-1
D . -347kJ·mol-1
|
|||||||||||||
高中化学 试卷推荐
- 高中化学人教版(2019)选择性必修1 第四章第一节 原电池
- 河北省邯郸市2017-2018学年高一上学期化学期中考试试卷
- 河北省邢台市2017-2018学年高三上学期理综-化学期末考试试卷
- 天津市五区县2016-2017学年高一上学期化学期末考试试卷
- 2015-2016学年江西省赣州市高一上学期期末化学试卷
- 广东省中山市2017-2018学年高二上学期化学期末考试试卷
- 北京市房山区2017-2018学年高考理综-化学一模考试试卷(4月)
- 四川省广安、眉山、内江、遂宁2017-2018学年高考理综-化学三模考试试卷
- 辽宁省大连市2017-2018学年高考理综-化学一模考试试卷
- 河北省邢台市2018-2019学年高三上学期化学第四次月考试卷
- 2015-2016学年河南省信阳市鸡公山风景区学校高三下学期月考化学试卷(2月份)
- 2017年浙江省高考化学模拟卷
最近更新
- 根据所给材料,回答下列问题。 材料一 喀斯特地貌(Karst landform)指可溶性岩石(主要是分布最广的碳酸盐岩
- 仿照下面的一段话,另写一段话,要求句式、修辞一致。 风从水上走过,留下粼粼波纹;骆驼人沙漠上走过,留下深深的脚印;哨鸽从
- They went right to Berlin by __ airinstead of taking a ride
- Would you mind if I played the violin here? — A.No,
- 用下列10种物质的序号,填空回答问题:①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2
- 一定温度下,用水稀释amol・L-1的稀醋酸,若用KW表示水的离子积,Ka表示CH3COOH的电离常数,则下列数值随水量
- Pop music is loved by lots of people, but it is not everyone
- 讽刺19世纪上半期中国社会现象的一副对联写道:“竹枪一支,打得妻离子散,未闻炮20070227 声震地,铜灯半盏,烧
- The pen _________him ten yuan. A. paid B. cost C.took D. spe
- 13、“不特别注意城市工作,想以‘乡村包围城市’……是一种极错误的观念。”这一材料反映了()。 A.中国革命必须以城市为
- 如图所示,A、B,C、D, E、F为处于勻强电场中一个边长为1Ocm的正六边形的六个顶点,A、B、C三点电势分别为1.0
- 过点A(0,2)可以作___条直线与双曲线x2-=1有且只有一个公共点
- 下列判断中一定正确的是( ) A.CaCl2及CaO2固体中阴、阳离子数之比均为2∶1 B.等质量的O2与O3中
- 我国耕地资源有限,要提高粮食产量,科学施肥是重要措施之一。农业技术员小王测定了某块耕地的耕层土壤氮磷钾含量,测定结果及土
- (本题满分18分)第一题满分4分,第二题满分6分,第三题满分8分.已知椭圆的长轴长是焦距的两倍,其左、右焦点依次为、,抛
- 第二节 信息匹配(共5小题;每小题2分,满分10分) 下面是一篇应用文及其应用场合的信息,请阅读下列应用文和相关信息,
- 公元前480年,波斯入侵雅典。最终雅典人决定放弃雅典城,全体公民上船与波斯人决战。作出这一决定的应该是() A.公民大会
- (北京卷理8文8)如图,动点在正方体的对角线上.过点作垂直于平面的直线,与正方体表面相交于.设,,则函数的图象大致是(
- 隋唐的三省六部制完善了自秦以来的中央集权制,其积极作用主要在于 ( ) A.解决了中央与地方的矛盾
- (几何证明选讲选做题)如图,已知⊙O的割线PAB交⊙O于A,B两点,割线PCD经过圆心,若PA=3,AB=4,PO=5,
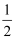 O2(g)=C4H8(g)+H2O(g)△H=-119kJ·mol-1
O2(g)=C4H8(g)+H2O(g)△H=-119kJ·mol-1
 O
O


