2017年北京市昌平区高考化学二模试卷
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 | ||||||||
|
下列电池工作时能量转化形式与其它三个不同的是( )
A . A
B . B
C . C
D . D
|
|||||||||
| 2. 单选题 | 详细信息 |
|
下列解释事实的方程式不正确的是( )
A . 焊接铁轨:2Fe+Al2O3
 2Al+Fe2O3
B . 工业固氮:N2+3H2 2Al+Fe2O3
B . 工业固氮:N2+3H2  2NH3
C . 用纯碱除油污:CO32﹣+H2O⇌HCO3﹣+OH﹣
D . 用湿润的淀粉KI试纸检验Cl2:Cl2+2I﹣═2Cl﹣+I2 2NH3
C . 用纯碱除油污:CO32﹣+H2O⇌HCO3﹣+OH﹣
D . 用湿润的淀粉KI试纸检验Cl2:Cl2+2I﹣═2Cl﹣+I2
|
|
| 3. 单选题 | 详细信息 |
|
关于a:0.1mol/L NH4Cl溶液和b:0.1mol/L NH3•H2O溶液,下列说法不正确的是( )
A . 两溶液中存在的微粒种类:a>b
B . c(NH4+):a>b
C . c(OH﹣):a<b
D . 水电离出的c(H+):a<b
|
|
| 4. 单选题 | 详细信息 |
|
某离子反应涉及到H2O、ClO﹣、NH4+、OH﹣、N2、Cl﹣等微粒,其中N2、ClO﹣的物质的量随时间变化的曲线如图所示,下列说法正确的是( )
A . 该反应中Cl﹣为氧化产物
B . 消耗1 mol还原剂,转移6 mol电子
C . 反应后溶液的酸性减弱
D . NH4+被ClO﹣氧化成N2
|
|
| 5. 单选题 | 详细信息 |
|
下列说法正确的是( )
A . 葡萄糖制镜利用了葡萄糖的氧化性
B . 室温下,在水中的溶解度:乙醇>苯酚>乙酸乙酯
C . 酯在碱性条件下水解生成对应的酸和醇
D . 甲苯能使酸性高锰酸钾溶液褪色,说明甲基使苯环变活泼
|
|
| 6. 单选题 | 详细信息 | ||||||||||||||||||||
|
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 7. 单选题 | 详细信息 |
|
常温时,用0.1000mol/L NaOH溶液滴定25.00mL 0.1000mol/L某一元酸HX溶液,滴定过程中pH变化曲线如图所示.下列说法不正确的是( )
A . 在A点:c(HX)>c(Na+)>c(X﹣)
B . 在B点,溶液中c(H+)=c(OH﹣)
C . C点溶液中存在的主要平衡是X﹣+H2O⇌HX+OH﹣
D . 0.05mol/L NaX溶液的pH≈9
|
|
| 8. 综合题 | 详细信息 |
|
天然产物萜类化合物eudesmane合成路线片段如图.(某些反应条件省略)
已知: i.RCHO+R′﹣CH2﹣CHO ii.RMgX+ iii. 回答下列问题:
|
|
| 9. 综合题 | 详细信息 |
|
磷石膏(主要成分是CaSO4•2H2O)是磷酸及磷肥类工业在生产过程中产生的一种废渣,我国每年排放的磷石膏大约2000万吨以上,开发利用磷石膏,保护资源和环境,符合持续发展的观念.图1所示为对磷石膏进行综合利用的路径之一.
|
|
| 10. 综合题 | 详细信息 | ||||||||||
|
纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用.
|
|||||||||||
- 河北省保定市定兴中学2019-2020学年高二下学期化学4月线上月考试卷
- 吉林省长春市2020年高考理综-化学二模试卷
- 2015-2016学年江西省上饶市广丰县一中高一上学期第二次月考化学试卷(星)
- 2016-2017学年江苏省连云港市锦屏高中高一上学期期中化学试卷
- 北京市昌平区2016-2017学年高三上学期化学期末考试试卷
- 吉林省松原市前郭尔罗斯蒙古族自治县蒙古族中学2019-2020学年高二下学期化学线上月考试卷
- 2015-2016学年陕西省西安市交通大学二附中高二上学期第二次月考化学试卷
- 备考2018年高考化学一轮基础复习:专题16 微粒之间的相互作用力
- 福建省泉州市2019-2020学年高一下学期化学期末考试试卷
- 2015-2016学年吉林省延边州汪清六中高二上学期第二次月考化学试卷
- 高中化学人教版(2019)必修第二册第六章 第二节 化学反应的速率与限度
- 2016年广东省广州市高考化学模拟试卷(1月份)
- 6分)现代家庭装修中浴室大多用燃气热水器提供热水,小芳家安装了燃气热水器。已知水进入热水器前的温度是100C,洗澡时热水
- 下列关于季风水田农业特点的叙述错误的是A.田地规模小,机械化水平低 B.科技水平低,水利工程量大C.单位面积产
- If I had worked harder at school, I ___ in a comfortable of
- 下列各项中,加点的成语使用不恰当的一项是 A.这个少年心机深沉,竟在十年前便开始布置这个圈套,他处心积虑,步步为营,阴狠
- 如图所示,、两城市相距,现计划在这两座城市间修建一条高速公路(即线段),经测量,森林保护中心在城市的北偏东和城市的北偏西
- 若x2﹣4x+p=(x+q)2,则pq=______.
- The Prime Minister refused to comment on the rumor that he h
- 我国的国家机构实行民主集中制的组织和活动原则,这是由 A.我国的国体和政体共同决定的 B.我国的经济基础和人民民主专政的
- 阅读下面的短文,然后按照要求写一篇150词左右的英语短文。 In junior high school, one of
- 阅读下面两首诗,完成1~2题。 送沈子福之江东唐 王维 杨柳渡头行客稀,罟师荡桨向临圻。 惟有相思似春色,江南江北送君归
- 关于x的不等式对一切实数x都成立,则a的范围是 ;
- 请完成有关氨气的问题。(1)实验室常用下列装置和选用的试剂制取NH3,其中正确的是__________(填序号)。(2)
- 读我国海峡西岸经济区及附近地区某月等温线和年等降水量(mm)分布图、福建地形示意图,回答下列问题。(1)图1所示为何月(
- 若将抛物线y=x2向右平移2个单位,再向上平移3个单位,则所得抛物线的表达式为()A. y=(x+2)2+3 B. y=
- 已知全集U=R,集合,集合,则 ( )
- 右图表示气温、降水与气候类型的关系。读图,回答8~10题:8.年温差最大的一组气候类型是 ( )A.①②⑥ B
- 《唐山大地震》上映不足半个月,票房已经超过3亿。优秀的文化产品,就是这个时代的阳光,永远温暖震撼着我们的心灵。优秀作品的
- 哲学要研究的问题有许多,其中有一个贯穿哲学发展始终的基本问题,即( ) A.思维和存在的关系 B.主观精神与客观精神
- 数列{an}中,an>0,且{anan+1}是公比为q(q>0)的等比数列,满足anan+1+an+1an+2>an+2
- 数列{an}中,a1,a2-a1,a3-a2,…,an-an-1…是首项为1、公比为的等比数列,则an等于












 .
.

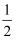 H2O(s)+
H2O(s)+  H2O(g)△H1=+83.2KJ•mol﹣1
H2O(g)△H1=+83.2KJ•mol﹣1





