安徽省宣城市2020年高考理综-化学二模试卷
安徽省宣城市2020年高考理综-化学二模试卷
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
化学与生产生活关系密切。下列有关说法错误的是( )
A . 港珠澳大桥使用的超高分子量聚乙烯纤维属于有机高分子化合物
B . 质谱法是测定有机物相对分子质量及确定化学式的分析方法之一
C . “玉兔二号”月球车使用的帆板太阳能电池的材料是
 D . 宋·王希孟《千里江山图》卷中绿色颜料“铜绿”的主要成分是碱式碳酸铜
D . 宋·王希孟《千里江山图》卷中绿色颜料“铜绿”的主要成分是碱式碳酸铜
|
|
| 2. 单选题 | 详细信息 |
|
设
 为阿伏加德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是: 为阿伏加德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是:  。下列说法正确的是( ) 。下列说法正确的是( )
A . 如果氯气管道漏气,则会看到有大量白雾生成
B . 反应中每形成
 键,转移电子数为 键,转移电子数为  C .
C .  的 的  溶液中, 溶液中,  的数目小于 的数目小于  D . 该反应中,氧化剂与还原剂的物质的量之比为
D . 该反应中,氧化剂与还原剂的物质的量之比为 
|
|
| 3. 单选题 | 详细信息 | ||||||||||||||||
|
乙酸异戊酯是蜜蜂信息素的成分之一,具有香蕉的香味。实验室中可利用乙酸和异戊醇
A . 反应方程式为CH3COOH+
 |
|||||||||||||||||
| 4. 单选题 | 详细信息 |
|
微生物燃料电池(MFC)为可再生能源的开发和难降解废弃物的处理提供了一条新途径。某微生物燃料电池示意图如图所示(假设废弃物为乙酸盐)。下列说法错误的是( )
A . 甲室菌为好氧菌,乙室菌为厌氧菌
B . 甲室的电极反应式为
 C . 该微生物燃料电池(MFC)电流的流向:由b经导线到a
D . 电池总反应式为
C . 该微生物燃料电池(MFC)电流的流向:由b经导线到a
D . 电池总反应式为 
|
|
| 5. 单选题 | 详细信息 |
 和 和  为原子序数依次增大的短周期元素, 为原子序数依次增大的短周期元素,  同主族且能形成离子化合物, 同主族且能形成离子化合物,  的最外层电子数是 的最外层电子数是  质子数之和的一半, 质子数之和的一半,  原子的核外电子数为偶数。四种元素组成的一种化合物 原子的核外电子数为偶数。四种元素组成的一种化合物 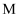 具有下列性质。下列说法正确的是( ) 具有下列性质。下列说法正确的是( ) 白色沉淀
A . 原子半径:
 B .
B . 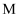 使溴水褪色体现氧化性
C . 简单氢化物的稳定性: 使溴水褪色体现氧化性
C . 简单氢化物的稳定性:  D .
D .  与 与  均能形成具有漂白性的物质 均能形成具有漂白性的物质
|
|
| 6. 单选题 | 详细信息 | ||||||||||||||||||||
|
下列有关实验现象和解释或结论都正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 7. 单选题 | 详细信息 |
|
常温下,向
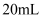 浓度均为 浓度均为  和 和  的混合溶液中滴加 的混合溶液中滴加  的 的  ,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积 ,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积 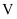 的关系如图所示(忽略混合时体积变化),下列说法正确的是( ) 的关系如图所示(忽略混合时体积变化),下列说法正确的是( )
A . 常温下,
 的 的  比同浓度 比同浓度  的 的  大
B . 大
B .  过程中水的电离程度先减小后增大
C . 过程中水的电离程度先减小后增大
C . 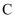 点溶液中, 点溶液中,  D .
D .  点时, 点时, 
|
|
| 8. 综合题 | 详细信息 |
|
硫酸镍广泛应用于电镀、电池、催化剂等工业。某科研小组以粗硫酸镍(含
 等)为原料,经如图一系列除杂过程模拟精制硫酸镍工艺。回答下列问题。 等)为原料,经如图一系列除杂过程模拟精制硫酸镍工艺。回答下列问题。
|
|
| 9. 实验探究题 | 详细信息 | |||||||||||||
|
某小组探究
 溶液和 溶液和  溶液的反应原理。 溶液的反应原理。
|
||||||||||||||
| 10. 综合题 | 详细信息 | ||||||||||||||||||||||||||
|
甲醇是一种可再生能源,具有广阔的开发和应用前景,可用
 等作为催化剂,采用如下反应来合成甲醇: 等作为催化剂,采用如下反应来合成甲醇: 
|
|||||||||||||||||||||||||||
高中化学 试卷推荐
- 江苏省泰州市2020年高考化学二模试卷
- 备考2019年高考化学二轮专题 07 电化学及其应用
- 2016-2017学年广西钦州市高新区高二上学期期末化学试卷
- 2015-2016学年山东省枣庄四中高三上学期开学化学试卷
- 高中化学人教版(2019)选择性必修1 第三章第一节 电离平衡
- 2017_2018学年高中化学人教版选修三 课时训练12晶体的常识
- 广东省潮州市2019-2020学年高二下学期化学期末考试试卷
- 福建省永泰县第一中学2018-2019学年高二上学期化学期末考试试卷
- 2016-2017学年江西省吉安三中高三上学期期中化学试卷
- 安徽省颍上三校联考2019-2020学年高三上学期化学第一次月考试卷
- 江苏省扬州市2019-2020学年高二学业水平合格性考试模拟试卷(二)
- 辽宁省重点高中协作校2017-2018学年高考理综-化学二模考试试卷
最近更新
- 若集合A={x|﹣1<x<2},B={x|2x2﹣5x﹣3>0},则A∩B=() A.{x|﹣1<x<﹣,或2<x<3}
- .5的相反数是 A.﹣5 B.5 C.D.
- 下列物质中,不属于卤代烃的是( ) A.氯乙烯
- 已知一个三棱锥的正(主)视图与俯视图如图所示,则该三棱锥的侧(左)视图的面积为()A. B. C.1 D.
- 利用如图所示装置进行实验,仪器a、b、c中分别盛装下列试剂,试管c中现象描述正确的是()选项 a b c c试管中现象
- 下列计算错误的是() A.(a3b)•(ab2)=a4b3 B.(﹣mn3)2=m
- 除去下列各组物质中的杂质(括号内为杂质),所选用的除杂方法错误 的是 选项 物质 除杂方法 A N2(O2) 通
- (09年济宁质检)(12分)已知点(1)若,求的值;(2)若,其中为坐标原点,求的值。
- 位于烟台市中部的东李家庄村是一个普通的小村,随着初冬的到来,人们除了忙着采摘买卖苹果、修理农具外,村里早晚串门的人多了,
- “余诚老于亡命之经验家也,余宁乐此,不愿苟活于此浊恶空气中也。”梁启超为此( )A. 创作《变法通议》等论文,阐述
- 深圳市社会保险局决定,对外来务工者办理养老保险。保险费按工资总额的10%缴纳,其中,企业为工人缴7%,工人缴3%,使外来
- 拉美独立运动中,被誉为“解放者”的领导人是( )。 A.玻利瓦尔 B.圣马丁
- 阅读下面的文字,完成后面题目。 市场经济条件下的人文精神 南帆 当下的文化领域弥漫着浓烈的世俗气息,人们可以察觉到文化领
- 右图表示一分子 A.DNA
- 马克思说,人是历史的剧作者,又是历史的剧中人,下列对这一观点理解正确的是 ①人是社会历史的主体,社会历史是由人的实践活
- 下列各句,没有语病的一项是 A.我们应该发挥广大青年的充分的作用,让他们在亚太市长峰会期间各显其能,使来宾从中感受到重庆
- 下列各式中,一定是二次根式的有个. A. 2 B.3 C. 4
- 多数同学家里都有调光台灯、调速电风扇。过去是用变压器来实现的,缺点是成本高、体积大、效率低,且不能任意调节灯的亮度或电风
- 如图所示,医生正在用听诊器为病人诊病。听诊器运用了声音_________ (填“具有能量”或“传递信息”)的道理;来自患
- 下列变化不属于化学变化的是(), A.煤的干馏 B.石油分馏 C.由乙烯制聚乙

 )
)
 M
M  溶液褪色并产生气泡
溶液褪色并产生气泡 悬浊液并加热
悬浊液并加热 溶液与
溶液与  溶液混合
溶液混合 和
和 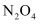 混合气体的密闭玻璃球浸泡在热水中
混合气体的密闭玻璃球浸泡在热水中 的
的 
 饱和溶液中滴入足量浓氨水,并加热至刚好沸腾
饱和溶液中滴入足量浓氨水,并加热至刚好沸腾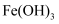 胶体
胶体

 和
和  的主要作用是。
的主要作用是。
 时,
时,  ;
;  。则“氟化除杂”过后滤液3中
。则“氟化除杂”过后滤液3中  。
。
 在硫酸盐中对某些金属离子的萃取率与溶液
在硫酸盐中对某些金属离子的萃取率与溶液 
 硫酸镍晶体(
硫酸镍晶体(  )样品溶解,定容至
)样品溶解,定容至  。取
。取  试液,用
试液,用  的
的  标准溶液滴定至终点。重复实验,平均消耗
标准溶液滴定至终点。重复实验,平均消耗  标准溶液体积为
标准溶液体积为  。反应为
。反应为  。计算样品纯度为。(不考虑杂质反应)
。计算样品纯度为。(不考虑杂质反应)
 溶液加入
溶液加入  酸性溶液(过量)中,混合后约5秒内无明显变化,随后有少量蓝色出现并迅速变蓝。
酸性溶液(过量)中,混合后约5秒内无明显变化,随后有少量蓝色出现并迅速变蓝。  慢
慢 _=_+_ 较快
_=_+_ 较快 快
快 氧化性比
氧化性比  强,该结论(填“合理”或“不合理”),理由是。
强,该结论(填“合理”或“不合理”),理由是。
 闭合后,电流表的指针偏转情况记录如表:
闭合后,电流表的指针偏转情况记录如表:




 的实验操作是。
的实验操作是。 时,直接向a极区滴加淀粉溶液,溶液未变蓝。取a极附近溶液于试管中,滴加淀粉溶液,溶液变蓝。判断
时,直接向a极区滴加淀粉溶液,溶液未变蓝。取a极附近溶液于试管中,滴加淀粉溶液,溶液变蓝。判断  发生反应
发生反应





 的混合气体,匀速通过装有催化剂的反应器反应(如图甲),反应器温度变化与从反应器排出气体中
的混合气体,匀速通过装有催化剂的反应器反应(如图甲),反应器温度变化与从反应器排出气体中  的体积分数φ关系如图乙,φ(CH3OH)变化的原因是。
的体积分数φ关系如图乙,φ(CH3OH)变化的原因是。 
 的恒容密闭容器内充入
的恒容密闭容器内充入  和
和  ,加入合适催化剂后在某温度下开始反应,并用压力计监测容器内压强的变化如表:
,加入合适催化剂后在某温度下开始反应,并用压力计监测容器内压强的变化如表:  时,
时,  的平均反应速率为,该温度下的平衡常数
的平均反应速率为,该温度下的平衡常数  加入密闭容器中,在一定条件下发生上述反应。平衡时
加入密闭容器中,在一定条件下发生上述反应。平衡时 
 由大到小的关系是,判断理由是。
由大到小的关系是,判断理由是。


