云南省大理州2020-2021学年高三上学期化学11月月考试卷
教材科目:化学
试卷分类:高三上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
短周期元素W、X、Y、Z的原子序数依次增大。W的单质与H2在暗处能化合并发生爆炸,X是同周期中金属性最强的元素,Y原子的最外层电子数等于电子层数,W和Z原子的最外层电子数相同。下列说法错误的是( )
A . 单质的沸点:Z>W
B . 简单离子半径:X>W
C . 元素X与氧可形成既含离子键又含非极性共价键的化合物
D . X、Y、Z的最高价氧化物对应的水化物两两之间能相互反应
|
|
| 2. 单选题 | 详细信息 |
|
化学与人类生活密切相关,下列说法正确的是( )
A . “红柿摘下未熟,每篮用木瓜三枚故入,得气即发,并无涩味”,其中“气”是指乙酸乙酯
B . 将碘酒滴到未成熟的苹果肉上变蓝说明苹果肉中含有淀粉
C . “丹砂烧之成水银,积变又还成丹砂”只涉及物理变化
D . 食用黑芝麻糊时可加入白砂糖作配料,白砂糖的上要成分是麦芽糖
|
|
| 3. 单选题 | 详细信息 |
|
对甲基苯乙烯(
A . 分子式为
 B . 能发生加聚反应和氧化反应
C . 具有相同官能团的芳香烃同分异构体有5种
B . 能发生加聚反应和氧化反应
C . 具有相同官能团的芳香烃同分异构体有5种  不考虑立体异构 不考虑立体异构  D . 分子中所有原子可能处于同一平面
D . 分子中所有原子可能处于同一平面
|
|
| 4. 单选题 | 详细信息 |
|
设NA为阿伏加德罗常数的数值,下列有关叙述错误的是( )
A . 电解精炼铜时,当阳极质量减少6.4g时,电路中转移的电子数目可能小于0.2NA
B . 78 g Na2O2中所含的阴离子数为NA
C . 0.1 mol Cu溶于足量稀硝酸中,转移的电子数为0.2NA
D . 某温度下,pH=2的H2SO4溶液中的H+总数为0.01NA
|
|
| 5. 单选题 | 详细信息 |
|
对于下列实验装置进行实验的描述正确的是( )
A . a装置制取CO2时可以做到随开随用、随关随停
B . b装置可以用于干燥D2、O2、NH3、Cl2等气体
C . c装置用于排空气集气时,从右边进气可以收集H2、NO、NH3等气体
D . d装置可用于Cl2的尾气处理
|
|
| 6. 单选题 | 详细信息 |
|
某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO2-、AlO2-中的若干种离子,离子浓度均为0.1 mol·L-1。某同学进行了如图所示实验,下列说法正确的是( )
A . 原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42-
B . 滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C . 无法确定原试液中是否含有Al3+、Cl-
D . 无法确定沉淀C的成分
|
|
| 7. 单选题 | 详细信息 |
|
室温时,下列说法正确的是( )
A . 0.1 mol·L-1 醋酸钙溶液中,c(Ca2+)>c(CH3COO-)>c(OH-)>c(H+)
B . 向BaSO4悬浊液中加入少量Na2SO4固体后振荡,Ksp(BaSO4)增大
C . 0.1 mol·L-1 Na2CO3溶液中加入少量NaOH固体后振荡,c(CO32-)不变
D . 相同物质的量浓度的CH3COOH和CH3COONa溶液等体积混合后,溶液中:c(CH3COO-)+c(CH3COOH)=2c(Na+)
|
|
| 8. 综合题 | 详细信息 |
|
第ⅢA元素也称为硼族元素,除硼外其余均为金属元素。硼的应用非常广泛,可用于原子反应堆和高温技术,甚至可用来制作火箭中所用的某些结构材料。
|
|
| 9. 综合题 | 详细信息 |
|
雾霾天气严重影响人们的生活,其中氮氧化物是造成雾霾天气的主要原因之一。
|
|
| 10. 综合题 | 详细信息 |
|
2017年4月26日,海军成立68周年时,我国第一艘国产航母成功下水。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
|
|
- 2016-2017学年江苏省扬州市宝应县安宜高中高二上学期期中化学试卷(选修)
- 2015-2016学年陕西省宝鸡市岐山县高二下学期期末化学试卷(文科)
- 广西南宁市“4N”高中联合体2018-2019学年高一下学期化学期末考试试卷
- 江西省吉安市2017-2018学年高二下学期化学期末考试试卷
- 四川省乐山市2016-2017学年高二上学期化学期末考试试卷
- 北京市怀柔区2015-2016学年高二上学期化学期末考试试卷
- 山东省滨州市2019-2020学年高二下学期化学期末考试试卷
- 2020年高考理综化学真题试卷(新课标II)
- 广东省潮州市2018-2019学年高二上学期理综-化学期末考试试卷
- 吉林省长春市兴华中学2019-2020学年高二上学期化学期末考试试卷
- 安徽省黄山市2019-2020学年高二下学期化学期末考试试卷
- 江苏省宿迁市2016-2017学年高一上学期化学期末考试试卷
- 头孢曲松纳是一种常见的抗生素,临床应用十分广泛。但是,如果把它和某些药物一起服用,就会导致药效减弱、副作用增强,对人体造
- 在△ABC中,若a∶b∶c=1∶2∶,则最大角的余弦值等于___________.
- 有一闭合金属线框,其曲线部分恰好是某个正弦曲线的正半周,直线部分的长度L=0.02 m,线框的总电阻为2 Ω,若线框从图
- 不惜千金买宝刀, 。(秋瑾《对酒》)
- 4.在下面的一段文字横线处,填入语句,衔接最恰当的一项是 群星之所以璀璨,是因为周围有数不清的热粒子滋养它们。
- 120℃,0.1mol烃与1molO2(过量)混合,完全燃烧后通过足量的Na2O2固体,固体增重15克, 从Na2O2中
- 在比例尺为1∶40000的工程示意图上,无锡地铁一号线的长度约为54.3cm,则它的实际长度约为
- 如图,射线OC的端点O在直线AB上,∠1的度数比∠2的度数的2倍多10°,则可列正确的方程组为( ). (A)(B
- 下列除去杂质的方法正确的是 ① 除去乙烷中少量的乙烯——光照条件下通入Cl2 ② 除去乙酸乙酯中少量的乙酸——饱和碳酸钠
- 西北地区气候干旱的主要原因是( ) A.距海较远 B.纬度较高 C.海拔较高 D.温度较
- 2001年中国作为亚太经合组织第九次领导人非正式会议的东道主,为APEC的发展作出相当大的努力。2003年,中国宣布加入
- (2009年黄冈模拟)如下图所示光学显微镜下观察到的根尖分生区的细胞,视野内看到最多的细胞是()
- 一段导体两端电压是4V,导体中的电流是1A,若通过导体的电流是250mA,则导体两端的电压是________。若两端电压
- 人生是一个令人深思的话题。下面这些引自课文中的语句给你什么启示?请默读一边,用一句话来表达你心中的感受。(6分)
- 为了测定和描绘“220V,40W”白炽电灯灯丝的伏安特性曲线,可以利用调压变压器供电.调压变压器是一种自耦变压器,它只有
- Hello, everyone.Nice to meet you.It is my 16 day (天) in t
- 概括下面这段文字的主要内容。(不超过20字) 中国农业大学今天专门为该校的15名大学生实习“村官”举行了欢送会。欢送会后
- 过点(-1, 3)且垂直于直线的直线方程为 A.2x + y1= 0
- 某班同学在学校网站上做了一个有关马泽东的网页,如果在“思想研究”栏目下再增加一个相关链接,则链接项“X”里应该是() A
- 下列有关基因重组的叙述中,不正确的是 A.基因重组过程中可产生新的基因型 B.基因重组是形成生物多样性的重要来源之一 C






 N2(g)+2NO2(g)△H<0,其正反应速率表达式为:v正=k正·cn(NO),测得反应速率和浓度的关系如下表。
N2(g)+2NO2(g)△H<0,其正反应速率表达式为:v正=k正·cn(NO),测得反应速率和浓度的关系如下表。
 的比值保持不变时就达到了化学平衡状态
的比值保持不变时就达到了化学平衡状态



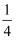 ,则该晶体中S2-和Zn2+之间的最短距离为nm。(写出计算式即可)
,则该晶体中S2-和Zn2+之间的最短距离为nm。(写出计算式即可)



