四川省南充市2019-2020学年高二下学期化学期末考试试卷
四川省南充市2019-2020学年高二下学期化学期末考试试卷
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
将0.2 mol/L的KI溶液和0.01mol/L Fe2(SO4)3溶液等体积混合后,取混合液分别进行实验。下列能说明溶液中存在平衡2Fe3++2I-
 2Fe2++I2的是( ) 2Fe2++I2的是( )
A . 滴入硝酸银溶液产生黄色沉淀
B . 加入酸性KMnO4溶液,溶液紫红色褪去
C . 滴入淀粉溶液,溶液变蓝色
D . 滴入KSCN溶液,溶液变红色
|
|
| 2. 单选题 | 详细信息 |
|
1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中能量变化如图所示,下列判断错误的是( )
A . 反应物的总能量大于生成物的总能量
B . 使用催化剂可降低E1
C . 升高温度,活化分子百分数不变
D . 热化学方程式为:NO2(g)+CO(g)=CO2(g)+NO(g) ΔH=-(a-c)kJ•mol-1
|
|
| 3. 单选题 | 详细信息 |
|
下列事实不能用勒夏特列原理解释的是( )
A . H2(g)、I2(g)、HI(g)平衡体系加压后颜色变深
B . 常温下,将pH=10的NH3•H2O溶液稀释10倍,pH>9
C . 利用TiCl4水解制备TiO2时,需加入大量水并加热
D . 向Mg(OH)2悬浊液中滴加FeCl3溶液,有红褐色沉淀生成
|
|
| 4. 单选题 | 详细信息 |
|
如图为以稀H2SO4为电解质溶液,Pt为电极的氢氧燃料电池的工作原理示意图。下列有关说法错误的是( )
A . 氢氧燃料电池是一种具有应用前景的绿色电源
B . a极为负极,电子由a极经外电路流向b极
C . b极的电极反应式为:O2+4H++4e-=2H2O
D . 电池工作一段时间后,装置中c(H2SO4)不变
|
|
| 5. 单选题 | 详细信息 | ||||||||||||
|
下列电化学装置及用途正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||
| 6. 单选题 | 详细信息 |
|
常温下,下列关于pH=3的CH3COOH溶液的叙述错误的是( )
A . 溶液中水电离出的c(H+)=10×10-11mol•L-1
B . 与等体积pH=11的NaOH溶液混合,所得溶液pH=7
C . 加入少量水稀释该溶液的过程中,
 增大
D . 加入0.1mol•L-1CH3COONa溶液使pH=7,则c(CH3COO-)=c(Na+) 增大
D . 加入0.1mol•L-1CH3COONa溶液使pH=7,则c(CH3COO-)=c(Na+)
|
|
| 7. 单选题 | 详细信息 | |||||||||||||||
|
常温下,进行下列实验操作,能达到预期目的的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 8. 综合题 | 详细信息 |
|
回答下列问题。
|
|
| 9. 综合题 | 详细信息 |
|
|
| 10. 综合题 | 详细信息 |
|
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。诮回答下列问题:
|
|
高中化学 试卷推荐
- 人教版化学高二选修6第三单元实验3-5比色法测定抗贫血药物中铁的含量同步练习
- 高中化学人教版(2019)必修第二册第五章 第一节 硫及其化合物
- 河北省石家庄市辛集市第一中学2019-2020学年高三下学期化学5月月考试卷
- 2015-2016学年四川省成都市龙泉中学高一下学期期末化学模拟试卷(二)
- 湖北省鄂州市泽林高中2019-2020学年高一上学期化学期末考试试卷
- 上海市普陀区2020年高考化学二模试卷
- 人教版化学高二选修5五章第三节功能高分子材料同步练习
- 福建省漳州市2020年高考化学三模试卷
- 2017-2018学年高中化学人教版 选修五第二章 第三节 卤代烃
- 2017年陕西省榆林市高考化学一模试卷
- 天津市红桥区2017-2018学年高考理综-化学一模考试试卷
- 2015-2016学年内蒙古鄂尔多斯市准格尔旗自治区世纪中学高二下学期第一次月考化学试卷
最近更新
- (本题满分8分)计算:(1); (2).
- 某反应前后分子变化的微观示意图如下,下列说法正确的是()A.反应物与生成物共有5种物质 B.反应后原子的个数增多 C.该
- 右图是一本连环画的封面,图中的“社”指的是A.农业生产合作组织 B.公私合营生产组织 C
- 提出元素周期律并绘制了第一张元素周期表的科学家是( ) A.道尔顿 B.阿伏伽德罗
- (2011年11月泰兴市期中15题)1933年8月14日,苏联杂志《为了工业化》写道:“美国的商业和科学与布尔什维克的智
- 2013年十二届全国人大会议提出,要着力扩大内需特别是消费需求,拓宽和开发消费领域,促进居民文化、旅游、健身、养老、家政
- “西气东输”工程是将塔里木盆地的天然气输往 ( ) A.华北地区 B.东北地区 C.西
- 2011•金华十校期末 全面建设小康社会的进程中,我们党根据时代的变化提出了以人为本、科学发展、和谐社会等新的理念
- 下图是某兴趣小组在探究绿色植物光合作用过程中的实验设计:请据图分析回答:(1)根据以上实验设计分析,甲、乙是一组
- 某研究小组制备消毒液(主要成分为NaClO)设计了A、B两套装置。并查阅到下列资料,“在加热情况下,卤素和碱液发生如下反
- (2009· 江苏扬州模拟考试)2008年GDP增长9%,其中消费贡献34%,投资贡献48%,剩下18%是出口的贡献。而
- 一个质量为0.5kg的小球,从距地面高5m处开始做自由落体运动,与地面碰撞后,竖直向上跳起的最大高度为4m,小球与地面碰
- 下列离子方程式正确的是()A.NaHSO3溶液中投入过氧化钠粉末:4HSO+2Na2O2===4SO+O2↑+4Na+B
- 一个中学生站在水平地面上对地面的压强最接近于:A、10帕; B、100帕; C、100
- 丁苯橡胶的结构简式为。合成这种橡胶的单体应是() ①C6H5—CH=CH2 ②CH3—CH=CH-
- 下列关于育种以及相关原理的说法正确的是( ) A.通过杂交育种培育高产抗病小麦的原理是染色体变异 B.可通过人工诱
- (09年长郡中学月考)如图所示将一光滑的半圆槽置于光滑水平面上,让一小球自左侧槽口A的正上方静止开始下落,与圆弧槽相切自
- 下列物质属于芳香烃,但不是苯的同系物的是A.③④ B.②⑤ C.①②⑤⑥ D.②③④⑤⑥
- 在欧洲西部,同时也是世界上最大的海港为( ) A.伦敦港 B.巴黎港 C.鹿特丹港 D.汉
- 公民行使监督权,实行民主监督,可以利用多种方法和渠道。如( ) ①信访举报制度 ②人大代表联系群众制度 ③专家咨询制度






 在溶液中存在水解平衡
在溶液中存在水解平衡



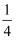 ,W基态原子的价电子排布式为。
,W基态原子的价电子排布式为。




