安徽省合肥市2021年高考化学三模试卷
安徽省合肥市2021年高考化学三模试卷
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
化学与生活、生产密切相关,下列说法错误的是( )
A . 煤的气化、液化和干馏都属于化学变化
B . 地沟油不宜食用,但可分馏提取汽油
C . 棉花的主要成分是纤维素,纤维素由碳、氢、氧元素组成
D . 硝酸铵用于制备医用速冷冰袋,是利用了其溶于水快速吸热的性质
|
|
| 2. 单选题 | 详细信息 |
|
化合物p(
 )、r( )、r(
A . r中所有原子可能共平面
B . q环上的一氯取代产物共有4种
C . p、q、r均能使溴的四氯化碳溶液褪色
D . 物质的量相等的p和q完全燃烧耗氧量相同
|
|
| 3. 单选题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法中一定正确的是( )
A . 1molFe3O4被完全还原为Fe2+时转移的电子数为2NA
B . 10.5gHClO中含有H—Cl键的数目为0.2NA
C . 2molSO2与1molO2充分反应后气体分子总数小于2NA
D . 8.8g由CO2和N2O组成的混合气体含氧原子总数为0.3NA
|
|
| 4. 单选题 | 详细信息 |
|
已知SiHCl3常温下为无色液体,沸点31.85℃,遇水剧烈反应。实验室用H2还原SiHCl3制备纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法错误的是( )
A . 装置II、Ⅲ中依次盛装的是浓硫酸、热水
B . 实验时,应先加热管式炉,再打开盛装稀硫酸的分液漏斗
C . 可以用盐酸、双氧水和硫氰化钾溶液来检验制得的硅中是否含铁单质
D . 装置I也可用于氢氧化钠固体与浓氨水反应制备氨气
|
|
| 5. 单选题 | 详细信息 |
|
X、Y、Z、W是原子序数依次增大的短周期元素。Z是短周期中金属性最强的元素,M是Y元素的单质,甲、乙、丙、丁、戊是由这些元素组成的二元化合物,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,戊是具有漂白性的无色气体。上述物质间的转化关系如图所示,下列说法中正确的是( )
A . 甲的水溶液显中性
B . 化合物乙也具有漂白性,且漂白原理和戊相同
C . Z分别与X、Y、W形成的化合物中,各元素原子均满足最外层8电子结构
D . 丁的稳定性和沸点均比丙高
|
|
| 6. 单选题 | 详细信息 |
|
某种微生物电池可用于降解铁硫化物(以FeS2计),其工作原理示意图如图。下列说法正确的是( )
A . 该微生物电池中,N极为正极
B . M极的电极反应式为O2-4e-+4H+=2H2O
C . 电池工作时负极附近溶液pH减小
D . 该电池中电子经过电解质溶液由负极流向正极
|
|
| 7. 单选题 | 详细信息 |
|
已知HB是一种弱酸,室温下向某浓度的HB溶液中滴入0.1mol·L-1的NaOH溶液,溶液的pH与离子浓度的关系如图所示。下列说法正确的是( )
A . 从a到d,水的电离程度逐渐减小
B . HB电离平衡常数Ka=101.3
C . b点时,c(HB)+c(OH-)=c(Na+)+c(H+)
D . a点时,c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
|
|
| 8. 实验探究题 | 详细信息 |
|
碘酸钙[Ca(IO3)2]是广泛使用的既能补钙又能补碘的新型食品添加剂,不溶于乙醇,在水中的溶解度随温度降低而减小。实验室制取Ca(IO3)2的流程如图所示:
已知:碘酸(HIO3)是易溶于水的强酸,不溶于有机溶剂。
|
|
| 9. 综合题 | 详细信息 | |||||||||||||||
|
MnO2是重要的化工原料,由软锰矿(主要成分为MnO2 , 还含有少量Fe3O4、Al2O3和SiO2等杂质)和硫化锰(MnS)制备精MnO2的一种工艺流程如图:
已知:相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
回答下列问题:
|
||||||||||||||||
| 10. 综合题 | 详细信息 |
|
SO2和H2S是大气污染物,这两种气体的转化研究对资源综合利用和环境保护有重要意义。
|
|
高中化学 试卷推荐
- 安徽省宿州市北方中学2021-2022学年高一上学期化学第一次月考试卷
- 北京市大兴区2020-2021学年高一上学期期末考试化学试题
- 陕西省渭南市大荔县2020-2021学年高一下学期期末考试化学试题
- 上海松江区2021-2022学年高三上学期期末考试化学试题
- 黑龙江省齐齐哈尔市2022届高三第二次模拟考试理科综合化学试题
- 河北省唐山市2022届高三普通高中学业水平选择性考试第二次模拟演练化学试题
- 河北省衡水中学2020-2021学年高三上学期化学期中考试试卷
- 四川省成都市2020-2021学年高二上学期期末调考化学试题
- 山西省沁源县第一中学2020-2021学年高二下学期化学开学考试试卷
- 湖北省十堰市2021年高考化学4月模拟试卷
- 山东省滨州市2022届高三第二次模拟考试化学试题
- 河北省唐山市2021年高考化学三模试卷
最近更新
- 如图9所示,AC、BD为圆的两条互相垂直的直径,圆心为O,半径为R。电荷量均为Q的正、负点电荷放在圆周上,它们的位置关于
- 根据电场强度的定义式E=,在国际单位制中,电场强度的单位应是() A. 牛/库
- 当 时,式子的值大于的值.
- ......
- 已知函数f(x)=loga(1+x),g(x)=loga(1﹣x),(a>0,且a≠1). (1)设a=2,函数f(x)
- 甲、乙两首诗的体裁均属于近体诗中的 。(限两字)甲
- “十一五”时期,我国在公共文化服务领域实施“乡镇综合文化站建设”、“流动综合文化服务车”、“农村书屋”等新项目。这些举措
- 在不计空气阻力的情况下,某物体以30m/s的初速度从地面竖直上抛,则(重力加速度 g 取10m/s2)
- 如图,在△ABC中,AB=AD=DC,若∠BAD=20°,则∠C= .
- 在单缝衍射实验中,中央亮条纹的光强占入射光光强的95%以上,假设现在只让一个光子通过单缝,则该光子
- (2005广东高考,31)现代经济发展虽然对自然条件的依赖性有所减弱,但由于受产业传统和其他社会因素的影响,各国各地区仍
- 《国务院关于鼓励和引导民间投资健康发展的若干意见》提出,要规范设置投资准入门槛,鼓励和引导民间资本进入市政公用事业、金融
- 美国总统里根10世纪80年代初提出组建北美自由贸易区构想时,墨西哥采取抵制政策。1988年,新总统就任后,墨西哥的态度发
- .下列溶液中阴离子浓度最大的是( ) A.0.5 mol.L-1HNO3溶液50mL B.0.6mol.
- 电灯L1和L2并联接入电路,通过它们的电流分别为I1和I2,干路中的电流为I,则
- 如果一次函数y=x+b经过点A(0,3),那么b= .
- 我们国家,国力的强弱,经济发展后劲的大小,越来越取决于劳动者的素质,取决于知识分子的数量和质量。 辨题:发展教育和科学是
- “单摆的周期T与摆长L的关系”的实验中,某次测量小球的直径的示数如图1所示,图中1游标上10格的长度为19mm,则小球
- 下列不属于运动系统的结构是( ) A. 骨 B. 骨骼肌 C. 关节 D. 神经
- B 解析:∵P(X<-1)= P(X>1),则P(X>-1)=1-p .






 +5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液,用0.1000mol·L-1Na2S2O3溶液滴定(I2+2S2O
+5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液,用0.1000mol·L-1Na2S2O3溶液滴定(I2+2S2O 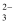 =2I-+S4O
=2I-+S4O  )至终点,消耗Na2S2O3溶液30.00mL。达滴定终点时的现象是,产品中Ca(IO3)2的质量分数为。[已知Ca(IO3)2的摩尔质量:390g·mol-1]。
)至终点,消耗Na2S2O3溶液30.00mL。达滴定终点时的现象是,产品中Ca(IO3)2的质量分数为。[已知Ca(IO3)2的摩尔质量:390g·mol-1]。






