福建省三明市三地三校2020-2021学年高二上学期化学期中考试试卷
福建省三明市三地三校2020-2021学年高二上学期化学期中考试试卷
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 | ||||||||||||||||
|
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应:mX(g)
 nY(g) ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示: nY(g) ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
下列说法正确的是( )
A . m>n
B . Q<0
C . 温度不变,压强增大,Y的质量分数减少
D . 体积不变,温度升高,平衡向逆反应方向移动
|
|||||||||||||||||
| 2. 单选题 | 详细信息 |
|
将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)
 2HBr(g) △ H<0;平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( ) 2HBr(g) △ H<0;平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
A . a>b
B . a=b
C . a<b
D . 无法确定
|
|
| 3. 单选题 | 详细信息 |
|
在理论上不能用于设计原电池的化学反应是( )
A . HCl+NaOH=NaCl+H2O ΔH<0
B . 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH<0
C . 4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) ΔH<0
D . 2H2(g)+O2(g)=2H2O(l) ΔH<0
|
|
| 4. 单选题 | 详细信息 |
|
可逆反应 aA(s) + bB(g)⇌cC(g) + dD(g)进行过程中,当其他条件不变时,C 的体积分数 C%与温度(T)、压强(P)的关系如图所示。下列叙述正确的是( )
A . 化学方程式中,b > c + d
B . 达到平衡后,加入催化剂,C 的体积分数增大
C . 达到平衡后,升高温度,平衡向左移动
D . 在P1时化学平衡常数大于P2时化学平衡常数
|
|
| 5. 单选题 | 详细信息 |
|
在同温同压下,下列各组热化学方程式中 ,ΔH2>ΔH1的是( )
A . 2H2(g)+O2(g)=2H2O(g)ΔH1 2H2(g)+O2(g)=2H2O(l) ΔH2
B . S(g)+O2(g)=SO2(g) ΔH1 S(s)+O2(g)=SO2(g) ΔH2
C . C(s)+
 O2(g)=CO(g) ΔH1 C(s)+O2(g)=CO2(g) ΔH2
D . 2HCl(g)= H2(g)+Cl2(g) ΔH1 O2(g)=CO(g) ΔH1 C(s)+O2(g)=CO2(g) ΔH2
D . 2HCl(g)= H2(g)+Cl2(g) ΔH1  H2(g)+ H2(g)+  Cl2(g)=HCl(g) ΔH2 Cl2(g)=HCl(g) ΔH2
|
|
| 6. 单选题 | 详细信息 |
|
可逆反应aX+bY
 cZ在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)~时间(t)图像如图所示。则下列说法中正确的是( ) cZ在一定温度下的密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(v)~时间(t)图像如图所示。则下列说法中正确的是( )
A . 若a+b=c,则t0时只能是增大了容器的压强
B . 若a+b=c,则t0时只能是加入了催化剂
C . 若a+b≠c,则t0时只能是增大了容器的压强
D . 若a+b≠c,则t0时只能是加入了催化剂
|
|
| 7. 单选题 | 详细信息 |
|
已知H2(g)+Cl2(g)=2HCl(g)△H=-184.6kJ/mol,则反应HCl(g)=
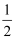 H2(g)+ H2(g)+ 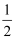 Cl2(g)的△H为( ) Cl2(g)的△H为( )
A . +184.6kJ/mol
B . -92.3kJ/mol
C . -369.2kJ/mol
D . +92.3kJ/mol
|
|
| 8. 单选题 | 详细信息 |
|
下列说法错误的是( )
A . 化学反应放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量的相对大小
B . 化学反应除了生成新物质外,还伴随着能量的变化
C . 需要加热才能发生的化学反应一定是吸热反应
D . 反应物的总能量高于生成物的总能量时,发生放热反应
|
|
| 9. 单选题 | 详细信息 |
|
下列说法正确的是( )
A . 已知2SO2(g)+O2(g)
 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后反应速率加快
C . 已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
D . 若1molSO2与0.5molO2反应生成SO3放出的热量为47.8kJ,则该反应的热化学方程式可表示为2SO2(g)+O2(g) 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后反应速率加快
C . 已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
D . 若1molSO2与0.5molO2反应生成SO3放出的热量为47.8kJ,则该反应的热化学方程式可表示为2SO2(g)+O2(g)  2SO3(g) ΔH=-95.6 kJ∙mol−1 2SO3(g) ΔH=-95.6 kJ∙mol−1
|
|
| 10. 单选题 | 详细信息 |
|
1g碳与适量水蒸气反应生成CO和H2 , 需吸收10.94KJ热量,此反应的热化学方程式为( )
A . C + H2O=CO + H2 ΔH=+131.3KJ·mol-1
B . C(s)+ H2O(g)=CO(g) + H2(g) ΔH=+10.94KJ·mol-1
C . C(s)+ H2O(l)=CO(g) + H2(g) ΔH= +131.3KJ·mol-1
D . C(s)+ H2O(g)=CO(g) + H2(g) ΔH=+131.3KJ·mol-1
|
|
高中化学 试卷推荐
- 2015-2016学年广西南宁市马山县高二下学期期末化学试卷
- 广东省东莞市光明中学2019-2020学年高三下学期化学第一次月考试卷
- 2015-2016学年河南省鹤壁市淇县一中高二下学期期中化学试卷
- 高中化学人教版(2019)必修第一册第一章第一节 物质的分类及转化
- 湖北省荆门市2016-2017学年化学高一上学期期末考试试卷
- 安徽省宿州市埇桥区2018-2019学年高一上学期化学期末考试试卷
- 2016-2017学年湖北省荆州市公安县车胤中学高一上学期期中化学试卷
- 四川省资阳市2016-2017学年高二下学期化学期末考试试卷
- 2015-2016学年陕西省西安三十三中高一下学期第一次月考化学试卷
- 湖南省湘西州2018-2019学年高二(文)上学期化学期末考试试卷
- 2015-2016学年甘肃省嘉峪关市酒钢一中、三中高二上学期期末化学试卷
- 湖南省郴州市2019-2020学年高一下学期化学期末考试试卷
最近更新
- 下列各组中两个变化所发生的反应,属于同一类型的是①由甲苯制甲基环己烷、由乙烷制溴乙烷 ②乙烯使溴水褪色、乙烯直接水化法
- 只用空气鉴别甲烷、乙烯和乙炔三种气体,可将它们分别______________,观察__________________
- 将一质量为5kg,体积为6×10-3m3的西瓜浸没水中,西瓜受到的浮力是 N,松手后西瓜会 (
- 如右图,中心在原点O的椭圆的右焦点为,右准线的方程为:. (Ⅰ)求椭圆的方程; (Ⅱ)在椭圆
- 如图是甲、乙、丙、丁四种物质的溶解度曲线,温度为t℃时,将等质量甲、乙、丙、丁四种物质分别加到100g水中,充分搅拌后只
- 衡量石油化工发展水平的标志是( ) A、乙烯产量 B、丙烯产量 C
- 十八大提出2020年全面建成小康社会。“十三五”时期(2016-2020年)是全面建成小康社会的关键期,经济发展全面进入
- The man ________ on the ground________ that he had ________
- The child complained that the old man made no answer when
- 任务型阅读 (共10小题;每小题1分,满分10分) One of the most well-known direct
- 5.下列各句中,加横线的成语使用正确的一项是( ) A.《舌尖上的中国》以富有草根气息的语调,把中国饮食文化讲述得
- You can’t________the fact that there are many difficulties b
- 下列说法中错误的是①化学性质相似的有机物是同系物②分子组成相 差一个或几个-CH2原子团的有机物是同系物③若烃中碳、
- 如图所示,已知圆为圆上一动点,点P在AM上,点N在CM上,且满足轨迹为曲线E. (1)求曲线E的方程; (2)(2)若
- 下列能用勒夏特列原理解释的是 A.高温及加入催化剂都能使合成氨的反应速率加快 B.棕红色NO2加压后颜色先变深后变浅 C
- 如图所示,在粗糙的水平桌面上,有—个物体在水平力F作用下向右作匀加速直线运动。现在使力F逐渐减小直至为零,但方向不变,则
- 已知函数f(x)=,则f[f(2)]=() A.2 B.4 C.8 D.16
- (08年福建卷) 阅读下面的文字,按要求与一篇不少于800字的文章。三个人走进商店。一个人买了一瓶果汁,说:“我喜欢甜的
- 古人云:“君子和而不同,小人同而不和。”这句话告诉我们 A.人无完人,朋友难免有缺点 B.人各有不同,朋友之间难免有分歧
- 假定英语课上老师要求同桌之间交换修改作文,请你修改你同桌写的以下作文。文中共有10处语言错误,每句中最多有两处,每处错误





