广东福建等省2019-2020学年高三下学期化学4月理综试卷(全国I卷)
广东福建等省2019-2020学年高三下学期化学4月理综试卷(全国I卷)
教材科目:化学
试卷分类:高三下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高三下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
文房四宝即笔、墨、纸、砚,其中以湖笔、徽墨、宣纸和端砚最为称著。下列说法正确的是( )
A . 徽墨中墨的主要成分是黑色的油脂
B . 湖笔中笔头的羊毫的主要成分是蛋白质
C . 宣纸的主要成分是无机碳和少量的纤维素
D . 含较多氧化铁的端砚呈黑色
|
|
| 2. 单选题 | 详细信息 |
|
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 11.2 LCl2通入足量的NaOH 溶液中充分反应 ,转移的电子数为 0.5NA
B . 4.4 g 由 CO2 和 N2O 组成的混合气体中含有的电子总数为 2.2NA
C . 常温下 ,1.0L p H=1 的 H2SO4溶液中含有H+的数目为 0.2NA
D . 11.5 g乙醇分子中含有C- H键的数目为1.5NA
|
|
| 3. 单选题 | 详细信息 |
|
化合物(a)在乙酸汞催化下与乙酸反应生成化合物(b):
下列说法错误的是( )
A . (a)具有含苯环的同分异构体
B . (a)能使酸性KMnO4溶液褪色
C . (b)能发生加成聚合反应
D . (b)的一氯代物有7种
|
|
| 4. 单选题 | 详细信息 |
|
海冰是海水冻结而成的咸水冰,海水冻结时,部分来不及流走的盐分(设以NaCl为主)以卤汁的形式被包裹在冰晶之间,形成“盐泡”,其大致结构如图所示,若海冰的冰龄达到1年以上,则融化后的水为淡水。下列叙述正确的是( )
A . 海冰内层“盐泡”越少,密度越大
B . 海冰冰龄越短,内层的“盐泡”越少
C . 每含1mol H2O的海冰内就有2×10-5 NA个NaCl分子(NA为阿伏加德罗常数)
D . 海冰内层NaCl的浓度约为l0-3 mol/L(设冰的密度为0.9 g.cm-3)
|
|
| 5. 单选题 | 详细信息 |
|
磷酸铁锂电池放电时正极的反应式为
 。该电池放电时的工作原理如图所示。下列叙述正确的是( ) 。该电池放电时的工作原理如图所示。下列叙述正确的是( )
A . 放电时,Li+通过隔膜移向正极
B . 放电时,电子由铜箔经溶液流向铝箔
C . 放电时,负极发生的电极反应:Cu-2e-=Cu2+
D . 该电池放电过程中C、Fe、P元素化合价均发生变化
|
|
| 6. 单选题 | 详细信息 |
|
短周期主族元素W、X、Y、Z的原子序数依次增大,W的原子序数是Z的原子序数的一半,W、X、Y三种元素形成的化合物M结构如图所示。下列叙述正确的是( )
A . 原子半径:Z>Y>W
B . 化合物M中W的原子满足8电子稳定结构
C . 对应单质的熔点:X>Z>Y
D . Z的氧化物对应的水化物为强酸
|
|
| 7. 单选题 | 详细信息 |
|
次磷酸(H3PO2一元弱酸)和氟硼酸(HBF4)均可用于植物杀菌。常温时,有1mol∙L-1的H3PO2溶液和1mol∙L-1的HBF4溶液,两者起始时的体积均为V0 , 分别向两溶液中加水,稀释后溶液的体积均为V,两溶液的pH变化曲线如图所示。下列说法错误的是( )
A . 常温下,NaBF4溶液的pH=7
B . 常温下,H3PO2的电离平衡常数约为1.1
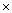 10-2
C . NaH2PO2 溶液中:c(Na+) =c( H2PO2- ) +c( HPO22-) +c(PO23-) +c( H3PO2)
D . 常温下,在0≤pH≤4时,HBF4溶液满足 10-2
C . NaH2PO2 溶液中:c(Na+) =c( H2PO2- ) +c( HPO22-) +c(PO23-) +c( H3PO2)
D . 常温下,在0≤pH≤4时,HBF4溶液满足 
|
|
| 8. 实验探究题 | 详细信息 |
|
NaNO2是一种白色或微黄色斜方晶体,易溶于水,微溶于乙醇。某校同学设计实验制备NaNO2并探究其性质。回答下列问题:
|
|
| 9. 综合题 | 详细信息 |
|
一种利用含AgCl的废渣制取AgNO3的工艺流程如下:
|
|
| 10. 综合题 | 详细信息 | ||||||||||||
|
2019年10月27日,国际清洁能源会议(ICCE2019)在北京开幕,一碳化学成为这次会议的重要议程。甲醇、甲醛(HCHO)等一碳化合物在化工、医药、能源等方面都有广泛的应用。
|
|||||||||||||
高中化学 试卷推荐
- 备考2020年高考化学二轮专题 03 化学中的常用计量
- 辽宁省辽阳市2019-2020学年高二下学期化学期末考试试卷
- 2015-2016学年广东省湛江市廉江一中高三上学期开学化学试卷
- 广东省揭阳市2017-2018学年高三上学期化学期末考试试卷
- 山东省临沂市2017-2018学年高一下学期化学期末考试试卷
- 吉林省白山市抚松县第六中学2019-2020学年高二上学期化学期中考试试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 吉林省长春市榆树市第一高级中学2019-2020学年高三上学期化学期末考试试卷
- 上海市浦东新区2020年高考化学二模试卷
- 广东省阳江市2016-2017学年高二下学期化学期末考试试卷
- 广东肇庆市2020年高考理综-化学三模试卷
- 2015-2016学年山东省济宁市任城区高一下学期期中化学试卷
最近更新
- 人民代表大会制度是我国的根本政治制度。
- .哪些能源是青藏地区特有的洁净能源:A.石油、铀矿B.煤、水能C.秸秆、天然气D.太阳能、地热能
- 如图B-4所示,A、B、C三点都在匀强电场中,已知AC⊥BC,∠ABC=60°,BC=20cm.把一个电荷量q=10-5
- ― Why didn’t you try your best to get on the bus? ― I tried
- 下列对有关实验的变量的叙述,正确的是() A.在探究温度对酶活性影响的实
- 阅读下面的材料,按要求作文。 爱,是润滑剂,是氨基酸,是人生的蜜糖。因为爱,我们的心田碧波荡漾;因为爱,我们的生
- 春晚①书山家屋壁(4分) 贯休 柴门寂寂黍饭馨,山家烟火春雨晴。 庭花蒙蒙水泠泠,小儿啼索树上莺。 【注释】①春晚,即晚
- 要使镜筒上升,可调节( ) A.转换器 B.粗准焦螺旋 C.遮光器 D.反光镜
- 肾动脉中的血液流经肾脏再由肾静脉流出后,血液发生的变化是()A. 尿素减少了 B. 营养物质增加了 C. 氧气增加了 D
- 钱穆曾说“内阁只是皇帝的私人办公厅,不是政府正式的政事堂,内阁学士也只是皇帝的内厅秘书,不是外朝正式宰相之职,于是皇帝在
- —Whata nice model ship! —Thankyou.It ________ me three days
- 根据公司法的规定,公司的决策机构是 A.经理B.股东会或股东大会及董事会C.监事会D.工会组织
- 今有一长2米宽1米的矩形铁皮,如图,在四个角上分别截去一个边长为x米的正方形后,沿虚线折起,做成一个无盖的长方体形水箱(
- 关于合理安排工业用地,叙述正确的是( ) A. 基本无污染的技术密集型和劳动密集型工业,一定要布置在城内居民区内
- (一) 阅读下面的文言文,完成4—7题。(共19分) 龚遂字少卿,山阳南平阳人也。以明经为官,至昌邑郎中
- 补出下列名篇名句中的空缺部分。(任选三题)(6分) (1)己所不欲, 。 三军可夺帅也 ,
- “淡水贵于油”是中东地区的真实写照,下列各项关于“淡水贵”的最主要原因,正确的是 ( ) A、水厂为了赚钱
- 下列说法中正确的是( ) A.在静电场中电场强度为零的位置,电势也一定为零 B.放在静电场中某
- 恩格斯曾说:“文艺复兴”这个名字并没有把这个时代充分表达出来,是因为 A它没有把古代希腊、罗马的文化全部复兴起来 B
- 当人体饮水不足或体内失水过多时,都会引起细胞外液渗透压升高,下丘脑感受到这种刺激后( ) A.垂体合成、分泌并释放







 B
B  E
E 
 NaNO2+PbO(难溶于水),并按下列实验流程制备NaNO2:
NaNO2+PbO(难溶于水),并按下列实验流程制备NaNO2: 



 =2投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图所示。则a (填“>”或“<”)0;压强p1、p2、p3由小到大的关系是。
=2投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图所示。则a (填“>”或“<”)0;压强p1、p2、p3由小到大的关系是。
 CH3NH3+的平衡常数K= (填数值)。
CH3NH3+的平衡常数K= (填数值)。



