人教高中化学一轮复习:专题4氧化还原反应
人教高中化学一轮复习:专题4氧化还原反应
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
向100 mL FeI2溶液中逐渐通入Cl2 , 其中n(I2)、n(Fe3+)随通入n(Cl2)的变化如图所示,下列说法错误的是( )
A . 还原性强弱:Fe2+<I-
B . n(Cl2)=0.12 mol时,溶液中的离子主要有Fe2+、Fe3+、Cl-
C . 由图可知,该FeI2溶液的浓度为1mol·L-l
D . n(Cl2)∶n(FeI2)=1∶2时,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-
|
|
| 2. 单选题 | 详细信息 |
|
Cu和Al的合金2.3g全溶于浓硝酸,若反应中硝酸被还原只产生2.24L的NO2气体和168mL的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入一定量的氢氧化钠溶液,使生成的沉淀的最大质量为( )
A . 4.1275g
B . 4.255g
C . 8.51g
D . 9.62g
|
|
| 3. 单选题 | 详细信息 |
|
向Cu、Cu2O和CuO组成的混合物中,加入1L0.6mol/LHNO3溶液恰好使其完全溶解,同时收集到2240mL NO气体(标准状况)。下列说法中不正确的是(已知:Cu2O+2H+=Cu+Cu2++H2O)( )
A . 上述体现酸性的硝酸与体现氧化性的硝酸其物质的量之比为5:1
B . 若混合物中含0.1 molCu,使该混合物与稀硫酸充分反应,消耗硫酸的物质的量为0.1mol
C . Cu2O跟稀硝酸反应的离子方程式为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O
D . 若将上述混合物用足量的H2加热还原,所得到固体的质量为32g
|
|
| 4. 综合题 | 详细信息 |
|
以下是氮循环的一部分:
|
|
| 5. 单选题 | 详细信息 |
|
已知:2Fe+3Br2=2FeBr3 , Fe2+的还原性大于Br-。现有16.8 g铁和0.3 mol Br2反应后加入水得到澄清溶液后,通入a mol Cl2。则下列叙述错误的是( )
A . 当a=0.1时,发生的反应为2Fe2++Cl2=2Fe3++2Cl-
B . 当a=0.45时,发生的反应为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
C . 若溶液中Br-有一半被氧化时,c(Fe3+)∶c(Br-)∶c(Cl-)=1∶1∶3
D . 当0<a<0.15时,始终有2c(Fe2+)+3c(Fe3+)+c(H+)=c(Cl-)+c(Br-)+c(OH-)
|
|
| 6. 综合题 | 详细信息 |
|
在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一,氰酸盐进一步被氧化为无毒物质。
|
|
| 7. 单选题 | 详细信息 |
|
已知还原性
 。向 。向 和 和 的混合溶液中通入适量氯气,原溶液中各离子的物质的量变化知下图所示( 的混合溶液中通入适量氯气,原溶液中各离子的物质的量变化知下图所示( 和 和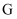 点横坐标为 点横坐标为 和 和 )。下列说法正确的是( ) )。下列说法正确的是( )
A .
 段表示 段表示 物质的量的变化情况
B . 原溶液中 物质的量的变化情况
B . 原溶液中 和 和 的物质的量均为 的物质的量均为 C .
C .  段发生的离子反应为 段发生的离子反应为 D . 反应
D . 反应 不能发生 不能发生
|
|
| 8. 综合题 | 详细信息 |
|
硫酸亚铁是一种补铁剂,某兴趣小组利用经初步处理的含有
 的废液制备硫酸亚铁晶体的流程如下: 的废液制备硫酸亚铁晶体的流程如下:
|
|
| 9. 单选题 | 详细信息 |
|
已知:
 ; ; , 向 , 向 、 、 的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。下列有关说法中,正确的是( ) 的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。下列有关说法中,正确的是( )
A . 还原性:
 B . 原混合溶液中
B . 原混合溶液中 的物质的量为3mol
C . 当通入1mol 的物质的量为3mol
C . 当通入1mol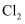 时,溶液中发生的离子反应为 时,溶液中发生的离子反应为 D . 原溶液中:
D . 原溶液中:
|
|
| 10. 单选题 | 详细信息 |
|
雄黄(
 )和雌黄( )和雌黄( )是提取砷的主要矿物原料,二者在自然界中共生, )是提取砷的主要矿物原料,二者在自然界中共生, 和 和 有如下反应: 有如下反应: 。下列说法错误的是( ) 。下列说法错误的是( )
A . 生成
 , 则反应中转移电子的物质的量为5 , 则反应中转移电子的物质的量为5 B . 若将该反应设计成原电池,则
B . 若将该反应设计成原电池,则 应该在负极附近逸出
C . 反应产生的 应该在负极附近逸出
C . 反应产生的 可用 可用 溶液吸收
D . 氧化剂和还原剂的物质的量之比为10:1 溶液吸收
D . 氧化剂和还原剂的物质的量之比为10:1
|
|
高中化学 试卷推荐
- 广东省八校2021-2022学年高一上学期期中调研考试化学试题
- 浙江省温州市2021-2022学年高二上学期12月普通高中学考适应性测试化学试题
- 河北省邯郸市2021-2022学年高三上学期化学开学考试试卷
- 吉林省长春市2021年高考化学模拟试卷
- 山东省济南市2022届高三3月高考模拟考试(一模)化学试题
- 广东省梅州市2020-2021学年高一上学期化学期末考试试卷
- 天津市河西区2021年高考化学三模试卷
- 四川省绵阳市重点中学2021-2022学年高二上学期化学开学考试试卷
- 安徽省宿州市砀山中学2021-2022学年高一上学期化学第一次月考试卷
- 山东省泰安肥城市2020-2021学年高二下学期化学期中考试试卷
- 陕西省宝鸡市金台区2020-2021学年高二上学期化学期中考试试卷(理)
- 河北省定州市2020-2021学年高一下学期化学期末考试试卷
最近更新
- 据统计,在我国网民中染有网瘾的的未成年人高达250万人。要戒除网瘾就应该( )A.关注现实,控制消极情绪B.远离网络,发
- 下列关于孔子思想主张的描述中,不正确的一项是A.“仁”就是要爱人,理解体贴别人,“己所不欲,勿施于人” B.“礼”就是要
- 如图,用直尺和圆规作一个角的平分线,是运用了“全等三角形的对应角相等”这一性 质,由作图所得条件,判定三角形全等运用的方
- (2013苏北三市一模).设想我国宇航员随“嫦娥”号登月飞船贴近月球表面做匀速圆周运动,宇航员测出飞船绕行n圈所用的时
- 已知向量,,且,则实数的值为( ) A. B. C.
- 2008年5月12日,四川汶川发生8级大地震,造成了巨大经济损失和人员伤亡,成为世界瞩目的焦点。早在北宋前期,四川地区商
- (本小题满分12分) 妯图,在直三棱柱中,平面丄侧面 (I )求证:AB丄BC (II)若直线AC与平
- 于2011年开始的全国新一轮县乡人大换届选举工作正在各地进行,参加选举的选民有9亿多人,将选举产生县乡两级人大代表200
- 一位诗人描述某历史人物,说他“生是天骄死鬼雄,全欧震荡气犹龙”;赞美他的主要事功是推动“世间一切人平等”,即使称帝,也仍
- 如图所示,该几何体的主视图应为( )
- 英国资产阶级革命发生的直接原因是 A.资本主义发展 B.斯图亚特王朝厉行专制 C.君主自上而下进行 D.宗教改革运动的推
- 定义max{a,b}=,已知实数x,y满足|x|≤1,|y|≤1,设z= max{x+y,2x-y},则z的取值范围是
- 下列由相关实验现象所推出的结论正确的是 ( ) A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 B
- 随着年龄的增长,中学生王帅开始追求“美”:穿名牌时装以赶上“时代潮流”;用高档手机以显示“大款风度”;抽烟喝酒以表现自己
- 第二节完形填空(共20小题;每小题l.5分,满分30分) 阅读下面短文,从短文后各题所给的四个选项(A、B、C和
- 如图是用燃磷法测定空气中氧气体积分数的实验装置。请你回答下列有关问题。(1)红磷燃烧时冒出浓厚的__ __,反应的化学方
- 设复数,若为实数,则等于A.-2 B.-1
- 若,关于的方程有两个不相等的实数根,则=________
- 一种新型的绿色电池——燃料电池,是把H2、CO、CH4等燃料和空气不断输入,直接氧化,使化学能转化为电能,被称为21世纪
- 设f(x)=-x+1,实数a满足|x-a|<1,求证:|f(x)-f(a)|< 2(|a|+1).



 溶液后,得到白色沉淀,则操作1为,若
溶液后,得到白色沉淀,则操作1为,若 _
_ _
_ _
_ _
_ _
_ _
_
 受热分解的方式分解,则
受热分解的方式分解,则 受热分解的化学方程式为;
受热分解的化学方程式为; 受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则
受热分解的方式分解,且产物中有一种碱性氧化物和两种酸性氧化物生成,则 的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的
的相互转化可用于物质含量的测定,如测定某氯化亚铜样品中CuCl的含量,流程如下:准确称取氯化亚铜样品mg,将其置于过量的 溶液中,发生以下反应:
溶液中,发生以下反应: , 待固体完全溶解后,加入适量稀硫酸,用
, 待固体完全溶解后,加入适量稀硫酸,用 的
的 溶液氧化反应生成的
溶液氧化反应生成的 不被氧化),消耗
不被氧化),消耗 被还原为
被还原为 。则样品中CuCl的质量分数为。
。则样品中CuCl的质量分数为。




