中考化学试题
(2019·滨州)钙元素是一种重要的金属元素,它可组成氢化钙、氢氧化钙等多种物质。
(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂。某实验探究小组的同学通过查阅资料得知,氢化钙在常温下能与水反应生成氢氧化钙和氢气,请你写出该反应的化学方程式: 。
(2)该实验探究小组将Na2CO3溶液滴加到Ca(OH)2 溶液中,充分反应后过滤,得到滤液和滤渣,经检验滤渣的成分是碳酸钙。
(提出问题)
滤液中溶质的成分是什么?
(猜想与假设)
猜想一:NaOH;
猜想二:NaOH和Ca(OH)2;
猜想三:NaOH和 ;
猜想四:NaOH、Na2CO3和Ca(OH)2。
经过讨论,大家认为猜想四不合理,原因是
。
(实验过程)
| 实验步骤 | 现象 | 结论 |
| 步骤Ⅰ:取滤液,向其中滴加适量的Na2CO3溶液 |
| 猜想二不成立 |
| 步骤Ⅱ:另取滤液,向其中加入足量的 溶液 | 产生气泡 | 猜想 成立 |
(拓展延伸)在分析反应后所得物质的成分时,除考虑生成物外,还需考虑 。
兴趣小组同学模仿工业高炉炼铁原理,用图 1 实验装置 ( 加热装置已省略 ) 探究治炼铜的化学原理。实验操作过程如下:


①将 CuO 加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量的焦炭,再向试管里通入干燥的 CO 2 ,此时用仪器测得 CO 2 含量为 a g/L ,用气球密封试管口。
②用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,随后熄灭酒精灯。
③高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图 1 中虚线框部位,数据输出得到图 11 。恢复至与 ①相同的条件测得 CO 2 含量为 0.2 a g/L 。
④再次用酒精灯加热氧化铜部位, 1 分钟左右黑色固体变成紫红色。
( 1 ) 操作 ②中实验现象说明 CO 2 ___________ ( 选填 “ 能 ” 或 “ 不能 ”) 与 CuO 反应。
( 2 ) 操作 ③中 CO 2 含量减小的原因是 __________ 。
( 3 ) 操作 ④中的化学反应方程式为 _____________ 。
( 4 ) 实验结束后,一般将装置内的气体灼烧处理,目的是 _________ 。
( 5 ) 由图 2 可知,刚停止加热后焦炭区温度降低更快,可能的原因是 _______ 。
一定条件下, A 和 B 反应生成 C 和 D 。反应前后分子种类变化的微观示意图如下所示:

( 1 ) 一个 B 分子中含有 ________ 个原子;
( 2 ) A 、 B 、 C 中属于化合物的是 ________ ;(填字母序号)
( 3 ) 写出 C 在通电条件下分解的方程式 ______________ 。
( 4 ) ①若 D 为空气中体积分数最大的气体,则该反应中生成的 C 和 D 的质量比为 __________ ;(填最简整数比)
②若 D 为氧化物,且 A 和 B 的分子个数比为 7 ∶ 4 ,则该反应的化学方程式为 _____________ 。
“庄稼一枝花,全靠肥当家。”下列属于复合肥料的是
A . NH 4 HCO 3 B . KCl C . (NH 4 ) 2 HPO 4 D . CO(NH 2 ) 2
以下属于化学变化的事例是
A. 冰雪融化 B. 纸张燃烧
C. 石蜡熔化 D. 酒精挥发
甲、乙是初中化学中常见的物质。如图1所示,甲发生一步反应转化为乙有两种途径,乙发生一步反应转化为甲,下列说法错误的是

A.若甲是Fe3O4,则乙是Fe
B.若乙是金属,则单质、氧化物中可能含有同种元素
C.若甲的相对分子质量比乙小16,则甲、乙一定分别是H2和H2O
D.若甲是氧化物,则反应①和③的基本反应类型不一定相同
金属材料在生活、生产中有广泛的应用。请回答下列问题:
(1)生活中用铁锅炒菜,主要利用了铁的__________________性。
(2)工业上用赤铁矿(主要成分为氧化铁)炼铁,其反应原理是________________(化学方程式表示)
(3)2020年6月21日,时速600公里的高速磁悬浮试验样车成功试跑,制造样车外壳的主要材料是铝合金。铝合金与纯铝相比具有的优点是______________(写出一点即可)。
(4)金属资源有限,不能再生。写出防止铁生锈的一种方法___________________。
蔬菜、水果是人类餐桌上的必备食物。
(1)食用果蔬前,用清水浸泡可适当降低农药残留。浸泡时间对农药去除率的影响如图所示,分析图示得到的结论是 。

(2020·淄博模拟)“宏观辨识与微观探析”是化学学科的核心素养之一、下列解释错误的是( )
A. 电解水生成氢气和氧气——化学变化中分子发生改变
B. 众人拾柴火焰高——可燃物越多,着火点越低,越易燃烧
C. 切开成熟的菠萝蜜能闻到浓浓的香味——分子在不断地运动
D. 用明矾净水——明矾可促进水中悬浮物的沉降
在化学实验中,很多因素对化学实验的现象或结果有影响。
(1)钢铁在夏天比冬天更易生锈,这个实例说明了什么?
(2)相同温度下,碘和高锰酸钾分别在等量的汽油中溶解的量不同,这个实例说明了什么?
下图A-H是实验室制取某些常见气体的装置示意图。请完成下列相关问题。

(1)写出图中仪器②的名称___________。
(2)实验室要制取一瓶干燥的氧气所选择的装置是___________(填序号);
(3)实验室制备CO2的化学方程式为_________,若用装置H收集CO2气体,产生的气体应从___(填“a”或“b”)端通入。
(4)用石灰石和稀盐酸制取二氧化碳,选取装置C或D相对于装置B在操作方面的优势为____________;若选择装置D用双氧水和二氧化锰制备氧气,能否体现该优点___(填“能”或“否”);
(5)用排水法与排空气法收集CO2及相关性质的比较(分别用体积相同的2个集气瓶收集)。
已知:向收集满CO2的集气瓶内倒入等体积适量澄清石灰水,并振荡。二氧化碳纯度越高,澄清石灰水先变浑浊后变澄清的时间越短。
| 比较项目 | 排水法 | 向上排空气法 |
| 收集方法可行性分析 | CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率 | _____,且不与空气发生反应。 |
| 收集过程分析 | 集满现象:______。 | “验满”分析:因气体无色,是否集满难确定,即便用燃着的木条移近容器口熄灭,也难以证明空气完全排尽。 |
| 石灰水变浑浊又变澄清所需时间分析 | 时间较短。 | 时间较长。 |
由上述实验可得结论:①二氧化碳可用排水法或向上排空气法收集;
②与排空气法相比,排水法的优点是_______。
化学实验操作的规范性、安全性是实验成败的关键。下列实验操作中正确的是( )
A. 点燃酒精灯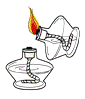
B. 测定空气中氧气含量
C. 测定溶液的pH
D. 稀释浓硫酸
A~J 是初中化学常见的物质,其中 B 与 D 可配制波尔多液 F 是黑色氧化物、 I 是紫红色金属,它们之间的转化关系如图所示 ( 反应条件已略去 ) 。请回答下列问题:

(1)I 的化学式为 _______ 。
(2)G 的一种用途是 _______ 。
(3) 反应 ② 的基本反应类型为 _______ 。
(4) 反应 ③ 的化学方程式为 _______ 。
下列图像不能正确反映对应变化关系的是
A .  一定量的镁在过量的氧气中充分燃烧
一定量的镁在过量的氧气中充分燃烧
B .  向稀硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液至过量
向稀硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液至过量
C .  向等质量等浓度的稀盐酸中分别加入铝和镁至过量
向等质量等浓度的稀盐酸中分别加入铝和镁至过量
D .  加热一定量的高锰酸钾固体
加热一定量的高锰酸钾固体
(2020·都江堰模拟)下列客观事实与对应微观解释错误的是( )
| 选项 | 客观事实 | 微观解释 |
| A | 糖块放入水中慢慢“消失” | 分子不停运动 |
| B | 酒精和水混合后体积减小 | 分子间有间隙 |
| C | 金刚石硬度比石墨大 | 碳原子的结构不同 |
| D | 水和过氧化氢的化学性质不同 | 构成它们的分子不同 |
请你根据所学知识并结合如图所示装置回答有关问题。

( 1 )装置 D 中仪器 a 的名称是 ______ 。
( 2 )实验室用装置 B 制取氧气,反应的化学方程式为 ______ 。
( 3 )实验室制取氢气选用的装置组合是 ______ 。
( 4 )若用 F 装置收集二氧化碳。气体应从 ______ (填 “ m ”或“ n ”)端通入。
利用厨房用品能完成的实验是( )
A.检验鸡蛋壳中是否含有碳酸钙
B.检验自来水中是否含有氯离子
C.测定蔬菜中农药的残留量
D.比较食用油与水的密度大小
实验是科学探究的重要手段,下列化学实验操作正确的是( )
A. 测溶液pH B.
测溶液pH B. 稀释浓硫酸
稀释浓硫酸
C. 倾倒液体 D.
倾倒液体 D. 取用固体药品
取用固体药品
用氯酸钾制取 ,下列化学方程式正确的是
A . 

C . 
下列物质中,既含有分子又含有离子的是()
A.生铁
B.浓盐酸
C.干冰
D.医用酒精
- 在人体下列结构中,不直接参与体温调节的是( ) A.下丘脑 B.大脑皮层的中央前回 C.皮肤 D.肾
- 提取下面材料中的要点,整合成一个单句,给“寒食节”下定义。(不超过40个字)(4分)①寒食节是我国民间的一个节日。②寒食
- 对,定义一种新运算,规定:(,)(其中、均为非零常数),这里等式右边是通常的四则运算,例如:(,). (1)已知(,),
- 中国人民银行宣布自2012年6月8日起,人民币存款基准利率下降0.25个百分点,同时,将金融机构存款利率浮动区间的上限调
- 若(﹣7m+A)(4n+B)=16n2﹣49m2,则A=,B=.
- 与双曲线有共同的渐近线,且经过点P(1,4)的双曲线方程为( ) A. B. C.
- 【历史上重大改革回眸】 材料一 《现代人》杂志上的一篇文章指出“俄罗斯好像从睡梦中醒来……人人都感觉有一根神经破裂了,
- Charles Dickens wrote many novels to catch people’s _______
- 下列词语中,没有错别字的一组是( ) A.蠕动 搅绊 寥若辰星
- 如图,在平面直角坐标系中,点A1是以原点O为圆心,半径为2的圆与过点(0,1)且平行于x轴的直线l1的一个交点;点A2是
- 2009年5月14日,欧盟理事会就蜡烛反倾销案发布终裁裁决,我国5家企业获得零税率。这是中国积极应对欧盟反倾销案的又一胜
- 黑火药是我国古代四大发明之一.黑火药爆炸的原理可以用下式表示:2KNO3+3C+SK2S+N2↑+3X↑,根据质量守恒定
- 请给出区分下列各组物质的具体方法(请写出实验的过程、现象及结论) (1)水和酒精
- 以争夺海洋资源、控制海洋空间、抢占海洋科技制高点为主要特征的21世纪国际海洋权益斗争呈现出日益加剧的趋势。在新一轮的海洋
- “当今世界20万亿美元的国民生产总值中,美欧各占5万亿美元,日本3万亿美元……这也是共同分担国际责任的结构比例,要建立国
- 初二年的学习告诉我们,生活会引发人们的思考,把自己的思考写出来,或阐明观点,或提出主张,或表面态度,这样的文章就是议论文
- 某物质由碳、氢、氧三种元素组成,图甲是该物质的元素质量分数圆饼图,图乙为该物质的分子结构模型图.据图分析,下列关于该物质
- 阅读《爬上窗台的绿色》选段,完成9~12题。(17分) ①窗台在二楼,那晌午里散着泥土糙香、夜晚嚼着寒露沁凉的绿色就顺着
- “”、“”、“”分别表示A、B、C三种物质的分子,下图形象的表示了某化学反应前后反应物与生成物的分子及数目变化。(1)该
- 下列事例中,通过做功使物体内能增加的是( ) A.夏天,在阳光照射下路面的温度升高 B.冬天,用嘴对着手“呵气”,



