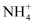二氧化硫的漂白作用 知识点题库
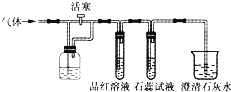
如图所示装置,若关闭活塞,则品红溶液无变化,石蕊试液变红,澄清石灰水变浑浊.若打开活塞,则品红溶液褪色,石蕊试液变红,澄清石灰水变浑浊.据此判断该气体和广口瓶中盛放的物质分别是( )
如图制取SO2并验证SO2性质的装置图
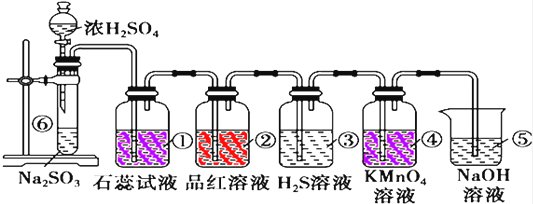
已知Na2SO3+H2SO4=Na2SO4+SO2+H2O
(1)①中为紫色石蕊试液,实验现象为 实验证明SO2是 气体
(2)②中为红色品红溶液,现象为 证明SO2有 性
(3)④为紫红色高锰酸钾,实验现象为 证明SO2有 性.
(4)⑤的作用 反应方程式 .
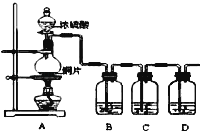
某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如图所示的装置.
请回答下列问题.
(1)铜和浓硫酸反应的化学方程式为
(2)B瓶中盛有品红溶液,观察到品红溶液褪色,这是因为 SO2具有 (填选项的字母,下同),C瓶中盛有新制的氯水,观察到氯水褪色,这是因为SO2具有 .
A.氧化性 B.还原性 C.漂白性
(3)D瓶中盛有NaOH溶液,作用是 .
(4)充分反应后,小组同学发现铜和硫酸都有剩余.若想使剩余的铜片溶解,可再加入(多选) (填选项的字母).
A.HNO3 B.NaNO3 C.Fe2O3 D.Na2CO3 .
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置.
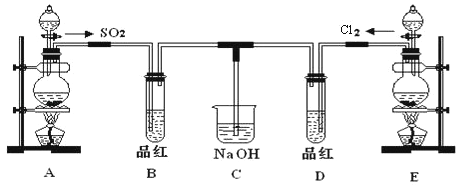
(1)实验室用装置A制备SO2 . 某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是: ;
(2)实验室用装置E制备Cl2 , 其反应的离子方程式为: .若有6mol的HCl参加反应,则转移的电子总数为 ;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B: ,D: .
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B: ,D: .
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强.他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样.请你分析该现象的原因(用离子方程式表示) .
-
(1) 写出氯化钡的电子式
-
(2) 盐溶液甲中可能含有的下列物质中的
A.Na2CO3
B.Na2SO3
C.NaHSO3
D.NaNO3
-
(3) 写出气体乙通入氯化铁溶液时的离子方程式
-
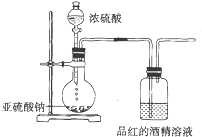
(1) 制备SO2气体的反应方程式为:.发生装置的玻璃仪器名称为、.
-
(2) 为了探究干燥的SO2能不能使品红褪色,某同学设计了如图所示实验装置,请指出实验装置设计中的不合理之处.
①;②
-
(3) 按照修改后的装置,实验中控制SO2以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色,这说明品红褪色不是SO2直接导致的.据此,SO2能使品红的水溶液褪色的可能微粒有(不考虑水及水电离出来的粒子).
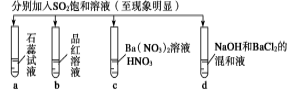
| A | 无色 | 无色 | 无现象 | 无色沉淀 |
| B | 红色 | 无色 | 白色沉淀 | 白色沉淀 |
| C | 红色 | 无色 | 无色溶液 | 白色沉淀 |
| D | 无色 | 无色 | 无色溶液 | 无色沉淀 |
-
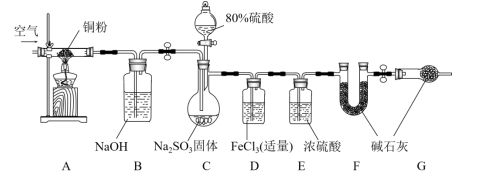
(1) C中发生反应的化学方程式是,B装置的名称是,关于该套装置说法正确的是(填标号)。
a 组装仪器、加入药品后检查气密性 b 实验开始和最后时均需要通入空气
c 利用A、B装置是为了减小实验误差 d F、G中的碱石灰可以换为无水CaCl2
-
(2) 甲同学认为很快可以看到D装置的现象,他的依据是(用离子方程式表示)。乙同学做实验时发现和甲同学预测的现象不一样,先出现棕红色,经过一段时间后变为浅绿色。于是查阅资料发现反应分为两步:
第一步:
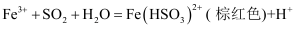 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)如果需要验证第一步反应是快反应,可以事先在D装置中滴加数滴试剂,相应的实验现象是。
-
(3) 学习小组通过实验后D和F装置中的数据来计算SO2的质量。D中加入足量的BaCl2溶液充分反应,经过操作,测得沉淀为m1g,F的质量差为m2g,C中产生SO2的体积(标准状况下)为L。该实验的设计中,仍然存在系统误差的可能原因是。
 浓度增大
浓度增大
| 操作和现象 | 结论 | |
| A | 向氯水中加入硝酸银溶液,有白色沉淀产生 | 氯水中已无Cl2 |
| B | 将SO2通入酸性高锰酸钾溶液,溶液紫色褪去 | SO2具有漂白性 |
| C | 向FeCl3和CuCl2混合溶液中加入少量铁粉,没有红色固体析出 | 氧化性:Fe3+>Cu2+ |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中含有SO42- |
-
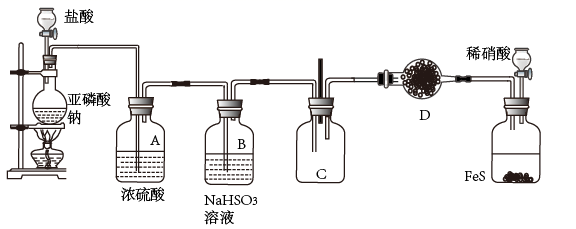
(1) 图中装置顺序错误的是;使用错误的药品是。
-
(2) 制取硫化氢的离子方程式为,制取二氧化硫的离子方程式为:。
-
(3) C中反应的化学方程式为: 。
-
(4) 将C导出的气体通入溶液可检验是否含有SO2。
-
(5) D中可选的干燥剂是,装置B的作用是,B中反应的离子方程式为:。
-
(6) 若用A代替D来干燥H2S产生的后果用化学方程式表示为:。
-
(7) 反应结束后,洗涤C瓶应先加入或。
-
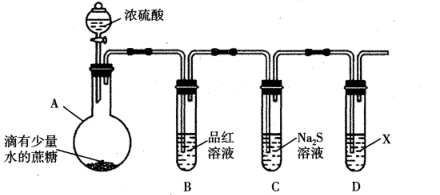
(1) 仪器A的名称是。
-
(2) A中滴入浓硫酸后,观察到蔗糖逐渐变黑,这是因为浓硫酸有性;之后观察到的现象是,有关反应的化学方程式是;蔗糖中滴加少量水的目的是。
-
(3) 装置B中观察到的现象是,由此得出的结论是。
-
(4) 装置C中观察到的现象是。
-
(5) 为证明实验最终排放的气体不污染空气,装置D中的X应是,试管中的现象是。
选项 | 实验操作 | 现象 | 解释或结论 |
A | 向某溶液中滴加盐酸,再将产生的无色气体通入品红溶液 | 品红溶液褪色 | 原溶液中一定存在 |
B | 向某溶液中滴加稀氢氧化钠溶液,将湿润的红色石蕊试纸置于试管口 | 红色石蕊试纸不变色 | 原溶液中一定不存在 |
C | 向某溶液中滴加硝酸,无明显现象,再加入硝酸银溶液 | 有白色沉淀产生 | 原溶液中一定存在 |
D | 将某溶液进行焰色试验 | 火焰呈黄色 | 原溶液中一定不存在 |
 , 既可以杀菌,又可防止营养成分被氧化
C .
, 既可以杀菌,又可防止营养成分被氧化
C .  通入
通入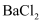 中,生成白色沉淀
D . 浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸
中,生成白色沉淀
D . 浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸
- 化学实验过程中要规范操作,注意实验安全。下列做法中正确的是 A.用嘴吹灭酒精灯的火焰 B.加热后的试管立即用水冲洗 C.
- It’s impolite to read _______ letter .A.else someone’sB.some
- 5.促进人类与环境统一,下列措施中正确的是() A.森林采伐量应高于木材自然增长率 B.在呼伦贝尔草
- 计算的结果是(). A. B. C. D.
- 下列说法正确的是( ) A.元素性质随原子序数的递增呈周期性变化的根本原因是元素的化合价呈周期性变化 B.核外电子
- 假如你沿着赤道步行绕地球一周,若每天走50千米,需要行走() A. 80天 B. 800天
- 为电视连续剧《武则天》布置场景,场景中最有可能出现的是 A.城市“买卖昼夜不绝” B
- 接种卡介苗一段时间后,血液中就会出现结核杆菌抗体,抗体的基本单位、产生抗体的细胞及合成抗体的细胞器依次是 A.氨基
- 如图所示,下列几何体各自的三视图中,有且仅有两个视图相同的是 () A.②③ B.①③
- 2011年10月12日,美国参议院通过了针对中国操纵人民币汇率的2011年货币汇率监督改革法案,该议案主要针对中国,旨在
- 下列句子顺序排列正确的一项是( )。(2分)______________________。这是2010上海世博会为公众所
- 如图甲,一理想变压器原、副线圈匝数比n1∶n2=11∶5,原线圈与正弦交变电源连接,输入电压u随时间t的变化规律如图乙所
- 有失去标签的硝酸钾、碳酸钠、硝酸银、硝酸钙和稀盐酸五瓶溶液。将其任意编号:A、B、C、D、E,进行两两混合,其现象如下表
- 下列事件与二月革命的性质相同的有 ( ) ①太平天国运动 ②戊戌变法 ③
- 我国目前采用的北京时间是( ) A.北京的地方时 B.北京所在经线的时间 C.北京所在的东8
- “夫珠玉金银,饥不可食,寒不可衣”,但人们还是喜欢金银。这表明金银作为货币 ①是商品经济发展到一定阶段的产物 ②货币
- ---Would yoube so kind as to close the window? ---_________.
- 可逆反应从正方向开始,并达到了平衡,此时和的物质的量之比为2:1,若采取某种措施,导致和又消耗了一些,并再次达到平衡,下
- 如图,rABC的内部有一点P,且D、E、F是P分别以AB、BC、AC为对称轴的对称点。若rABC的内角ÐA=70°,ÐB
- 对下列划线词解释有误的一项是( ) A 乃传言开壁门 传令、下令 B 损其家口,充狙之欲