物质的量与其浓度和气体摩尔体积的综合应用 知识点题库
下列叙述正确的是( )
A . 同温同压下,相同体积的物质,其物质的量一定相等
B . 任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等
C . 1 L一氧化碳气体一定比1 L氧气的质量小
D . 相同条件下的一氧化碳气体和氮气,若物质的量相等则体积相等,但质量不相等
在标准状况下,将aLNH3完全溶于水得到V mL氨水,溶液的密度为ρg/cm3 , 溶质的质量分数为ω,溶质的物质的量浓度为cmol/L.下列叙述中正确的是( )
A . ω=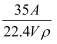 ×100%
B . c=
×100%
B . c=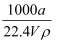 ×100%mol/L
C . 上述溶液中再加入1.5VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(NH4+)>c(Cl﹣)>c(H+)>c(OH﹣)
D . 上述氨水中再加入V mL水后,所得溶液的质量分数大于0.5ω
×100%mol/L
C . 上述溶液中再加入1.5VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(NH4+)>c(Cl﹣)>c(H+)>c(OH﹣)
D . 上述氨水中再加入V mL水后,所得溶液的质量分数大于0.5ω
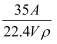 ×100%
B . c=
×100%
B . c=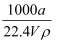 ×100%mol/L
C . 上述溶液中再加入1.5VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(NH4+)>c(Cl﹣)>c(H+)>c(OH﹣)
D . 上述氨水中再加入V mL水后,所得溶液的质量分数大于0.5ω
×100%mol/L
C . 上述溶液中再加入1.5VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(NH4+)>c(Cl﹣)>c(H+)>c(OH﹣)
D . 上述氨水中再加入V mL水后,所得溶液的质量分数大于0.5ω
如果a g某气体中含有b个分子,则c g该气体在标准状况下的体积是(NA为阿伏加德罗常数)( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下列有关NA的叙述正确的是( )
A . 某无水乙醇与足量金属钠反应生成5.6LH2(标况),则该乙醇分子中共价键总数为4NA
B . 标况下,22.4L甲烷与22.4L氯气在光照下充分反应,生成的CH3Cl分子数一定为NA
C . 在密闭容器中加入1.5 mol H2和0.5 mol N2 , 充分反应后得到NH3分子数为NA
D . 常温常压,56g铁片投入足量浓硫酸中生成SO2分子数为NA
设NA为阿伏加德罗常数的数值.下列说法正确的是( )
A . 50mL18.4mol•L﹣1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
B . 若由CO2和O2组成的混合物中共有NA个分子,则其中的氧原子数为2NA
C . 某密闭容器盛有0.1molN2和0.3molH2 , 充分反应后转移电子的数目为0.6NA
D . 常温下,1L0.1mol•L﹣1NH4NO3溶液中的氢原子数为0.4NA
在一定温度下,Cl2通入到1L 0.7 mol· L-1的NaOH溶液中,恰好生成NaCl、NaClO、NaClO3 , 其中生成NaCl和NaClO的物质的量之比为11:1,求:
-
(1) 生成NaClO3的物质的量是
-
(2) 通入的Cl2在标准状况下的体积
标准状况下,①6.72L NH3 ②1.204×1023个CO2 ③6.4g CH4 ④0.5mol HCl,下列关系错误的是( )
A . 体积大小:④>③>①>②
B . 原子数目:③>①>④>②
C . 密度大小:②>④>①>③
D . 质量大小:④>③>②>①
下列数量的各物质中,含分子个数最多的是( )
A . 1mol HCl
B . 3.01×1023个氧分子
C . 22g CO
D . 标况下5.6L H2
某三原子分子构成的气体mg,其摩尔质量为Mg·mol-1 , 阿伏加德罗常数为NA , 则:
①该气体在标准状况下的体积为L;
②该气体在标准状况下的密度为g·L-1;
③该气体所含的原子总数为个;
④该气体一个分子的质量为g。
已知NH3气体34.0g,求:
-
(1) NH4+的物质的量为mol;
-
(2) NH3所含分子总数为个;
-
(3) NH3在标准状况下的体积为L;
-
(4) NH3溶于水后形成2L溶液,其溶液的物质的量浓度为 mol/L。
相同物质的量浓度的NaCl、MgCl2、AlCl3三种溶液,其c(Cl-)之比是( )
A . 1:2:3
B . 3:2: 1
C . 1:1:1
D . 6:3: 1
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 0.1 mol丙烯中含有的双键数目为0.3 NA
B . 标准状况下,2.24LH2O中含有的共价键数目为0.2NA
C . 6.2 g白磷分子中含P—P键为0.2 NA
D . 7.8 g Na2O2和Na2S的固体混合物中含有的离子总数为0.3 NA
-
(1) 3.6克H2O的物质的量是,含有个H2O。
-
(2) 物质的量浓度为18.4 mol·L-1 , 密度为1.84 g·mL-1的硫酸的质量分数为 ,配制1000 mL浓度为1.84 mol·L-1 的硫酸,需要物质的量浓度为18.4 mol·L-1的硫酸L。
-
(3) 将190 g MgCl2溶于水配制成1 L溶液。溶液中MgCl2的物质的量浓度为。从中取出50 mL溶液,含有Cl-的物质的量为。
已知  为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
A . 标准状况下,22.4L HF含有电子数为10NA
B . 12g金刚石中,含C—C键数目为2 NA
C .  溶液中含
溶液中含  数为
数为  D . 密闭容器中
D . 密闭容器中 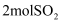 与
与 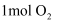 反应,生成
反应,生成 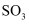 的分子数为
的分子数为 
 溶液中含
溶液中含  数为
数为  D . 密闭容器中
D . 密闭容器中 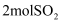 与
与 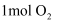 反应,生成
反应,生成 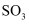 的分子数为
的分子数为 
如图所示,相同状况下,分别用氯化氢和四种混合气体吹出体积相等的五个气球。A、B、C、D四个气球中所含原子数与氯化氢气球中所含原子数一定相等的是( )
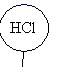
A . 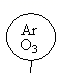 B .
B . 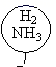 C .
C . 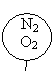 D .
D . 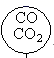
 B .
B . 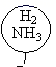 C .
C .  D .
D . 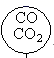
设 NA 为阿伏加德罗常数的值,下列说法正确的是( )
A . 标准状况下,1 L 己烷完全燃烧后,所生成的气态产物的分子数为 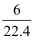 NA
B . 10 g 46%的乙醇溶液中氢原子的个数为 0.6 NA
C . 28 g 乙烯与丙烯的混合气体,共用的电子对数为 6 NA
D . 100 mL 0.1 mol/L CH3COOH 溶液跟足量乙醇、浓硫酸共热,发生酯化反应,生成乙酸乙酯分子 数为 0.01 NA
NA
B . 10 g 46%的乙醇溶液中氢原子的个数为 0.6 NA
C . 28 g 乙烯与丙烯的混合气体,共用的电子对数为 6 NA
D . 100 mL 0.1 mol/L CH3COOH 溶液跟足量乙醇、浓硫酸共热,发生酯化反应,生成乙酸乙酯分子 数为 0.01 NA
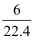 NA
B . 10 g 46%的乙醇溶液中氢原子的个数为 0.6 NA
C . 28 g 乙烯与丙烯的混合气体,共用的电子对数为 6 NA
D . 100 mL 0.1 mol/L CH3COOH 溶液跟足量乙醇、浓硫酸共热,发生酯化反应,生成乙酸乙酯分子 数为 0.01 NA
NA
B . 10 g 46%的乙醇溶液中氢原子的个数为 0.6 NA
C . 28 g 乙烯与丙烯的混合气体,共用的电子对数为 6 NA
D . 100 mL 0.1 mol/L CH3COOH 溶液跟足量乙醇、浓硫酸共热,发生酯化反应,生成乙酸乙酯分子 数为 0.01 NA
NA是阿伏加德罗常数的值。下列说法正确的是( )
A . 1 mol SiO2中含有2 mol硅氧键
B . 1 mol T2O比1 mol H2O多4 NA个中子
C . 1 L 0.1 mol/LNa2CO3溶液中含有的阴离子的总数为0.1 NA
D . 标准状况下,1 mol O2和O3的混合物中有5NA个氧原子
用8.70g
MnO2与100mL 36.5%密度为1.20g/cm3的浓盐酸共热(假设HCl没有损失且MnO2被完全消耗),请回答(要求写出运算过程)
-
(1) 求出浓盐酸的物质的量浓度
-
(2) 反应中生成的Cl2在标准状况下的体积。
NA代表阿伏加德罗常数,下列叙述正确的是( )
A . 3.2g氧气含有的质子数为8NA
B . 1L 0.1mol/L Na2SO4水溶液,含有的氧原子数为0.4 NA
C . 1mol Na与O2完全反应生成Na2O2 , 转移电子数为NA
D . 相同物质的量的CO和CO2气体所含碳原子数均为NA
已知 催化氧化生成
催化氧化生成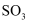 的热化学方程式为
的热化学方程式为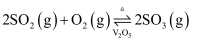
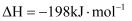 。设
。设 为阿伏加德罗常数的值。下列有关叙述正确的是( )
为阿伏加德罗常数的值。下列有关叙述正确的是( )
 催化氧化生成
催化氧化生成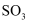 的热化学方程式为
的热化学方程式为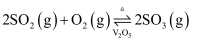
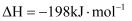 。设
。设 为阿伏加德罗常数的值。下列有关叙述正确的是( )
为阿伏加德罗常数的值。下列有关叙述正确的是( )
A . 1mol 和
和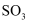 混合气体中硫原子数目为
混合气体中硫原子数目为 B . 等物质的量的
B . 等物质的量的 和
和 ,
,  的中子数比
的中子数比 的中子数多
的中子数多 C . 当放出39.6kJ热量时,消耗
C . 当放出39.6kJ热量时,消耗 的分子数为
的分子数为 D . 标准状况下,
D . 标准状况下,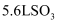 中所含有的原子数目为
中所含有的原子数目为
 和
和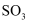 混合气体中硫原子数目为
混合气体中硫原子数目为 B . 等物质的量的
B . 等物质的量的 和
和 ,
,  的中子数比
的中子数比 的中子数多
的中子数多 C . 当放出39.6kJ热量时,消耗
C . 当放出39.6kJ热量时,消耗 的分子数为
的分子数为 D . 标准状况下,
D . 标准状况下,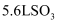 中所含有的原子数目为
中所含有的原子数目为
最近更新
- —How do you like this film? —__________. A.I enjoy it verymu
- 读“最近100年来海平面的变化图”,判断问题。根据图中“海平面上升曲线”,近100年来世界气温:( ) A.呈直线
- 下面有关晶体的叙述中,不正确的是 A.在石墨晶体中,每一层中的C原子均以共价键结合,所以石墨是原子晶体 B.氯化钠晶体中
- 若关于x的方程=+2产生增根,那么m的值是.
- ①曾经的初中,我是她的班主任,而她和我,却对抗了两年,在她黑色封面的日记本里,我是第一个被她写进“死亡日记”的人。
- 【广西柳州市】下列句子中加点词语有错别字的一项是( ) A.一个老城,有山有水,在天底下晒着阳光,安适地睡着,只
- 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )选项 实验 现象 结论 A 将打磨过的铝条插入1
- 唐代,我国境内生活着许多少数民族,他们都曾以各种方式与唐朝建立密切联系。唐玄宗时,有一少数民族赞普上表自称“外甥”,与唐
- 27. 1974年在联合国大会上发言说:“新的世界大战的危险依然存在……当前世界的主要倾向是革命。”但在80年代初,他却
- 下列电离方程式中,正确的是A. Ca(OH)2==Ca2++2(OH)- B. FeCl2==Fe2++3
- ________ amazed usgreatly was that Linda could speak five la
- ......
- 11.阅读下面的文字。完成(1)~(4)题。(25分) 吊炕 许福元 吊炕,就是将土炕吊起来。行吗?去了“吗”就行。…
- 下列验证Zn、Fe、Ag三种金属活动性顺序的实验方案中(“—”表示未进行金属与盐溶液之间的实验),不能达到实验目的的是(
- A、B、C、D、E均为可溶于水的固体,组成它们的离子有分别取它们的水溶液进行实验,结果如下:①A溶液与B溶液反应生成白色
- 下列哪项不是与家兔食草生活相适应的特点?( ) A.犬齿发达 B.消化管长 C.盲肠发达
- 如图,点A、B、C在⊙O上,∠AOC=70°,则∠ABC的度数为 A、10°; B、20°;
- 商鞅在变法时曾说:“治世不一道,便国不法古”,他宣传这种观点的直接目的是 A.建立君主的专制统治
- 水杨酸是合成阿司匹林的重要原料。水杨酸的学名是邻羟基苯甲酸,结构简式为请回答下列问题。(1)请写出与水杨酸互为同分异构体
- 某水上运动项目使用的长方体水上标志物,经测量其质量为100kg、体积为0.2m3,它的密度为kg/ m3。它漂浮在平静的



