原子结构的构造原理 知识点题库
人们常将在同一原子轨道上运动的,自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”.以下有关主族元素原子的“未成对电子”的说法,错误的是( )
A . 核外电子数为奇数的基态原子,其原子轨道中一定含有“未成对电子”
B . 核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子”
C . 核外电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子”
D . 核外电子数为奇数的基态原子,其原子轨道中可能不含“未成对电子”
构造原理揭示的电子排布能及顺序,实质是各能级能量高低顺序.则下列能级的能量高低顺序正确的是( )
A . 5s>4f>4s>3d
B . 3d>4s>3p>3s
C . 4s>3s>2s>1s
D . 5s>4s>4f>3d
下列多电子原子的原子轨道能量高低顺序正确的是( )
A . 2s>3s
B . 2s>2d
C . 2px<2Py
D . 2px=2py
根据泡利的原子轨道能级图和“能级交错”现象,原子轨道的能量高低顺序是:ns<(n﹣3)g<(n﹣2)f<(n﹣1)d<np(n为能层序数,g能级中有9个轨道).则未来的第八周期应包括的元素的种类是( )
A . 32
B . 50
C . 64
D . 128
若将15P原子的电子排布式写成1s22s22p63s23px23py1 , 它违背了( )
A . 能量守恒原理
B . 泡利不相容原理
C . 洪特规则
D . 能量最低原理
如图1为周期表的一部分,表中所列的字母分别代表一种化学元素。回答下列问题: 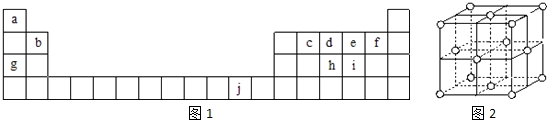
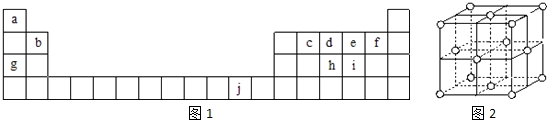
-
(1) f的基态原子核外电子排布式。
-
(2) 在c2a4分子中,c为杂化,c与c间存在的共价键类型有两种。
-
(3) ci2与ce2比较,沸点较高的是(写分子式)。
-
(4) 将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液。深蓝色溶液中是由于存在(写结构式)
-
(5) j的金属晶体的晶胞如图2所示,则一个晶胞中每个j原子周围与它最接近且距离相等的j共有的个数是个,已知该元素的相对原子质量为64,单质晶体的密度为ρg•cm-3 , 阿伏加德罗常数的值为NA , 试求铜的金属半径为 pm(用含NA、ρ的表达式表达)。
下列能级能量由小到大排列顺序正确的是()
A . 3s 3p 3d 4s
B . 4s 4p 3d 4d
C . 4s 3d 4p 5s
D . 1s 2s 3s 2p
以下是摘自高二实验班某学生在这次考试复习中对教材选修3第一章《原子结构和性质》的总结,其中与教材说法不符的是( )
A . 同一原子的能层越高,s电子云半径越大
B . 任一能层的能级总是从s能级开始,而且能级数等于该能层序数
C . 书写电子排布式时,按照构造原理,依据电子的填充顺序从左到右书写能级
D . 处于最低能量的原子叫做基态原子,我们通常所说的电子排布指的是基态原子的电子排布
-
(1) 镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。已知:SeO2在常温下是白色的晶体,熔点为340-350℃,则SeO2晶体属于晶体,SeO2中Se原子采取的杂化类型为。
-
(2) A、X、Y、Z、W、M、G等原子序数一次增大的前四周期元素
元素
相关信息
A
原子核外电子总数与其周期数相同
X
其羞态原子的L层中有3个未成对电子
Y
荃态原子的2p轨道上有一个电子的自旋方向与2p轨道上其它电子的自旋方向相反
Z
原子核外p电子数比s电子数多l个
W
原子的第一至第四电离能(kJ·mol-1)分别是:I1=578,I2=1817 I3=2745 I4=11575
M
元素的主族数与周期数相差4
G
其基态原子最外层电子数为1,其余各电子层均充满电子
画出W基态原子的核外电子排布图。
-
(3) A2Y的VSEPR模型名称为。
-
(4) 已知为X2Y分子中Y原子只与一个X原子相连,请根据等电子原理,写出X2Y的电子式。
-
(5) X、G形成的某种化合物的晶胞结构如图所示,则其化学式为。
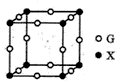
-
(6) 已知Z和M形成的化合物的晶体密度为pg·cm-3 , 阿伏加德罗常效为NA , 该晶体中两个距离最近的Z离子中心间距离为cm。
下列排布不符合泡利原理的是( )
A . 2p能级:  B . 3d能级:
B . 3d能级: 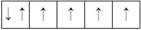 C . 2p能级:
C . 2p能级:  D . 3d能级:
D . 3d能级: 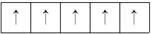
W、X、Y、Z、N是短周期元素,它们的核电荷数依次增大。
|
元素 |
元素性质或原子结构 |
|
W |
原子核内无中子 |
|
X |
在Y的上一周期,原子核外s能级上的电子总数与p能级上的电子总数相等 |
|
Y |
元素的离子半径在该周期中最小 |
|
Z |
原子核外p能级上的电子总数比s能级上的电子总数多2 |
|
N |
最外层电子数比次外层电子数少1 |
-
(1) W单质的化学式为,Z元素原子核外有原子轨道填充了电子。
-
(2) Y、Z和N三种元素第一电离能由大到小的顺序为(填元素符号)。
-
(3) X与Z两元素的电负性较大的是(填元素符号)。
-
(4) Z元素原子共有种不同运动状态的电子。
下列说法中正确的是( )
A . CH4、BCl3、SO2都是含有极性键的非极性分子
B . 甲烷分子失去一个H+ , 形成  ,其碳原子的杂化类型发生了改变
C . SO2和O3、
,其碳原子的杂化类型发生了改变
C . SO2和O3、  和
和 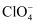 互为等电子体
D . 元素的基态原子核外电子排布都遵循构造原理
互为等电子体
D . 元素的基态原子核外电子排布都遵循构造原理
 ,其碳原子的杂化类型发生了改变
C . SO2和O3、
,其碳原子的杂化类型发生了改变
C . SO2和O3、  和
和 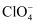 互为等电子体
D . 元素的基态原子核外电子排布都遵循构造原理
互为等电子体
D . 元素的基态原子核外电子排布都遵循构造原理
下列说法错误的是( )
A . ns电子的能量可能低于(n-1)p电子的能量
B . 6C的电子排布式  ,违反了洪特规则
C . 电子排布式(22Ti)ls22s22p63s23p10违反了能量最低原理
D . 电子排布式(22Ti)1s22s22p63s23p10违反了泡利不相容原理
,违反了洪特规则
C . 电子排布式(22Ti)ls22s22p63s23p10违反了能量最低原理
D . 电子排布式(22Ti)1s22s22p63s23p10违反了泡利不相容原理
 ,违反了洪特规则
C . 电子排布式(22Ti)ls22s22p63s23p10违反了能量最低原理
D . 电子排布式(22Ti)1s22s22p63s23p10违反了泡利不相容原理
,违反了洪特规则
C . 电子排布式(22Ti)ls22s22p63s23p10违反了能量最低原理
D . 电子排布式(22Ti)1s22s22p63s23p10违反了泡利不相容原理
下列关于原子结构模型的说法正确的是( )
A . 道尔顿的原子结构模型将原子看作实心球,故不能解释任何问题
B . 汤姆孙的“葡萄干布丁”原子结构模型成功地解释了原子中的正、负粒子是可以稳定共存的
C . 卢瑟福的原子核式结构模型指出了原子核和核外电子的质量关系、电性关系及占有体积的关系
D . 玻尔的电子分层排布原子结构模型引人了量子化的概念,能够成功解释所有的原子光谱
下列与原子核外电子排布规律相关的叙述中(n为能层序数),错误的是( )
A . 第三周期元素的基态原子中,未成对电子数最多的是磷
B . 电子填入能级的顺序是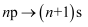 , 因此原子核外最外层电子数一般不超过8
C . 由3d能级有5个轨道可知,元素周期表中第四周期元素比第三周期元素多10种
D . 基态原子的最外层电子排布为ns2的元素,在元素周期表中均位于第ⅡA族
, 因此原子核外最外层电子数一般不超过8
C . 由3d能级有5个轨道可知,元素周期表中第四周期元素比第三周期元素多10种
D . 基态原子的最外层电子排布为ns2的元素,在元素周期表中均位于第ⅡA族
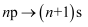 , 因此原子核外最外层电子数一般不超过8
C . 由3d能级有5个轨道可知,元素周期表中第四周期元素比第三周期元素多10种
D . 基态原子的最外层电子排布为ns2的元素,在元素周期表中均位于第ⅡA族
, 因此原子核外最外层电子数一般不超过8
C . 由3d能级有5个轨道可知,元素周期表中第四周期元素比第三周期元素多10种
D . 基态原子的最外层电子排布为ns2的元素,在元素周期表中均位于第ⅡA族
在核电荷数为26的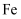 的价层电子排布图中,处于基态的是( )
的价层电子排布图中,处于基态的是( )
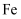 的价层电子排布图中,处于基态的是( )
的价层电子排布图中,处于基态的是( )
A . 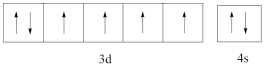 B .
B . 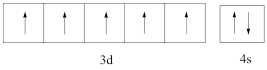 C .
C . 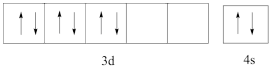 D .
D . 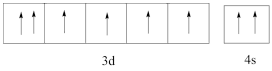
 B .
B .  C .
C .  D .
D . 
磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。回答下列问题:
-
(1) 在周期表中,与Li的化学性质最相似的邻族元素是,该元素基态原子核外M层电子的自旋状态(填“相同”或“相反”)。
-
(2) FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3 , 其中Fe的配位数为。从结构角度来看,Fe2+易被氧化成Fe3+的原因是。
-
(3) NH4H2PO4中P的杂化轨道与O的2p轨道形成键。
-
(4) 磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池的电极材料,磷酸亚铁锂电池总反应为:FePO4+Li
 LiFePO4 , 下列叙述错误的是____。
A . 放电时,Li作负极 B . 电解质溶液为非水溶液体系 C . 充电时铁元素发生还原反应 D . 若用该电池电解饱和食盐水(电解池电极均为惰性电极)当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为1.4g
LiFePO4 , 下列叙述错误的是____。
A . 放电时,Li作负极 B . 电解质溶液为非水溶液体系 C . 充电时铁元素发生还原反应 D . 若用该电池电解饱和食盐水(电解池电极均为惰性电极)当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为1.4g
硼酸和乙醇可以发生酯化反应:B(OH)3+3C2H5OH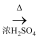 (C2H5O)3B+3H2O。生成的硼酸三乙酯点燃时产生绿色火焰,可通过该现象鉴定硼酸,下列表示正确的是( )
(C2H5O)3B+3H2O。生成的硼酸三乙酯点燃时产生绿色火焰,可通过该现象鉴定硼酸,下列表示正确的是( )
 (C2H5O)3B+3H2O。生成的硼酸三乙酯点燃时产生绿色火焰,可通过该现象鉴定硼酸,下列表示正确的是( )
(C2H5O)3B+3H2O。生成的硼酸三乙酯点燃时产生绿色火焰,可通过该现象鉴定硼酸,下列表示正确的是( )
A . 中子数为8的O原子: B . 乙醇分子的比例模型:
B . 乙醇分子的比例模型: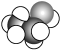 C . 基态C原子核外价电子的轨道表达式:
C . 基态C原子核外价电子的轨道表达式: D . 硼酸在水中的电离方程式:B(OH)3+H2O=B(OH)
D . 硼酸在水中的电离方程式:B(OH)3+H2O=B(OH) +H+
+H+
 B . 乙醇分子的比例模型:
B . 乙醇分子的比例模型: +H+
+H+
下列说法正确的是( )
A .  的空间充填模型:
的空间充填模型: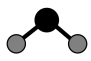 B . 2,3-二甲基丁烷的键线式:
B . 2,3-二甲基丁烷的键线式: C .
C .  的电子式:
的电子式: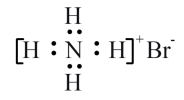 D . 基态N原子的轨道表示式:
D . 基态N原子的轨道表示式: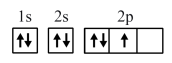
 的空间充填模型:
的空间充填模型: B . 2,3-二甲基丁烷的键线式:
B . 2,3-二甲基丁烷的键线式: 的电子式:
的电子式: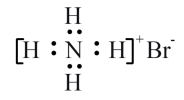 D . 基态N原子的轨道表示式:
D . 基态N原子的轨道表示式:
设 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
A . 1molSi原子含有的未成对电子数为 B . 1mol羟基(
B . 1mol羟基(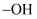 )所含有的电子数为
)所含有的电子数为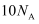 C . 常温下,14g乙烯含有的共用电子对数为
C . 常温下,14g乙烯含有的共用电子对数为 D . 25℃,
D . 25℃,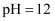 的NaOH溶液中含有
的NaOH溶液中含有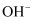 的数目为
的数目为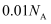
 B . 1mol羟基(
B . 1mol羟基(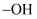 )所含有的电子数为
)所含有的电子数为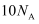 C . 常温下,14g乙烯含有的共用电子对数为
C . 常温下,14g乙烯含有的共用电子对数为 D . 25℃,
D . 25℃,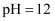 的NaOH溶液中含有
的NaOH溶液中含有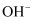 的数目为
的数目为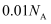
最近更新
- 摩尔质量是指单位物质的量的物质所含有的质量。 (1)已知NH3的相对分子质量为17,则NH3的摩尔质量为________
- 硬水和软水的区别( ) A.硬水中含污染物,软水中无污染物 B.硬水中含较多的可溶性的钙,镁化合物,软水中含有较少
- 如图为用单摆测重力加速度的实验(1)(多选题)为了减小误差,下列措施正确的是(A)摆线长度L应为线长与摆球半径的和,且在
- 小施学校的教学楼有东、南、西、北四扇大门,放学后要求都要将门关上。平时传达室的蒋师傅住在南门,每天都要跑三个地方检查门是
- The boy is Jim.I’m ______ good friend. A.his
- 书面表达(满分25分) 2010年上海世博会即将开幕,作为一名中学生志愿者,你感觉身边还存在许多不文明行为。请你写一篇1
- —What do you think of my marriage? —______, if I were you,
- 在台球比赛中,母球(白色球)必须在碰到其他球之前先碰到目标球,否则将被罚分.现在台面上形成如图所示的局面,目标球为红色球
- 阅读下面的唐诗,然后回答问题。 八月秋高风怒号,卷我屋上三重茅。茅飞渡江洒江郊,高者挂罥长林梢,下者飘转沈塘坳。 南村群
- 下列说法正确的是 A.需要通电才可进行的有:电解、电泳、电离、电镀、电化腐蚀 B.在Fe(OH)3胶体中滴加稀硫酸的现象
- 数列的前n项的和Sn =3n2+ n+1,则此数列的通项公式a n=__ .
- 下图反映了某时期我国公私经济成分的比例情况,这种情况最早应出现于A.1949年 B.1952年
- 14._______on May 12,2008, Wenchuan county has taken on dynam
- “世间苍痍,诗中圣哲;民间疾苦,笔底波澜。”这副对联称颂的是 A.屈原 B. 王维
- 曾主持中国海关总税务司的英国人赫德在其《中国见闻录》中写道:“中国有世界上最好的粮食——大米;最好的饮料——茶;最好的衣
- 先化简 (1+ )÷,然后在0,1,-1中挑选一个合适的数代入求值.
- A recent report found that women graduates are more likely t
- 读下面两段材料,回答33~36题。 我国水能蕴藏量约6.8亿千瓦,主要分布在西南地区。我国电力工业主要有水电和火电两种形
- cos(45°-α)+cos(45°+α)= ________________.
- 一飞机以200 m/s的速度在高空沿水平线做匀速直线飞行.每相隔1 s 先后从飞机上落下A、B、C三个物体.不计空气阻力



